СОВМЕСТНОЕ ОПРЕДЕЛЕНИЕ β-ЦИКЛОДЕКСТРАНА И ПОЛИВИНИЛПИРРОЛИДОНА В МНОГОКОМПОНЕНТНЫХ ПРЕПАРАТАХ МЕТОДОМ ВЭЖХ
Aннотация
Актуальность. Перспективные препараты для лечения целого ряда инфекционных заболеваний наиболее часто представлены многокомпонентными инъекционными лекарственными формами, в состав которых входит набор неорганических солей, антибактериальные и противовирусные вещества, а также вспомогательные вещества, выполняющие роль пролонгаторов и консервантов. От количества этих веществ и их соотношения в составе зависит срок годности препарата и его фармакокинетические характеристики. Цель исследования. Разработка и валидация методики совместного определение β-циклодекстрана и поливинилпирролидона в многокомпонентных препаратах методом высокоэффективной жидкостной хроматографии (ВЭЖХ). Материалы и методы. В данном исследовании осуществлен подбор оптимальных колонки и сорбента для проведения количественного определения ПВП отдельно от β-циклодекстрана методом эксклюзионной хроматографии и выполнена валидация методики по показателям правильность, сходимость (прецизионность), линейность, диапазон применения. В работе использован блочный жидкостный хроматограф модели LC-20 (Shimadzu Co. Япония) и метод хроматографирования с одновременным применением двух колонок. Результаты. Подобраны оптимальные колонки для проведения количественного определения ПВП отдельно от β-циклодекстрана методом эксклюзионной хроматографии. Были выбраны колонки: основная – размером 250 мм х 0.46 мм, заполненная сорбентом Equisil ODS, размер частиц 5 мкм, (производство Dr. Maisch, Германия); защитная – размером 20 мм х 4.0 мм Discovery HS C18, размер частиц 5 мкм (Supelco, США). Заключение. Методика количественного определения и установления подлинности β-циклодекстрана соответствует всем метрологическим требованиям к методике характеризуется достаточной сходимостью и правильностью. Систематическая ошибка методики для каждого определяемого компонента удовлетворяет требованиям практической незначимости.
Ключевые слова: высокоэффективная жидкостная хроматография, β-циклодекстран, поливинилпирролидон, пролонгаторы, консерванты, фармакокинетика, количественное определение
Введение. Условия количественного определения β-циклодекстрана методом ВЭЖХ описаны в монографии “Betadex” Европейской фармакопеи, а также в фармакопеи США и в многочисленных информационно-рекламных материалах фирм, производящих хроматографические колонки. Наиболее полная информация о режимах хроматографирования представлена фирмой “Showa Denko K.K.”., Япония. При количественном определении по методике Европейской фармакопеи применяют колонку, заполненную сорбентом с октадецильными группами, по методике фармакопеи США анализ проводят на колонке с аминными группами. Условия хроматографирования, приведенные в рекламных материалах фирмы “Showa Denko K.K.”, предполагают использование эксклюзионных колонок с рабочим диапазоном, начиная с 3000 дальтон [1, 2].
Поскольку в составе препарата присутствуют различные неорганические ионы и высокомолекулярное соединение – ПВП, применять колонку с аминными группами нельзя ввиду происходящих между сорбентом и компонентами пробы необратимых реакций. Применить эксклюзионный режим хроматогафирования возможно, но при этом на сорбенте, который обеспечивает необходимое разделение ближайших к β-циклодекстрану веществ (ά- и γ-циклодекстранов) получается размытый пик ПВП, который при регистрации на рефрактометрическом детекторе частично, перекрывается с пиком β-циклодекстрана, что существенно ухудшает метрологические характеристики методики. Хроматографирование в условиях монографии “Betadex” Европейской фармакопеи позволяет получить полное разделение хроматографических зон β-циклодекстрана от других компонентов препарата, но при этом время ПВП выхода превышает 120 мин, при том, что время выхода β-циклодекстрана находится в пределах от 5 до 7 мин. Значительное время удерживания ПВП приводит к сильному расширению его хроматографической зоны, при этом чувствительность используемого для регистрации β-циклодекстрана рефрактометрического детектора уже не позволяет получать достоверные результаты количественного содержания ПВП в препарате. А в случае не полного элюирования хроматографической зоны ПВП уже наблюдается невоспроизводимость времен удерживания и площадей пиков β-циклодекстрана из-за модификации сорбента ПВП [3].
Установить время полного элюирования пика ПВП можно проводя одновременно детектирование рефрактометрическим и УФ-ВИД спектрофотометрическим детектором. Использование УФ-ВИД спектрофотометрического детектора позволяет существенно увеличить чувствительность регистрации ПВП, поскольку в УФ спектре этого соединения имеется коротковолновый участок, в котором наблюдается достаточно интенсивное поглощение.
Цель исследования: разработка и валидация методики совместного определение β-циклодекстрана и поливинилпирролидона в многокомпонентных препаратах методом ВЭЖХ.
Задачи исследования:
1. Подбор оптимальных колонки и сорбента для проведения количественного определения ПВП отдельно от β-циклодекстрана методом эксклюзионной хроматографии
2. Валидация методики по показателям правильность, сходимость (прецизионность), линейность, диапазон применения.
Материалы и методы исследования. При разработке данной методики и проведение валидационных исследований использовали блочный жидкостный хроматограф модели LC-20 (Shimadzu Co. Япония) в следующей комплектации:
- два насоса высокого давления модели LC 20 ADvp;
- автоинжектор SIL-20A
- термостат колонок CTO-20A в термостат, в которого вмонтирован 6 ти портовой кран высокого давления FCV-12AH2
- рефрактометрический детектор RID-10A;
- спектрофотометрический детектор SPD-20A.
Испытуемый раствор препарата готовят путем его разбавления в воде или подвижной фазе, чтобы получить концентрацию β-циклодекстрана и ПВС на уровне около 10 мг/мл и 3 мг/мл соответственно.
Отдельно готовят раствор сравнения β-циклодекстрана и раствор сравнения ПВП с теми же концентрациями.
По 20 мкл испытуемого раствора и раствора сравнения β-циклодекстрана и раствора сравнения ПВП хроматографируют.
Условия хроматографирования:
- основная колонка – размером 250 мм х 0,46 мм, заполненная сорбентом Equisil ODS, размер частиц 5 мкм, (производство Dr. Maisch, Германия);
- защитная колонка – размером 20 мм х 4,0 мм Discovery HS C18, размер частиц 5 мкм (Supelco, США);
- подвижная фаза: вода – метанол (90 : 10);
- скорость подачи подвижной фазы через основную колонку – 1 мл/мин;
- скорость подачи подвижной фазы через защитную колонку – 2 мл/мин;
- длина волны детектирования УФ-ВИД детектором – 226 нм;
- температура термостата колонок – 30 оС;
Концентрацию β-циклодекстрана или ПВС в испытуемом растворе (Сi) определяют по формуле:
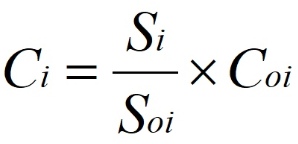
где: Si – среднее значение площадей пиков β-циклодекстрана или ПВП, рассчитанное из хроматограмм испытуемого раствора;
Soi – среднее значение площадей пиков β-циклодекстрана или ПВП, рассчитанное из хроматограмм раствора сравнения β-циклодекстрана или раствора сравнения ПВП;
Coi – концентрация β-циклодекстрана или ПВП в соответствующем растворе сравнения, в миллиграммах в 1 мл.
Для устранения негативного влияния ПВП на результаты анализа автором была предложено проводить хроматографирование проб содержащих β-циклодекстран и ПВП с использованием двух колонок подключенных к 6-ти портовому крану, расположенному в термостате колонок [4]. Одна из колонок выполняет защитную функцию и предотвращает попадание ПВП во вторую, а вторая колонка служит для отделения β-циклодекстрана от других компонентов препарата. Схема подключения колонок показана на рис. 1:
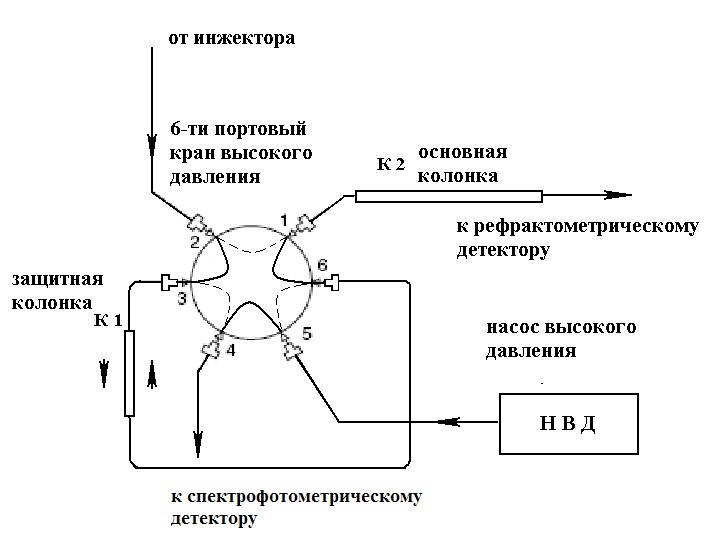
Рис. 1. Схема подключения колонок к 6-портовому крану
Fig. 1. The scheme of connecting the columns to the 6-port tap
Как видно из рис.1, принцип работы этой схемы заключается в том, что в момент введения 6-ти портовый кран находится в положении показанном сплошными линиями на рис. 1 и все компоненты пробы попадают в защитную колонку К1, в которой происходит разделение ПВП от остальных веществ, включая и β-циклодекстран. Скорость продвижения хроматографической зоны ПВП по колонке 1 составляет около 1 мм/мин и за время нахождения 6-ти портового крана в этом положении (1.5 мин) успевает пройти около 1.5 мм. После переключения 6-ти портового крана поток подвижной фазы направляется в основную колонку К2 уже минуя защитную колонку, а в защитную колонку отдельным насосом подается подвижная фаза в противоположном направлении. Хроматографическая зона ПВП из защитной колонки элюируется и попадает в УФ-ВИД спектрофотометрический детектор, где и происходит ее регистрация. При прохождении подвижной фазы по колонке в обратном направлении происходит фокусировка хроматографической зоны ПВП, за счет чего пик ПВП получается достаточно симметричным.
В основной колонке происходит разделение пиков β-циклодекстрана от остальных компонентов препарата и хроматографическая зона β-циклодекстрана регистрируется рефрактометрическим детектором. Таким образом при одном введении пробы испытуемого раствора происходит определение и β-циклодекстрана, и ПВП. Время хроматографирования составляет около 10 мин.
Результаты и их обсуждение. Методики с переключением потоков подвижной фазы и предварительным отделением от других компонентов препарата и концентрированием определяемых веществ в непосредственно ходе проведения анализа мало распространенны в практике фармацевтического анализа [6, 7].
Разработанная методика идентификации и количественного определения β-циклодекстрана и ПВП была исследована по показателям: «специфичность», правильность; прецизионность (сходимость), линейность, диапазон применения. Исследования проводили на модельных образцах, полученных в лабораторных условиях с использованием двух вариантов раствора «плацебо» препарата. В первом случае – без β-циклодекстрана, а во втором – без ПВП. Соответствие методики требованиям по показателю специфичность подтверждается следующими данными:
1. На хроматограмме раствора плацебо и хроматограмме растворителя отсутствуют пики со временем удерживания, совпадающим со временем удерживания пиков бетадекса на хроматограмме испытуемого раствора. То есть, все остальные компоненты препарата и растворитель не мешают проведению испытаниям на подлинность и количественному определению β-циклодекстрана.
2. На хроматограмме раствора для проверки пригодности хроматографической системы наблюдается полное разделение пиков бетадекса и пиков его ближайших аналогов – α-циклодекстрана и γ-циклодекстрана.
3. Доверительные интервалы времен удерживания пиков β-циклодекстрана на хроматограммах испытуемого раствора и доверительные интервалы времён удерживания пиков β-циклодекстрана на хроматограммах суммарного раствора сравнения перекрываются, т.е. не имеют статистически значимой ошибки. Значения времен удерживания пиков β-циклодекстрана представлены в таблице 1.
Таблица 1
Значения времен удерживания пиков β-циклодекстрана на хроматограммах испытуемого раствора препарата и раствора сравнения β-циклодекстрана
Table 1
The retention times of β-cyclodextran peaks on the chromatograms of the test solution
and the β-cyclodextran comparison solution
№ хроматограмм | Значения времен удерживания | |
Испытуемый раствор | Раствор сравнения | |
1 | 8.664 | 8.645 |
2 | 8.638 | 8.657 |
3 | 8.639 | 8.648 |
4 | 8.651 | 8.647 |
5 | 8.637 | 8.654 |
Среднее значение | 8.646 | 8.650 |
ОСО | 0.136 | 0.059 |
Макс. значение | 8.664 | 8.657 |
Минимальное значение | 8.637 | 8.645 |
Доверительный интервал | 0.012 (от 8.634 до 8.658) | 0.005 (от 8.645 до 8.655) |
Требование к перекрыванию доверительных интервалов значений времен удерживания пиков определяемых веществ на хроматограммах испытуемого раствора и раствора сравнения представляется более правильным, чем обычно указываемое в НД требование о 2 % совпадении времен удерживания. Поскольку возможен случай, когда доверительные интервалы могут не перекрываться, при этом попадать в 2 %
диапазон.
Проведение идентификации по совпадению времен удерживания по разработанной методике для ПВП не корректно, поскольку роль защитной хроматографической колонки сводится только к отделению хроматографической зоны ПВП от других компонентов препарата, и время удерживания зависит от времени переключения 6-ти портового крана.
Данные о других метрологических характеристик методики были получены путем хроматографирования модельных растворов с концентрацией ПВП и β-циклодекстрана от 80 % до 120 % от номинального значения. Результаты хроматографирования модельных растворов и расчет метрологических характеристик методики при определении β-циклодекстрана и ПВП представлены в таблицах 2 и 3.
Таблица 2
Результаты анализа модельных смесей препарата, содержащих от 80% до 120 %
по отношению к номинальной концентрации β-циклодекстрана,
и их статистическая обработка
Table 2
The results of the analysis of model mixtures of the preparation containing from 80% to 120% with respect to the nominal concentration of β-cyclodextran and their statistical treatment
№ раствора | Введено в % от номинальной концентрации (Xi, факт., %) | Найдено в % от номинальной концентрации (Yi, %) | Найдено в % к введенному Zi = 100 • (Yi/Xi) |
1 | 79.740 | 79.709 | 99.962 |
2 | 85.000 | 84.789 | 99.752 |
3 | 89.942 | 89.783 | 99.823 |
4 | 94.855 | 94.495 | 99.620 |
5 | 100.231 | 100.291 | 100.060 |
6 | 104.913 | 104.508 | 99.614 |
7 | 110.087 | 109.913 | 99.842 |
8 | 114.827 | 114.364 | 99.597 |
9 | 120.202 | 118.748 | 98.790 |
Среднее, Zср, % = | 99.673 | ||
Относительное стандартное отклонение, RSDz, % = | 0.369 | ||
Относительный доверительный интервал Δz % = t (95 %, 9 – 2) x RSDz = 2.36 x 0.369 = | 0.87 | ||
Критическое значение для сходимости результатов ΔAs, % = | 1.6 | ||
Систематическая ошибка d % = | Zср – 100 | = | 0.327 | ||
Критерий незначимости систематической ошибки: |
| ||
1) статистическая незначимость: d < Δz : √9 = 0.87 : 3 = 0.29 % < 0.327 % | Не выполняется | ||
Если не выполняется 1), то d ≤ max d: 2) практическая незначимость: δ % ≤ 0.32 ´ 1,6 = 0.501 % > 0.327 % | Выполняется | ||
| Корректна | ||
Из данных, приведенных в табл. 2, следует, что методика количественного определения β-циклодекстрана и ПВП характеризуется достаточной правильностью и сходимостью (прецизионностью) во всем диапазоне концентраций, является корректной и не имеет практически значимой систематической ошибки.
Характеристику «Линейность» исследовали в диапазоне концентраций бетадекса от 80 % до 120 % по отношению к номинальному значению.
Графики линейной зависимости найденного количества бетадекса от введенного для представлен на рис.2, а результаты расчета параметров линейной зависимости – в таблице 3.
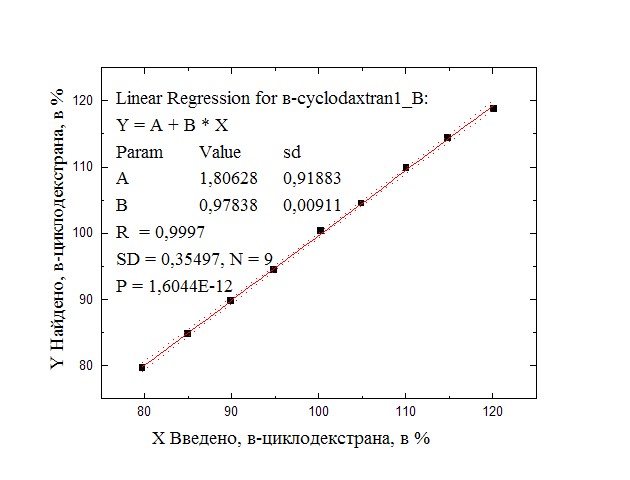
Рис. 2. График линейной зависимости найденного количества β-циклодекстрана от введенного
Fig. 2. The graph of the linear dependence of the found amount of β-cyclodextran on the introduced amount
Таблица 3
Метрологические характеристики линейной зависимости найденной концентрации
β-циклодекстрана от его введенной концентрации
Table 3
Metrological characteristics of the linear dependence of the found concentration
of β-cyclodextran on its administered concentration
Параметры | Значения | Требования 1 | Требования 2 | Заключение |
b | 0.97838 |
|
|
|
Sb | 0.00911 |
|
|
|
a | 1.80628 | >|0.900| | |2.6| | Выдерживается по 2 критерию |
Sa | 0.91883 |
|
|
|
RSD0 | 0.35497 |
|
|
|
RSD0/b | 0.363 | <|0.84| |
| Выполняются |
r | 0.9997 | >|0.9980| |
| Выполняются |
Выводы
1. Подобраны оптимальные колонки для проведения количественного определения ПВП отдельно от β-циклодекстрана методом эксклюзионной хроматографии. Были выбраны колонки: основная – размером 250 мм х 0.46 мм, заполненная сорбентом Equisil ODS, размер частиц 5 мкм, (производство Dr. Maisch, Германия); защитная – размером 20 мм х 4.0 мм Discovery HS C18, размер частиц 5 мкм (Supelco, США);
2. Проведена валидация методики по показателям правильность, сходимость (прецизионность), линейность, диапазон применения.
Методика количественного определения β-циклодекстрана и ПВП характеризуется достаточной правильностью и сходимостью (прецизионностью) во всем диапазоне концентраций, является корректной и не имеет практически значимой систематической ошибки.
Характеристику «Линейность» исследовали в диапазоне концентраций бетадекса от 80% до 120% по отношению к номинальному значению.
Методика количественного определения и установления подлинности β-циклодекстрана соответствует всем метрологическим требованиям к методике характеризуется достаточной сходимостью и правильностью. Систематическая ошибка методики для каждого определяемого компонента удовлетворяет требованиям практической незначимости.
Высокое значение коэффициента корреляции r = 0.9997 удовлетворяет требованиям критерия приемлемости (r = 0.9980) и подтверждает линейность зависимости между взятым и найденным количеством каждого из действующих веществ препарата в области от 80 % до 120 % относительно их номинальных концентраций в препарате.
Выполняются требования к параметрам линейной зависимости (а, RSD0/b, r) методики определения β-циклодекстрана во всем диапазоне концентраций от 80% до 120% от номинального значения.
В отношении данной статьи не было зарегистрировано конфликта интересов.




















Список литературы