Ценность определения концентраций кальцидиола и сосудисто-эндотелиального фактора роста для прогнозирования неразвивающейся беременности
Aннотация
Актуальность: Неразвивающаяся беременность – одна из наиболее сложных медико-социальных проблем современного акушерства и гинекологии, не имеющая тенденции к снижению. Перенесенная неразвивающаяся беременность является предиктором неблагоприятных исходов последующих беременностей, вплоть до привычного невынашивания. Неразвивающаяся беременность является многофакторным и полиэтиологическим осложнением гестации, что диктует необходимость комплексной оценки вероятности возникновения патологического состояния в каждом конкретном случае. Цель исследования: Оценка факторов, способствующих формированию неразвивающейся беременности, для выявления пациенток группы риска. Определение статуса витамина D и концентрации СЭФР в плазме крови пациенток с неразвивающейся беременностью как информативных маркеров для прогнозирования патологического состояния. Материалы и методы: В исследовании приняли участие 116 пациенток: 76 пациенток с неразвивающейся беременностью и 40 – с физиологически протекающей беременностью. Собраны сведения о репродуктивном и соматическом здоровье женщин, их социальном статусе. Были исследованы уровни невротизации и тревожности – шкалы Хека и Хесса и Ч.Д. Спилберга, Ю.Л. Ханина. Определены типы акцентуации темперамента согласно тесту Г. Шмишека и К. Леонгарда. Уровень перинатального риска был определен по шкале В.Е. Радзинского, С.А. Князева, И.Н. Костина (2011). Иммуноферментный анализ 25-OH Vitamin D плазмы крови проводили с использованием набора реагентов ELISA, EUROIMMUN AG (Германия), СЭФР - human VEGF-A ELISA с применением реактивов фирмы Thermo Fisher Scientific (США). Результаты: Определены факторы, способствующие развитию изучаемого патологического состояния. Установлено, что дефицит витамина D является фактором риска возникновения неразвивающейся беременности. При снижении концентрации кальцидиола плазмы ниже 10 нг/мл вероятность развития неразвивающейся беременности увеличивается в 4.74 раз. Уровень СЭФР у пациенток с неразвивающейся беременностью в 5.1 раза выше по сравнению с показателем группы контроля. Заключение: Определение статуса витамина D и концентрации СЭФР является дополнительным диагностическим методом, позволяющим прогнозировать вероятность возникновения неразвивающейся беременности. Выявление пациенток группы риска по формированию неразвивающейся беременности возможно при помощи тщательного сбора анамнеза, выяснения социальных факторов, способствующих возникновению патологического состояния и оценки психоэмоционального статуса. Пациенткам группы риска по формированию изучаемого осложнения гестации целесообразно определение уровня кальцидиола плазмы с целью своевременной коррекции гиповитаминоза.
Введение. Невынашивание беременности, в частности неразвивающаяся беременность, по-прежнему остается одной из наиболее острых проблем практического акушерства. Несмотря на многочисленные эффективные методы диагностики и лечения, разработанные в последнее время, статистика репродуктивных потерь не имеет тенденции к снижению [1, 2]. Из общего числа клинически установленных беременностей самопроизвольно прерываются около 25%, невынашивание в анамнезе – предиктор неблагоприятных перинатальных исходов. Профилактика репродуктивных потерь и улучшение перинатальных исходов – важнейшие направления исследований в сфере акушерства и гинекологии.
Неразвивающаяся беременность – одна из наиболее сложных медико-социальных проблем современного акушерства и гинекологии. В структуре невынашивания частота данной патологии достаточно высока (45-88,6%), а традиционное лечение малоэффективно, так как в большинстве случаев точные этиопатогенетические факторы, способствующие остановке развития беременности, остаются неустановленными [2].
Неразвивающаяся беременность является многофакторным и полиэтиологическим осложнением гестации, что диктует необходимость комплексной оценки вероятности возникновения патологического состояния в каждом конкретном случае. В последние годы обсуждаются роли витамина D и сосудисто-эндотелиального фактора роста (СЭФР) в инициации и поддержании физиологической беременности, в связи с чем интересна их оценка и при патологическом течении гестации [3, 4, 5, 6, 7].
Причин, приводящих к возникновению неразвивающейся беременности великое множество. К основным относятся анатомические изменения и функциональные нарушения маки, эндокринные нарушения (недостаточность лютеиновой фазы, гиперандрогения, синдром поликистозных яичников, гипотиреоз, аутоиммунный тиреоидит, ожирение), тромбофилические факторы (мутации в генах фактора V, протромбина, фермента метилентетрагидрофолатредуктазы, генетически обусловленный дефицит антитромбина III, протеинов С и S), аутоиммунные нарушения (антифосфолипидный синдром, аутосенсибилизация к хорионическому гонадотропину, прогестерону), генетическая патология, инфекционные причины, приводящие впоследствии к хроническому эндометриту или синдрому регенераторно-пластической недостаточности эндометрия, соматические заболевания матери, мужской фактор. Выделяют также ряд социальных факторов, способствующих развитию неразвивающейся беременности: возраст матери старше 30 лет, отца – старше 40, неправильное питание, вредные привычки, несоблюдение режима труда и отдыха, работа в ночные смены, употребеление кофеина в высоких дозах [8-16].
В последнее время говорят о дефиците витамина D, как о независимом факторе риска осложнений беременности. По данным Е.С. Шелеповой, концентрация кальцидиола в сыворотке крови матери в первом триместре беременности ниже 50 нмоль/л ассоциирована с увеличением частоты самопроизвольного прерывания беременности более чем в два раза [17]. Дефицит витамина D установлен у 77-98% пациенток, страдающих бесплодием. Согласно результатам, полученным X. Zhao et al. (2017), необходимым условием полноценного формирования фетоплацентарного комплекса является концентрация кальцидиола плазмы не ниже 40 нг/мл [18].
В Российской Федерации распространенность гиповитаминоза D, по данным разных исследователей, варьирует от 45 до 98%, причем чаще страдают женщины репродуктивного возраста, в группе риска беременные и кормящие.
Российская ассоциация эндокринологов классифицирует концентрацию кальцидиола в крови ниже 20 нг/мл как дефицит, ниже 10 нг/мл – тяжелый дефицит, а от 20 до 30 нг/мл – как недостаточность [19].
Положительное влияние витамина D на репродуктивную функцию обусловлено его внескелетными эффектами: участием в стероидогенезе прогестерона, эстрадиола, антимюллерова гормона, иммуномодуляторным действием за счет способности снижать цитотоксичность натуральных киллеров и уменьшать продукцию провоспалительных цитокинов. Витамин D способен воздействовать на транскрипцию генов сосудисто-эндотелиального фактора роста, стимулируя ангиогенез [20, 21].
Дефекты ремоделирования сосудов децидуальной ткани и дифференцировки трофобласта ассоциированы с тяжелыми гестационными осложнениями, включая неразвивающуюся беременность. СЭФР играет важную роль в ангиогенезе и развитии плаценты. Было установлено, что у женщин с неразвивающейся беременностью экспрессия его в ворсинах хориона и децидуальной оболочке значительно ниже в сравнении с женщинами с физиологическим течением беременности [21]. Наличие патологического аллеля 936Т гена СЭФР увеличивает вероятность формирования неразвивающейся беременности [20].
Во время эмбрионального развития СЭФР является сигнальным цитокином, который стимулирует васкулогенез и ангиогенез. Инвазия трофобласта в материнские спиральные артерии приводит к созданию циркуляции с высоким потоком и низким сосудистым сопротивлением. Это обеспечивается за счет продукции вазоактивных веществ, таких как СЭФР и, в меньшей степени плацентарный фактор роста, которые вызывают ангиогенез и активируют эндотелиальную синтетазу окиси азота, приводящую к образованию оксида азота, расширяющего сосуды. Недостаточная инвазия трофобласта приводит к снижению плацентарной перфузии и окислительному стрессу, а также продукции провоспалительных цитокинов. СЭФР индуцирует пролиферацию и миграцию эндотелиальных клеток, снижает их апоптоз, увеличивает сосудистую проницаемость и ускоряет протеолиз, обеспечивает децидуализацию, имплантацию и плацентацию. При снижении экспрессии СЭФР увеличивается сопротивление сосудов матки, угнетается плацентарный ангиогенез, снижается кровоснабжение, что приводит к гибели эмбриона или фетоплацентарной недостаточности [4, 20, 21].
Учитывая важность вышеперечисленных функции витамина D и СЭФР и наличие литературных данных, свидетельствующих об изменении их концентраций при осложнениях гестации, их количественное определение представляет научный интерес.
Материалы и методы. В исследовании приняли участие 116 пациенток: 76 пациенток с неразвивающейся беременностью (основная группа) и 40 – с физиологически протекающей беременностью, обратившихся в БУЗ ВО «ВГКБ№3» для прерывания беременности (группа контроля). Срок гестации варьировал от 5 до 11,5 недель. Длительность нахождения погибшего эмбриона/плода не превышала 7 дней, что было подтверждено данными УЗ-диагностики.
Всем женщинам, обратившимся в стационар за медицинской помощью, был произведен в полном объеме стандарт обследования и оказания помощи с учетом нозологии (согласно приказу №572 н) и дополнительно осуществлен забор крови для иммуноферментного анализа.
Были собраны сведения о репродуктивном здоровье женщины (начале и характере менструальной функции, количестве половых партнеров, перенесенных заболеваниях, предшествующих беременностях, наличии абортов и внутриматочных вмешательств), соматическом статусе и семейной предрасположенности к наличию экстрагенитальных заболеваний, социальном уровне (образование, бытовые условия, качество питания, взаимоотношения с партнером, условия труда и наличие профессиональных вредностей). Проводилось анкетирование согласно специально разработанным для научного исследования опросникам. Были исследованы уровни невротизации и тревожности – шкалы Хека и Хесса и Ч.Д. Спилберга, Ю.Л. Ханина. Определены типы акцентуации темперамента согласно тесту Г. Шмишека и К. Леонгарда. Уровень перинатального риска был определен по шкале перинатального риска В.Е. Радзинского.
Определение 25-OH витамина D плазмы крови и СЭФР проводилось на базе лаборатории ООО «Новые медицинские технологии» с использованием иммуноферментных наборов: ELISA, EUROIMMUN AG (Германия, Регистрационное удостоверение № ФСЗ 2012/12311 от 07.06.2012 г.) и human VEGF-A ELISA с применением реактивов фирмы Thermo Fisher Scientific (США).
Результаты и их обсуждение. Возраст пациенток обеих групп был сопоставим, составив 29,99±0,5 лет в основной группе и 29,83±0,5 лет – в контрольной. Возраст полового партнера старше 40 лет в основной группе был установлен в 25% случаев, в группе контроля – в 12,5% (р<0,05).
Средний срок остановки развития беременности составил 6,93 и 7,83 недели соответственно.
В основной группе 48 пациенток рожавшие (63,16%), 72,92% из них имели одни роды в анамнезе, 27,18% – повторные. Родоразрешение путем кесарева сечения составил 35,42%, родов, осложненных инструментальным контролем полости матки – 6,25%. В анамнезе 33 (43,42%) женщин с неразвивающейся беременностью установлены медицинские аборты, у 14 из них – повторные (42,42%). В группе контроля 37 (92,5%) рожавших женщин, из них 72,97% имело в анамнезе двое и более родов. Аборты имело 47,5% пациенток, два и более – 31,58% из них. Родоразрешение путем кесарева сечения встречалось в 21,62% случаев (р<0,05).
Избыточную массу тела имели 11,84% пациенток основной группы, ожирение I степени – 10,53%. В группе контроля ИМТ не превышал 30, ИМТ свыше 25 встречался в 7,5% случаев (р<0,05).
Была исследована заболеваемость пациенток общими и гинекологическими заболеваниями. В основной группе была установлена более высокая частота эндокринной патологии (23,68% против 7,5%), заболеваний сердечно-сосудистой системы (28,95% против 12,5%), заболеваний кроветворной системы (15,79% против 7,5%), воспалительных заболеваний органов мочевыделительной системы (14,47% против 10%), аллергических реакций (23,68% против 12,5%), заболеваемости в детском возрасте, установленной анамнестически (38,16% против 15%). Частота заболеваемости дыхательной и пищеварительной систем была сопоставима. Однако пациентки основной группы болели ОРВИ за последний год в 1,5 раза чаще (р<0,05) (рисунок 1). Интересно отметить, что и заболеваемость родственников первой линии также была выше.
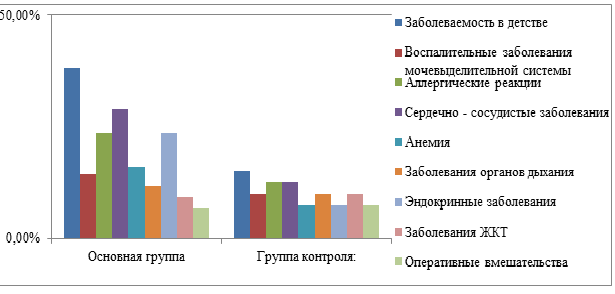
Рис. 1. Заболеваемость обследованных женщин по группам
Fig. 1. The incidence of diseases in the examined women in groups
Несвоевременное менархе в основной группе анамнестически установлено у 18,42% пациенток основной группы и у 2,5% пациенток группы контроля. Раннее начало половой жизни выявлено у 39,47% женщин в основной группе и у 22,50% – в группе контроля. В качестве метода контрацепции 6,58% пациенток из группы женщин с неразвивающейся беременностью использовали внутриматочные контрацептивы. Изменения вагинального биоценоза установлено в 69,74% случаев в основной группе и в 27,50% - в контрольной (р<0,05).
Нарушения менструального цикла имели 18,42% пациенток основной группы и 5% – в контрольной, заболеваемость миомой матки – 18,42% и 10%, воспалительными заболеваниями органов малого таза - 63,16% и 33% соответственно (р<0,05). Распространенность эндометриоза была сопоставима. Женщины группы контроля в анамнезе не страдали бесплодием и не переносили оперативных вмешательств на органах малого таза за исключением операций кесарева сечения и абортов (рисунок 2).
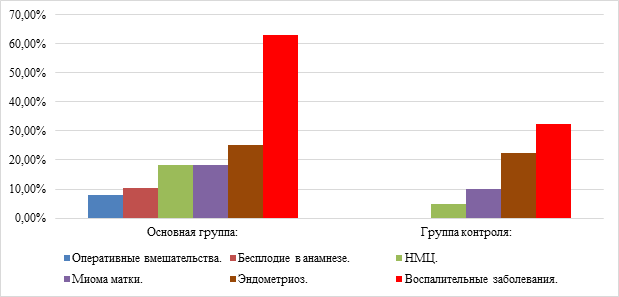
Рис. 2. Структура гинекологической заболеваемости
Fig. 2. Тhe structure of gynecological morbidity
Средняя степень риска перинатальной патологии по шкале Радзинского В.Е., Князева С.А., Костина И.Н., 2009 в основной группе была выявлена у 43,42% женщин, тогда как в группе контроля – 12,50% (р<0,05).
Большая часть женщин основной группы являлись работниками умственного труда и имели высшее образование, тогда как в группе контроля преобладали пациентки со средним образованием, работали только 32,5%. Взаимоотношения с партнером, материальная обеспеченность, социальное положение, отношения с родственниками, согласно опросу, были лучше у пациенток основной группы. Воздействие стрессовых факторов было выражено интенсивно как в группе контроля, так и в основной группе. В то же время высокий уровень невротизации установлен у 40,8% пациенток основной группы и у 7,5% – группы контроля (р<0,05). Аналогичные показатели личностной тревожности были установлены и по шкале тревоги Спилберга-Ханина. В основной группе, согласно опроснику Г. Шмишека, К. Леонгарда, 27,63% женщин имели тревожный, экзальтированный и эмотивный типы акцентуации темперамента, тогда как в группе сравнения данные типы акцентуаций были установлены лишь у 7,5% женщин (р<0,05).
Высокий уровень соматической и гинекологической заболеваемости, несвоевременное менархе, раннее начало половой жизни, наличие в анамнезе внутриматочных вмешательств, различные варианты нарушений микрофлоры влагалища и использование внутриматочной контрацепции, а также возраст отца старше 40 лет являются факторами риска возникновения неразвивающейся беременности. Высшее образование, умственный характер труда, высокие уровни тревожности и невротизации благоприятствуют развитию осложнений гестации. При этом в исследовании не было выявлено увеличения вероятности развития неразвивающейся беременности с худшей материальной обеспеченностью, фактом отсутствия замужества, плохими взаимоотношениями пациенток с партнерами и родственниками.
В сравниваемых группах были определены средние значения кальцидиола и СЭФР, результаты приведены в таблице 1.
Таблица 1
Результаты иммуноферментного исследования биологических жидкостей пациенток основной группы и группы контроля
Table 1
Results of enzyme immunoassay of biological fluids of patients in the main group and control group
Определяемый ИГХ – показатель | Основная группа (n=76) | Группа контроля (n=40) |
25-OH Vitamin D плазмы (ELISA, EUROIMMUN AG), нг/мл | 18,02±1,11* | 31,41±1,66 |
Сосудисто-эндотелиальный фактор роста (human VEGF-A ELISA), пг/мл | 156,73±3,40* | 30,73±4,47 |
Примечание: *достоверность различий между группами, p*<0,05 Note: *significance of differences between groups, p*<0.05
| ||
Гиповитаминоз D был установлен у 92,1% пациенток основной группы и у 62,5% женщин группы контроля: уровень кальцидиола плазмы менее 10 нг/мл был выявлен у 32,89% женщин основной группы, в группе контроля – у 12,5%, от 10 до 20 нг/мл – у 34,21% и у 25% женщин соответственно (р<0,05) (рисунок 3).
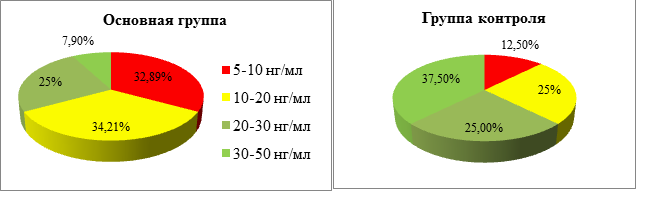
Рис. 3. Концентрация кальцидиола в исследуемых группах
Fig. 3. Calcidiol concentration in the studied groups
Был произведен рассчет вероятности формирования неразвивающейся беременности в зависимости от концентрации кальцидиола плазмы. Установлено, что снижение кальцидиола плазмы ниже 10 нг/мл увеличивает вероятность развития неразвивающейся беременности в 4,74 раз (р<0,05).
Исследование подтверждает имеющиеся литературные данные о распространенности гиповитаминоза и влиянии дефицита витамина D на прогноз беременности, что свидетельствует о важности исследования кальцидиола плазмы и своевременной профилактики дефицита и недостаточности [19]. Положительное воздействие витамина D на течение беременности объясняется его противовоспалительным и иммуномодулирующим эффектами, а также способностью регулировать ангиогенез, за счет влияния на транскрипцию генов сосудисто-эндотелиального фактора роста.
Уровень СЭФР у пациенток с неразвивающейся беременностью оказался в 5,1 раза выше по сравнению с показателем группы контроля (р<0,05). Аналогичные данные были получены Лигидовой А.Т. (2011) при угрожающем выкидыше в первом триместре, где повышение уровня СЭФР ассоциировано с усилением роста сосудов хориона [14]. Повышение СЭФР является следствием активации компенсаторно-приспособительных реакций в ответ на гипоксию, сопровождающую развитие неразвивающейся беременности, направленной на усиление ангиогенеза.
Заключение. Выявление пациенток группы риска по формированию неразвивающейся беременности возможно при помощи тщательного сбора анамнеза, выяснения социальных факторов, способствующих возникновению патологического состояния и оценки психоэмоционального статуса.
Определение статуса витамина D и концентрации СЭФР является дополнительным диагностическим методом, позволяющим прогнозировать вероятность возникновения неразвивающейся беременности. При снижении концентрации кальцидиола плазмы ниже 10 нг/мл вероятность развития неразвивающейся беременности увеличивается в 4,74 раз (р<0,05). Повышение уровня СЭФР следует расценивать как компенсаторно-приспособительную реакцию в ответ на гипоксию.
Пациенткам группы риска по формированию изучаемого осложнения гестации целесообразно определение уровня кальцидиола плазмы и своевременная коррекции гиповитаминоза с целью устранения управляемого фактора риска неразвивающейся беременности – дефицита витамина D.
В отношении данной статьи не было зарегистрировано конфликта интересов.





















Список литературы