Клинический случай синдрома Протея у ребенка раннего возраста
Aннотация
Несмотря на несомненный прогресс медицинской науки во всем мире, за последнее время отмечается тенденция увеличения частоты встречаемости врожденных пороков развития и наследственных заболеваний у детей. Поэтому знание симптоматики различных наследственных синдромов у детей определяют диагностику и тактику дальнейшей терапии, что имеет большое значение не только для прогноза течения заболевания, но и качества дальнейшей жизни пациента. В статье представлен клинический случай синдрома Протея (СП) у ребенка раннего возраста на фоне врожденного порока развития мозга (гемимегалэнцефалии слева). По результатам УЗИ-скрининга во второй половине беременности у матери ребенка были выявлены множественные врожденные пороки развития ЦНС у плода. После рождения пациент наблюдался в отделении патологии новорожденных, где впервые был выставлен диагноз: синдром Протея на фоне врожденной аномалии головного мозга. С 2-месячного возраста у ребенка наблюдались приступы в виде инфантильных спазмов. А в возрасте 6 месяцев на ЭЭГ определены изменения эпилептиформного характера. Постоянно получает противосудорожную терапию. В возрасте 8 месяцев в НИИ нейрохирургии им. акад. Н.Н. Бурденко ему была проведена операция – анатомическая гемисферэктомия слева. После оперативного лечения больной был выписан в удовлетворительном состоянии с основным клиническим диагнозом: врожденный порок развития мозга (гемимегалэнцефалия слева), симптоматическая фокальная левополушарная фармакорезистентная эпилепсия. На фоне противосудорожной терапии судороги не возникали. В 1год 2 месяца был обследован и консультирован врачом-генетиком в Медико-генетическом научном центре г. Москва, где было дано заключение: учитывая результаты геномного секвенирования, вероятнее всего, у ребенка имеет место Proteus-like синдром. Врожденный средний меланоцитарный невус. Пациент является инвалидом с грубой задержкой нервно-психического развития. Планируется удаление образования левой щеки с обязательным гистологическим исследованием.
Введение. За последнее время во многих странах мира отмечается рост врожденных пороков развития у детей. Эта проблема является довольно серьёзной, так как нередко множественные пороки развития у детей вызваны хромосомными мутациями, причем в большинстве случаев это мутации de novo [1]. Мутация de novo – это изменение в гене, которое возникло впервые у одного из членов семь и как результат мутации в зародышевой клетке у одного из родителей или в уже оплодотворенной яйцеклетке. Такие мутации могут привести к различным серьезным врожденным расстройствам мозга: аутизм, эпилепсия, шизофрения и пр.
Синдром Протея (СП) относится к редким генетическим заболеваниям с довольно трудной генетической идентификацией [2-6]. Частота встречаемости данного заболевания – менее 1 случая на 1 млн. населения. В настоящее время в мире зарегистрировано около 100 случаев синдрома Протея у детей различного возраста [7]. Он впервые был описан M.M. Cohen и P.W. Hayden в 1979г. [8]. Многие ученые считают, что причина возникновения СП вызвана летальной доминантной соматической мутацией, происходящей в постзиготной стадии развития эмбриона.
Клинические проявления СП сходны с некоторыми наследственными заболеваниями у детей [6, 9, 10]. СП характеризуется прогрессирующим разрастанием различных тканей организма с преимущественно асимметричной макродактилией, соединительнотканными и эпидермальными невусами, врожденными пороками развития кровеносных и лимфатических сосудов, гиперостозом костей черепа [6, 11-13]. СП характеризуется чрезмерным асимметричным ростом тканей, который начинается чаще после 6-18 мес. жизни и быстро прогрессирует. Так называемый «симптом мокасин» проявляется в виде липом или атрофии жировой ткани, капиллярных, артериальных, венозных мальформаций, асимметричного роста отдельных частей тела за счет костной ткани, разрастания невусов, кист легкого [1, 2, 6].
В качестве примера представлен клинический случай течения СП у ребенка в возрасте 1 года и 8 месяцев жизни на фоне врожденного порока развития мозга (гемимегалэнцефалии слева). Отмечены основныеэтапы диагностикиСПу пациента, представленыклинические особенности течениязаболевания и наблюдения за больным пациентом в динамике.
Клинический случай. Ребенок Е. в возрасте 1 года 8 месяцев жизни поступил в отделение приемного покоя ОГБУЗ «Детской областной клинической больницы» (ДОКБ) г. Белгорода 27.02.2017 г. с жалобами на повышение Т0тела до 38оС, малопродуктивный кашель, слизистые выделения из носа. Ребенок заболел за неделю до поступления в ДОКБ после контакта с больным членом семьи острой респираторной инфекцией (ОРИ), когда впервые у ребенка появилось повышение Т0тела до 38,5 оС, сухой кашель, заложенность носа. Участковым педиатром было назначено амбулаторное этиотропное и симптоматическое лечение лекарственными препаратами внутрь в возрастных дозах (ибуклин, виферон, сумамед, флуифорт) без видимого эффекта.
До поступления в ДОКБ в условиях детской поликлиники по месту жительства было проведено рентгенологическое исследование органов грудной клетки 26.02.2017 г. Заключение: признаки бронхита. Была проведена консультация ЛОР-врача 26.02.2017 г. Заключение: острый левосторонний неперфоративный средний отит.
Из анамнеза жизни известно, что ребенок от 1 беременности и родов. Беременность протекала на фоне токсикоза легкой степени, анемии на всем протяжении беременности, угрозы прерывания беременности на сроках 22 и 32 неделях гестации, хронической фетоплацентарной недостаточности (ХФПН). По результатам 1 и 2 УЗИ – скрининга патология не была обнаружена. Результаты 3 УЗИ – скрининга выявили врожденные пороки развития (макроцефалия, супратенториальная опухоль головного мозга слева, односторонняя окклюзионная гидроцефалия, ассимметрия лицевых структур, гидроцеле с обеих сторон). На 34 неделе беременности мать ребенка была консультирована в Центре медицины плода (г.Москва). Были даны рекомендации. Роды срочные, оперативные, путем экстренного кесарева сечения на сроке 38-39 недель. В родах у ребенка было тройное обвитие шеи пуповиной, у матери – зеленые воды. Вес при рождении – 3840 г, рост – 54 см. Оценка по шкале Апгар 7-8 баллов. Состояние при рождении тяжелое, физиологические рефлексы вялые, выраженная асимметрия лица за счет увеличения мягких тканей левой щеки, мышечный тонус снижен в нижних конечностях. На 6 день после родов ребенок был переведен в отделение патологии новорожденных и недоношенных детей ДОКБ, где он находился на лечении и обследовании в течение 2 недель с диагнозом: неонатальная гипербилирубинемия. Синдром дезаптациисердечно-сосудистой системы. Пре- и перинатальное поражение ЦНС смешанного генеза, подострый период. Синдром тонусных нарушений. Врожденная аномалия головного мозга: шизэнцефалия в левой гемисфере. Внутренняя левосторонняя окклюзионная гидроцефалия. Синдром Протея. Малые аномалии развития сердца (МАРС): открытое овальное окно (ООО) – 4,1 мм, аневризма межпредсердной перегородки. Дополнительные трабекулы левого желудочка. Внутриутробные инфекции (ВУИ): гнойный конъюнктивит стафилококковой этиологии, реконвалесцент.
С 2-месячного возраста у ребенка наблюдались ежедневные приступы в виде инфантильных спазмов, по поводу чего он впервые был госпитализирован в психоневрологическое отделение для детей раннего возраста ДОКБ г.Белгорода с жалобами на беспокойство, частые эпизоды поджимания ног к туловищу, сопровождающиеся пронзительным громким криком. В ходе проведения ЭЭГ с видео 26.11.2015 г. были зарегистрированы изменения биоэлектрической активности головного мозга эпилептиформного характера. Была назначена противосудорожная терапия (препарат вальпроевой кислоты из расчета 30 мг/кг/сут). По данным МРТ головного мозга от 03.06.2015 г. выявлена левосторонняя гемимегалэнцефалия, смешанная гидроцефалия, агенезия мозолистого тела. Шизэнцефалия в левой гемисфере.
Голову держит с 6 мес. жизни, не сидит, не ползает, не ходит, не говорит. При ухудшении состояния ребенок периодически находился на стационарном лечении в психоневрологическом отделении для детей раннего возраста ДОКБ, где проводилась метаболическая и противосудорожная терапия.
В возрасте 8 мес. был госпитализирован во 2 отделение НИИ нейрохирургии им. акад. Н.Н. Бурденко (г. Москва) для дообследования и оперативного лечения на структурах головного мозга. 21.03.2016 г. была проведена операция – анатомическая гемисферэктомия слева. В послеоперационном периоде у ребенка наблюдались водно-электролитные нарушения с тенденцией к гипонатриемии, на фоне которой были зафиксированы генерализованные судорожные приступы, которые были купированы в отделении ИТАР. На момент выписки из отделения водно-электролитные нарушения регрессировали. В неврологическом статусе – правосторонний гемипарез, задержка в психомоторном развитии без отрицательной динамики. Была назначена противосудорожная терапия, и после снятия послеоперационных швов ребенок был выписан по месту жительства в удовлетворительном состоянии с соответствующими рекомендациями под наблюдение участкового педиатра и детского невролога с основным клиническим диагнозом: врожденный порок развития мозга (гемимегалэнцефалия слева), симптоматическая фокальная левополушарная фармакорезистентная эпилепсия, задержка психоречевого и моторного развития.
Гистологический диагноз по данным биопсии: морфологическая картина соответствует кортикальной мальформации и не противоречит клиническому диагнозу.
Сопутствующий диагноз: нейрофиброма мягких тканей левой щечной области. Оценка состояния по шкале Карновского – 50%.
После выписки из НИИ нейрохирургии постоянно находился под наблюдением детского невролога и нейрохирурга по месту жительства. В результате оперативного лечения судорожные приступы у ребенка прекратились. В динамике 28.06.16 г. была проведена повторная МРТ головного мозга с контрастным усилением. Заключение: МРТ-признаки врожденной аномалии развития головного мозга (левосторонняя мегалэнцефалия). Состояние после оперативного лечения (удаление левого полушария). Агенезия мозолистого тела. Объемное образование левой щечной области.
10.11.2016 г. был консультирован врачом-генетиком в ФГБНУ «Медико-генетический научный центр» и онкологом совместно с генетиком в ФГБУ «Федеральный научно-клинический центр детской гематологии, онкологии и иммунологии имени Д.Рогачева». Заключение: учитывая результаты геномного секвенирования, вероятнее всего, у ребенка имеет место Proteus-like синдром. Врожденный средний меланоцитарный невус. Было рекомендовано плановое удаление образования щеки с обязательным гистологическим исследованием образования. Рекомендовано наблюдение врачей-специалистов (генетика, невролога, сосудистого хирурга, дерматолога, офтальмолога и стоматолога) по месту жительства.
Общее состояние ребенка при поступлении в отделение патологии детей раннего возраста ДОКБ было средней степени тяжести за счет респираторного и интоксикационного синдромов. Тотела – 37.5оС. Вес тела – 12.6 кг, рост – 89 см. Окружность головы 53 см, окружность груди – 54 см. Ребенок сложен непропорционально: голова значительно больше по отношению к другим частям тела. Лицо ассимметрично за счет выраженной гипертрофии его левой щеки. В области левой щеки отмечался невус размером 5.0×2.0 см с выраженной пигментаций, выступающий над уровнем кожи. На коже левой половины лица и на разгибательной поверхности левого предплечья определялись единичные пигментные пятна размерами от 1.0×1.5-2.0 см до 1.5×3.0 см. На остальных участках туловища и конечностей пигментированных пятен не было. При осмотре определялись в основном лицевые стигмы дизэмбриогенеза (СДЭ): выраженная долихоцефалия, вытянутое лицо, линия глазной щели имеет косой наклон вниз, наружный угол глаза несколько опущен, широкая носовая перегородка, высокое «готическое» твердое небо, неправильный рост зубов (рис. 1)
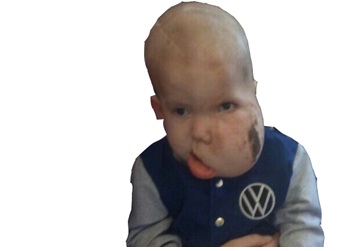
Рис. 1. Синдром Протея у ребенка Е. 1 г. 8 мес.
Fig. 1. Proteus syndrome in a 1 year and 8 months child E.
Кожные покровы бледные, эластичные. Отмечался умеренный периорбитальный и периоральный цианоз. Тургор тканей сохранен. Ребенок умеренного питания. Определялась полилимфоаденопатия. Пальпировались периферические задне-, переднешейные, подчелюстные, околоушные, подмышечные, паховые лимфоузлы размерами 0,5-0,7 см в диаметре, множественные, подвижные, безболезненные. Отмечалась гиперемия зева, язык был влажный, умеренно обложен белым налетом у корня. ЧД – 27 в минуту. Носовое дыхание затруднено. Отмечался малопродуктивный периодический кашель, чаще в утреннее время суток. Над легкими при перкуссии с обеих сторон определялся ясный легочный звук. При аускультации легких выслушивалось жесткое дыхание, единичные сухие рассеянные хрипы с обеих сторон. Область сердца при осмотре не изменена. Границы относительной тупости сердца соответствовали возрастной норме. ЧСС – 120 ударов в минуту. Тоны сердца были приглушены, ритмичные. Живот обычной формы, активно участвовал в акте дыхания. При пальпации он был мягкий, безболезненный. Печень выступала из-под края реберной дуги на 1,0 см. Селезенка не увеличена. Стул – 1 раз в сутки, оформлен, без патологических примесей. Диурез – в норме.
В неврологическом статусе: сознание ясное. Острота зрения снижена, глазные щели симметричны, зрачки равные, движения глазных яблок в полном объеме. Диплопии нет. Конвергенция ослаблена, нистагма нет, реакция зрачков на свет вялая. Острота слуха в норме. Лицо и мимика ассимметричны. Точки выхода тройничного нерва безболезненны. Отмечалось поперхивание и кривошея. Фонация не нарушена. Девиация языка вправо. Менингеальных симптомов нет, определялось снижение чувствительности в области левой щеки. Объем и сила активных и пассивных движений были снижены. Мышечная гипотония. Сухожильно-периостальные рефлексы оживлены, D>S. Отмечалась грубая задержка нервно-психического развития. Не сидит самостоятельно, не ходит. В психоэмоциональной сфере: вялый, моторно расторможен, эмоционально лабилен.
На основании жалоб при поступлении, анамнеза заболевания и жизни, клинического осмотра был выставлен предварительный диагноз: острый бронхит, ДН 0 ст. Врожденный порок развития мозга (гемимегалэнцефалия слева), состояние после оперативного лечения (удаление левого полушария). Симптоматическая фокальная левополушарная фармакорезистентная эпилепсия, задержка психоречевого и моторного развития. Proteus-like синдром. Врожденный средний меланоцитарныйневус.
Было назначено необходимое лабораторно-инструментальное обследование.
Общий анализ крови (ОАК) от 28.02.2017 г.: Эр – 3,76 × 1012/л, НВ – 96 г/л, Л. – 7,1 × 109/л, Тр. –203× 109/л, б – 0%, п – 1%, э – 0%, с – 11%, м – 10%, л – 77%, СОЭ – 50 мм/ч.
Общий анализ мочи (ОАМ) – в норме.
Копрограмма – в норме.
ЭКГ от 28.02.2017 г.: синусовая тахикардия, ЧСС – 167 ударов в 1 минуту, ЭОС в норме.
Консультация невролога от 27.02.2017 г.: резидуально-органическое поражение ЦНС, синдром Протея. Грубая задержка психоречевого развития. Внутричерепная компенсированная гипертензия, судороги в анамнезе. Задержка статико-моторного развития, правосторонний гемипарез. Назначен внутрь препарат элькар и глицин в возрастных дозах.
Консультация ЛОР-врача от 27.02.2017 г.: острый левосторонний неперфоративный средний отит. Ринофарингит.
С первого дня пребывания ребенка в отделении проводилась необходимая комплексная терапия: этиотропная противовирусная терапия (виферон); антибактериальная (внутримышечно (в/м) цеперон, амикацин); симптоматическая терапия (антипиретики – ибупрофен внутрь, в/м литическая смесь с 2% раствором хлоропирамина, с 50 % раствором анальгина, с 2% раствором дротаверина); муколитики (амбробене виде ингаляций и внутрь); противосудорожная терапия (карбамазепин внутрь); противогрибковая (флуконазол внутрь); местное лечение отита (0,5% раствор диоксидина в виде капель в нос и в уши); физиолечение (лазеротерапия на область грудной клетки, ингаляции с 0,5% раствором диоксидина, массаж грудной клетки).
На фоне данного лечения отмечалась положительная динамика в состоянии и самочувствии ребенка: снизилась температурная реакция до субфебрильных цифр, улучшился аппетит, уменьшился кашель. Ребенок стал более активным. В легких на фоне жесткого дыхания исчезли сухие хрипы. Отмечалась и положительная динамика и со стороны лабораторных данных.
ОАК от 03.03.2017 г.: Эр – 4,45 × 1012/л, НВ – 113 г/л, Л. – 7,1 × 109/л, Тр. –302× 109/л, б – 0%, п – 1%, э – 1%, с – 40%, м – 8%, л – 50%, СОЭ – 37 мм/ч.
ОАМ от 03.03.2017 г.: в норме.
Несмотря на проводимую комплексную терапию, с 09.03.2017 г. в течении заболевания у ребенка отмечалось резкое ухудшение общего состояния и самочувствия на фоне реинфекции ОРИ в результате контакта его с больным отцом. У пациента появились клинические симптомы бронхообструктивного синдрома (БОС), экспираторная одышка в покое, усилился влажный кашель на фоне повышения Тотела до 38,5 оС.
Учитывая ухудшение общего состояния ребенка на фоне реинфекции смешанной вирусной этиологии (вирус Эпштейн-Барр, цитомегаловирус, вирус простого герпеса 1 и 2 типов) по данным клинического и лабораторного обследования, были назначены с дезинтоксикационной целью инфузионная терапия из расчета 20 мл/кг массы ребенка в сутки (внутривенно (в/в) капельной инфузии 10% раствора глюкозы с 10% раствором глюконата кальция, 2% раствором пентоксифиллина, 2% раствором рибоксина); иммунотерапия (в/в капельно раствор иммуноглобулина человеческого из расчета 0,1 г/кг массы тела №3); глюкокортикостероиды (ингаляции пульмикорта и в/м дексаметазона). А также продолжена антибактериальная терапия (в/в капельно цефтриаксон) на фоне противосудорожных и противовирусных препаратов.
ОАК от 10.03.2017 г.: Эр – 4,78 × 1012/л, НВ – 118 г/л, Л. – 10,7 × 109/л, Тр. – 406 × 109/л, б – 0%, п – 2%, э – 1%, с – 40%, м – 7%, л – 50%, СОЭ – 35 мм/ч.
Биохимическое исследование крови от 10.03.2017 г.: общий белок – 62 г/л, сахар – 4,5 ммоль/л, АЛТ – 38 мЕ/л, кальций – 2,2 ммоль/л, фосфор – 1,45 ммоль/л, СРБ<6мг/л, щелочная фосфатаза – 239 Ед/л, АЛТ– 18 Ед/л, АСТ – 26 Ед/л.
ИФА крови от 10.03.2017г.: антитела к цитомегаловирусу IgM+; антитела к цитомегаловирусу IgM(КП) – 2,96; антитела к цитомегаловирусу IgG+; антитела к цитомегаловирусу IgG (конц.) – 5,23; антитела к вирусу простого герпеса 1 и 2 типов IgG+; антитела к вирусу простого герпеса 1 и 2 типов IgG(КП) – 9,06; антитела к капсидному антигену IgG вируса Эпштейн-Барр+; антитела к капсидному антигену IgМ вируса Эпштейн-Барр (КП) – 3,94; антитела к капсидному антигену IgG вируса Эпштейн-Барр (КП) – 19,38.
Бактериологическое исследование отделяемого из носа на флору от 10.03.2017 г.: выделен Staphylococcus haemolyticus (условно-патогенная микрофлора), умеренный рост. Данный микроорганизм является нормальной микрофлорой носовой полости.
Бактериологическое исследование отделяемого из зева флору и чувствительность к антибиотикам от 10.03.2017 г.: выделена условно-патогенная микрофлора, обильный рост (Klebsiellapneumonia – 1,0+05 KOE/г). Антибиотикограмма: ампициллин+, амоксициллин/клавулоновая кислота-, цефазолин-, цефепим+, цефтриаксон+.
ЭХОКГ от 14.03.2017 г.: ООО – 2 мм. Камеры сердца не расширены. Систолическая функция миокарда левого желудочка удовлетворительная.
На фоне проведенного лечения у ребенка через несколько дней нормализовалась температурная реакция тела, исчезли симптомы интоксикации, улучшился аппетит, кашель практически исчез, отмечалась положительная динамика в легких и со стороны лабораторных данных.
ОАК от 13.03.2017 г.: Эр – 4,79 × 1012/л, НВ – 115 г/л, Л. – 12,1 × 109/л, Тр. – 352× 109/л, б – 0%, п – 2%, э – 4%, с – 31%, м – 7%, л – 55%, СОЭ – 15 мм/ч.
ОАМ от 13.03.2017 г.: в норме.
Больной ребенок был выписан 15.03.2017 г. с улучшением и с соответствующими рекомендациями под наблюдение участкового педиатра, детского невролога, врача-генетика по месту жительства с диагнозом: острый обструктивный бронхит, ДН 0-1 ст. на фоне смешанной вирусной инфекции (вирус Эпштейн-Барр, цитомегаловирус, вирус простого герпеса 1 и 2 типов). Врожденный порок развития мозга (гемимегалэнцефалия слева), состояние после оперативного лечения (удаление левого полушария). Симптоматическая фокальная левополушарная фармакорезистентная эпилепсия, задержка психоречевого и моторного развития. Proteus-like синдром. Врожденный средний меланоцитарный невус.
Заключение. Таким образом, представляя описание данного клинического наблюдения, хотелось бы обратить внимание врачей-специалистов на одно из редко встречающихся заболеваний – Proteus синдром, который, вероятнее всего, сформировался у ребенка в результате доминантной соматической мутации в зародышевой клетке, и представить особенности клинического проявления СП в динамике на фоне течения смешанной острой вирусной инфекции у больного ребенка раннего возраста.
СП – это редкая патология детского возраста, которая характеризуется довольно непростой генетической идентификацией, имеет сходную клиническую картину с рядом наследственных заболеваний и формированием осложнений в виде новообразований. Поэтому своевременная диагностика имеет большое значение не только для прогноза течения данного заболевания, но и качества дальнейшей жизни пациента.
Автор статьи подтверждает отсутствие финансовой поддержки исследования, о которой необходимо сообщить.





















Список литературы