Современная геномика в изучении проблем адаптации человека к климату в высоких широтах Сибири
Aннотация
Актуальность: Коренные жители Сибири живут в экстремально суровых природных условиях на Земле, испытывая на себе длительное воздействие холода, сильных колебаний продолжительности светового дня и довольно ограниченного рациона питания. Очевидно, что успешное освоение человеком столь сложных для проживания территорий связано не только с культурной, но и с генетической адаптацией. Однако конкретные механизмы генетического приспособления к холодному климату, а также к диете с высоким содержанием животных жиров до сих пор остаются мало изученными. Цель исследования: Поиск маркеров полигенного отбора к климатическому стрессу в высоких северных широтах и пищевому рациону, основанному на богатой животными жирами пище. Материалы и методы: Исследование состояло из трёх этапов. На первом этапе в популяциях нганасан Таймыра (N=21) и якутов Республики Саха (N=21) выполнены отборочное полноэкзомное сканирование и полногеномный анализ однонуклеотидных замен (SNP). На втором этапе в «хвостах» эмпирических распределений выявлены гены-кандидаты, связанные с биологическими процессами и фенотипами, имеющими отношение к адаптации в циркумполярных группах. На третьем этапе лучшие кандидаты генотипированы в дополнительных популяциях Сибири, чтобы определить пространственное распределение частот аллелей и их ассоциации с климатическими переменными. Результаты: Были выявлены гены-кандидаты, из которых наибольший интерес представили гены PLA2G2A, PLIN1, ANGPTL8, вовлечённые в липидный метаболизм и связанные с бурой жировой тканью. В этих генах обнаружены несинонимичные замены, распространённость которых в северных популяциях указывает на вероятное воздействие естественного отбора. Заключение: Полученные результаты подтверждают гипотезу о том, что коренные популяции Сибири генетически адаптировались к жёсткой среде обитания путем отбора по нескольким генам, имеющим отношение к метаболизму жиров.
Ключевые слова: генетика популяций, естественный отбор, холодный климат, липидный обмен, гены PLA2G2A, PLIN1, ANGPTL8, однонуклеотидный полиморфизм
Введение. Одной из самых больших проблем, с которой столкнулись люди современного типа, мигрируя на север Евразии, был более холодный климат. Это давление отбора было особенно сильным в Сибири, где температуры минус 40°C не являются редкостью, а иногда доходят и до -70°. Постоянный многомесячный холод приводит к увеличенной потребности в калориях, при этом пищевые ресурсы довольно ограниченны и не постоянны. В отличие от северной Европы, Сибирь большей частью была свободной от ледников в течение последнего ледникового периода, и археологические находки показывают, что люди распространились по всей северной Сибири (72° с.ш.) не менее 45 тысяч лет назад [1-3].
Сегодня в этом большом регионе проживает ~ 31 коренная этническая группа, а культурные, генетические и лингвистические исследования показывают, что они имеют долгую и сложную историю [4, 5]. Поэтому у них имелся значительный период времени для локальных адаптаций, предшествующих, например, началу отбора на устойчивость к лактозе у европейцев [6, 7].
Было проведено несколько генетических исследований по определению генов-кандидатов, подвергшихся отбору в условиях холодного климата или особой диеты в циркумполярных популяциях. Хэнкок и соавт. [8] обнаружили доказательства отбора, влияющего на гены митохондриального разобщающего белка, UCP1 и UCP3, которые имеют важное значение для несократительного термогенеза в бурой жировой ткани и скелетных мышцах, соответственно [9, 10]. Сканирование выборки популяционных образцов из центральной и восточной Сибири обнаружило сильный сигнал в гене CPT1A, кодирующем карнитин-пальмитоилтрансферазу 1A [11, 12], которая необходима для транспортировки длинноцепочечных жирных кислот в митохондрии для окисления [13].
Имеются также данные по гренландским инуитам (родственным эскимосам Чукотки), свидетельствующие об отборе, действующем на кластер генов FADS (FADS1/2/3), который кодирует белки, участвующие в синтезе полиненасыщенных жирных кислот [14], а также на локус вокруг геновTBX15 и WARS2 [15], которые участвуют в несократительной терморегуляции [16].
В дополнение к этим отдельным генам-кандидатам, в 2017 г. обнаружены доказательства полигенной адаптации у нганасан и якутов, указывающей на отбор, действующий на многие биологические пути, включая цикл кальнексина, метаболизм жирных кислот, а также переваривание и усвоение белка [17]. Хотя до настоящего времени не было исследований народов Сибири, связывающих фенотипические различия с каким-либо из этих генов, эти результаты указывают на участие липидного обмена и генов, связанных с несократительным термогенезом и бурой жировой тканью, в качестве перспективных кандидатов.
Исследования физиологии и здоровья коренных сибирских групп (например, эвенков, бурят, селькупов, нганасан) выявили низкий уровень липидов в сыворотке крови [18, 19], высокую базальную скорость метаболизма и высокий уровень гормона щитовидной железы тироксина [20, 21].
Целью исследования. Поиск маркеров полигенного отбора к климатическому стрессу в высоких северных широтах и к пищевому рациону, основанному на богатой животными жирами пище.
Материалы и методы исследования. Настоящее исследование является результатом долголетнего международного сотрудничества между Лабораторией геномного анализа, отдел биотехнологии Аризонского университета, г. Тусон, штат Аризона, США (Майкл Хаммер, Т.М. Карафет) и лабораторией популяционной этногенетики ИЦиГ СО РАН по изучению генетического разнообразия в сибирских популяциях человека, а с 2013года- по изучению генетических основ адаптации к климатическому стрессу в коренных популяциях Сибири.
Биологический материал был собран в экспедиционных исследованиях в 2000 году в Республике Саха (Якутия) и на полуострове Таймыр под руководством к.б.н Осиповой Л.П. с участием к.б.н. Карафет Т.М. у практически здоровых лиц-добровольцев с использованием «Информированного согласия».
Для выявления генов, вовлеченных в процесс локальной адаптации у коренных сибиряков, был использован многоступенчатый подход.
На I этапе в популяциях Сибири выполнены отборочное полноэкзомное сканирование и полногеномный анализ однонуклеотидных замен (SNP).
На II этапе в «хвостах» эмпирических распределений выявлены гены-кандидаты, связанные с биологическими процессами и фенотипами, имеющими отношение к адаптации в циркумполярных группах.
На III этапе лучшие кандидаты генотипированы в дополнительных популяциях, чтобы определить пространственное распределение частот аллелей и их ассоциации с климатическими переменными. Протестировано 382 индивидов, в том числе 297 коренных сибиряков из 17 разных этнических групп.
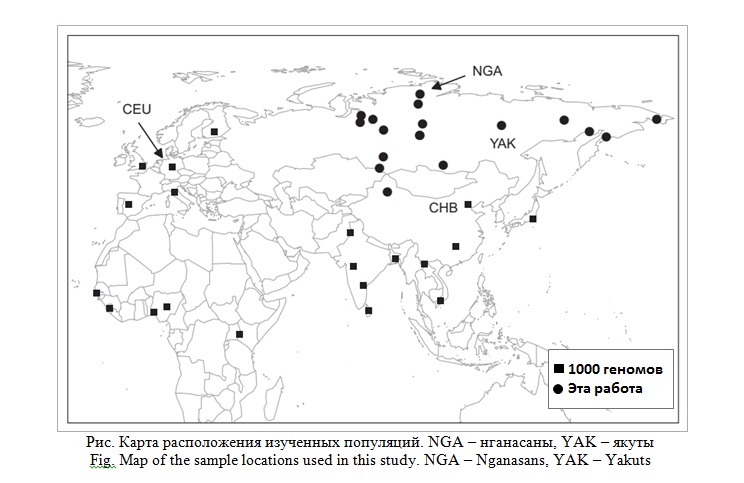
Основная выборка для полноэкзомного секвенирования была представлена образцами из двух популяций: нганасан (n = 21, покрытие = 6X) Таймыра, которые являются самой северной аборигенной группой в Евразии, и якутов (n = 21, покрытие = 4X) Республики Саха, региона Сибири с самыми низкими зимними температурами и одной из самых больших разниц летней и зимней температур в мире. Дополнительно были проанализированы данные анализа SNP высокой плотности Affymetrix, полученные на 307 представителях сибирских популяций и других. На рисунке показано положение на карте сибирских популяций, включенных в это исследование.
Результаты и их обсуждение. В результате работы были обнаружены три гена с разными вариантами, чьи функциональные характеристики, географическое распределение и геномные паттерны наиболее «экономично» объясняются локальной адаптацией к сибирской среде. Примечательно, что все три гена малы. PLA2G2A и ANGPTL8 составляют всего ~ 5 КБ, а PLIN1 составляет ~ 15 КБ.
PLA2G2A–фосфолипаза А2, группа IIA. В этом гене найдена редкая несинонимичная замена G>A (rs11573162) в гене PLA2G2A, который кодирует секреторную фосфолипазу A2-IIa (sPLA2IIa). Производный аллель A практически отсутствует за пределами Азии. В образцах проекта «1000 геномов» максимум частоты этого аллеля (7%) наблюдается у китайцев Хан, а средняя частота составляет 1%. Однако в наших сибирских выборках наибольшая частота обнаружена у лесных ненцев (48%) и у коряков (45%), причем в обеих этих популяциях более 80% людей имеют один или несколько аллелей A. Гомозигот АА за пределами Сибири обнаружено не было, при этом с максимальной частотой (23%) гомозиготы АА встречены у тундровых ненцев.
PLIN1–Перилипин 1. Найдена несинонимичная замена G>C (rs6496589) в гене PLIN1. Этот ген кодирует белок перилипин 1, главный регулятор липолиза и липогенеза в адипоцитах [22]. Для предкового аллеля G этого сайта ранее была показана связь с более низким уровнем липидов в сыворотке [23, 24]. Интересно, что предковый аллель имеет очень низкую частоту в Африке и Европе. В выборке проекта «1000 геномов» наибольшая частота аллеля G в популяциях Азии обнаружена у японцев (31%). В наших выборках якутов и нганасан частота аллеля G составила 45% и 55% соответственно, причем более 60% людей в обеих популяциях имеют по крайней мере один предковый аллель G.
Интересно, что самая высокая частота аллеля G (64%) найдена в панамских популяциях, говорящих на языках чибча и чокана, и у 87% людей в выборке из этой популяции имеется хотя бы один аллель G. Относительно высокие частоты были также обнаружены у майя и сапотеканцев из южной Мексики.
ANGPTL8–ангиопоэтиноподобный белок 8. Обнаружена несинонимичная замена C>T (rs2278426) в гене ANGPTL8, частота которой возрастает в Сибири. Этот ген также имеет названия C19orf80 и RIFL и кодирует ангиопоэтин-подобный белок 8, который также известен в литературе как липазин и бетатрофин. Для производного аллеля Т в этом сайте в нескольких исследованиях была показана связь с более низким сывороточным холестерином [25, 26]. В наших выборках частота аллеля Т достигает самых высоких значений у юкагиров (72%), эвенов (63%) и нганасан (60%). Примечательно, что 60% юкагиров являются гомозиготами ТТ, а 90% образцов из выборки коряков являются носителями по крайней мере одного Т-аллеля. Аллель Т также встречается с умеренной частотой в популяциях западной Африки.
Многие известные примеры естественного отбора в организме человека предполагают «селективные зачистки» (selective sweeps), но другие исследования показали, что такие «зачистки» были относительно редки в человеческой эволюции, и что преобладали другие режимы отбора [27, 28]. В случае адаптации к климату, Хэнкок и др. [8, 29, 30] предоставили доказательства того, что этот процесс в первую очередь обусловлен небольшими изменениями частоты аллелей множества генов, но неизвестно, сколько генов вовлечено и насколько малы могут быть изменения частоты аллелей.
У нганасан и якутов в 2017 году были обнаружены доказательства селекции, действующей на множественные группы генов, в том числе на метаболизм жирных кислот [17], но мы не выявили конкретные гены, управляющие этими сигналами. В настоящем исследовании тщательный анализ и аннотация вариантов с более низкими значениями PBS выявили три новых гена-кандидата, которые не обладали наивысшими сигналами и не были обнаружены предыдущим поиском полигенной селекции. Только PLA2G2A присутствует в одном из семи наборов значимых генов, полученных в предшествующей работе, и это не был ген, вносящий основной вклад [17]. Данное исследование было ограничено прежде всего кодирующими участками, так что, возможно, существуют более сильные сигналы в регионах, не охваченных экзомным секвенированием, хотя таковые не были обнаружены в массиве SNP из некодирующих областей. Что касается экзома, то мы не нашли никаких сильных сигналов отбора. Вместе с нашей предыдущей работой, эти данные согласуются с моделью локальной адаптации, при которой отбор действует одновременно, с различными коэффициентами, на варианты в нескольких функционально связанных генах. Однако в дальнейшем необходима работа по определению деталей этих процессов.
Полученные результаты показывают, как небольшие или средние изменения в частотах аллелей нескольких генов могут кооперативно привести к более быстрой дифференциации, чем это может быть достигнуто по одному локусу. В то время как эволюционная теория предсказывает фиксацию полезных аллелей, этот процесс может занимать очень много времени при реалистичных коэффициентах отбора и демографических сценариях [31]. Вместо этого, увеличение частот полезных аллелей в нескольких биологически родственных генах может происходить параллельно, что приведет к более быстрой дифференциации и адаптации. Вероятно также, что отбор часто происходит на основе ранее нейтральной "застывшей" вариации. В настоящем исследовании показано, что предковый аллель для rs6496589 (PLIN1) оказался под действием положительной селекции. Для rs22788426 (ANGPTL8) кандидатом на отбор является производный аллель, но он встречается в Африке с низкой частотой, что наводит на мысль о том, что эта замена возникла задолго до начала действия отбора. Только rs115773162 (PLA2G2A) согласуется с селекцией новой мутации, так как производный аллель географически ограничен Центральной/Восточной Азией и Сибирью.
Ассоциации с уровнями липидов в сыворотке. Все три гена-кандидата играют важную роль в метаболизме липидов, и однонуклеотидные замены в этих генах связаны с уровнями липидов в сыворотке и другими фенотипически релевантными состояниями. Эти ассоциации различаются в зависимости от этнической принадлежности, и как диета, так и метаболическое состояние (например, ожирение) играют роль в модулировании их эффектов.
Известно, что PLIN1 экспрессируется в жировой ткани и кодируемый им белок, перилипин 1, находится на поверхности липидных капель и функционирует в качестве основного регулятора как липолиза, так и липогенеза [32, 33]. Учитывая эту роль, неудивительно, что в ряде исследований были обнаружены связи между полиморфизмом PLIN1 и ожирением, увеличением веса и гипертонией [34], что входит в понятие «метаболический синдром». Для PLIN1 обнаружено, что генотипы rs6496589, CG и GG тесно связаны с риском центрального ожирения у взрослых китайцев, и анализы in vitro показали различия в накоплении липидных капель между генотипами GG и CC, причем гомозиготы GG показывают больше мелких капель [24]. Генотип GG также был связан с более низким уровнем циркулирующих свободных жирных кислот у корейцев после умеренной потери веса [23]. И стоит напомнить, что 37% нганасан являются гомозиготами GG.
Ген ANGPTL8 (~ 5kb) играет важную роль в метаболизме липидов, и новые исследования показывают, что он работает совместно с двумя близкородственными генами ANGPTL3 и ANGPTL4 для регуляции и адекватного распределения триглицеридов в различных тканях и различных физиологических условиях, включая голодание, физические упражнения и воздействие холода [35, 36]. Он также активируется гормоном щитовидной железы и, по-видимому, играет роль в метаболизме глюкозы [37-39]. Ранее было показано, что генотипы по ANGPTL8, rs2278426, были связаны с липопротеинами как низкой плотности(ЛПНП), так и высокой плотности (ЛПВП) у латиноамериканцев и афроамериканцев, причем у гомозигот ТТ уровень ЛПНП был ниже на 15% [25]. Го и соавт. [26] также обнаружили связь между генотипами в этом локусе и уровнями липидов в сыворотке у женщин Хан в Китае, причем у генотипов СТ или ТТ уровни холестерина, ЛПНП и АроВ были значительно ниже. Напомним, что частота аллеля Т увеличивается в Сибири, а юкагиры, эвены и нганасаны имеют частоты аллеля выше 0,6.
Фермент, кодируемый геном PLA2G2A, секреторная фосфолипаза A 2, группа IIA (sPLA2-IIA), непосредственно влияет на уровень циркулирующих липидов путем гидролиза сложноэфирной связи фосфолипидов с образованием свободных жирных кислот и лизофосфолипидов [40]. Этот белок хорошо известен своей ролью и прогностической ценностью при атеросклерозе и сердечно-сосудистых заболеваниях [41, 42], а более высокие уровни sPLA2-IIa в крови связаны с множественными негативными метаболическими и сердечно-сосудистыми сценариями. В том числе с более высоким уровнем холестерина, аполипопротеина B, ЛПНП и более мелких частиц ЛПНП [43]. Неудивительно, что варианты этого гена также связаны с метаболическим синдромом, ожирением и диабетом 2 типа [44, 45].
Таким образом, исследования сибирских популяций выявили три возможных типа физиологических адаптаций к среде их обитания: повышенный базальный метаболический уровень, очень низкий уровень липидов в сыворотке и высокий уровень гормонов щитовидной железы [19]. Проведённое исследование позволяет дать генетическое объяснение, особенно для низких уровней липидов в сыворотке. Интересно, что нганасаны имеют самые низкие сывороточные уровни липидов среди всех исследованных сибирских групп, включая низкий уровень общего холестерина, ЛПНП, ЛПОНП и триглицеридов [19]. В этом исследовании нганасаны также имеют наибольшее количество отобранных аллелей на человека по сравнению с другими популяциями. Другие сибирские народы также имеют низкий уровень липидов в сыворотке и разделяют эти полиморфизмы.
К сожалению, в настоящее время нет параллельных одномоментных фенотипических данных для каждого образца ДНК у конкретного индивида, необходимых для определения более точных отношений между генотипами и фенотипами, но результаты выполненной работы дают несколько конкретных гипотез для будущих работ.
Роль бурой жировой ткани. Несократительный термогенез в бурой жировой ткани (БЖТ) или индуцибельной жировой ткани бежевого цвета обеспечивает объединяющую биологическую функцию, которая помогает объяснить как наблюдаемые фенотипические различия у сибирских популяций, так и адаптивную роль для трёх обнаруженных генов-кандидатов. Накопленные данные указывают на то, что адаптация к холодному климату и диете сопряжена, и БЖТ обеспечивает связь между ними, так как несократительный термогенез требует постоянного запаса жирных кислот и глюкозы для производства тепла [9]. Следовательно, если БЖТ постоянно активна, как это может быть при сильном холоде, то необходим эффективный механизм для хранения и мобилизации топлива в адипоцитах. Хотя взаимодействие между активированной БЖТ и уровнем липидов в сыворотке до сих пор остается не совсем ясным, исследования показали более низкий уровень общего холестерина, ЛПНП и триглицеридов, но более высокий уровень ЛПВП у пациентов с активной БЖТ [46, 47]. Кроме того, как холодовое воздействие, так и действие гормона щитовидной железы активируют БЖТ. К сожалению, данные о БЖТ в сибирских популяциях в настоящее время отсутствуют, – но если у сибиряков есть дополнительная или более активная БЖТ, это может объяснить их повышенную базальную скорость метаболизма. На молекулярном уровне данные указывают на прямое участие всех трех генов-кандидатов в функционировании БЖТ.
Было обнаружено, что перилипин 1 необходим для липолиза, индуцированного норадреналином, в БЖТ мышей [48], а избыточная экспрессия вызывает появление у белых адипоцитов БЖТ-подобного фенотипа [49], что свидетельствует о «потемнении» белой жировой ткани и может также играть роль в адаптивном ответе на холод в сибирских популяциях. ANGPTL8 высоко экспрессируется в БЖТ и активируется как воздействием холода [50], так и гормоном щитовидной железы [37]. А для PLA2G2A Kuefneretal. [51] недавно предоставили доказательства того, что этот ген необходим для активации митохондриального разобщения в БЖТ.
К сожалению, тесная связь между адаптацией к холоду и диетой подтверждается недавним увеличением метаболических нарушений среди циркумполярных групп, которые отошли от традиционных диет и образа жизни [52, 53]. Аборигенные сибирские популяции особенно уязвимы к таким изменениям питания, так как аллели, которые когда-то были полезны в холодном климате, теперь являются генетическими факторами риска. Можно ожидать, что будущие исследования по выяснению молекулярных механизмов адаптации к диете и холоду обеспечат дополнительное понимание генетической архитектуры метаболизма и этиологии метаболических нарушений у человека.
Заключение. Полученные результаты подтверждают гипотезу о том, что коренные народности Сибири генетически адаптировались к жёсткой среде обитания путем отбора по нескольким генам, имеющим отношение к метаболизму жиров.
Благодарности
Работа была поддержана грантом РНФ № 19-15-00219.





















Список литературы