Эффекты психофармакотерапии и приверженность пациентов лечению: взаимообусловленность в рамках биопсихосоциальной парадигмы
Aннотация
Актуальность: Ожидаемые в клинике эффекты психофармакотерапии опосредуются изменениями дофаминовой и серотониновой нейротрансмиции, которые в свою очередь могут определять у пациентов нарушения мотивационных процессов. Цель исследования: Изучить взаимосвязи получаемой психотропной терапии с биологическими, психологическими и социальными факторами приверженности пациентов психиатрическому лечению. Материалы и методы: 83 пациента, госпитализированные в связи с экзацербацией для подбора терапии. Социо-демографические, анамнестические данные собраны из медицинской документации. Использованы оригинальный Опросник оценки мотивации к лечению и Шкала медикаментозного комплайенса. Проведён дисперсионный анализ при p≤0.05. Подсчёты размеров эффектов (ES) проводили с использованием Cohen’s d и Cramer’s V. Результаты: Принимавшие атипичный антипсихотик пациенты отличались меньшей длительностью заболевания и редкими госпитализациями (ES=0.68 и 0.47). Терапию двумя нейролептиками получали только бездетные и одинокие пациенты (ES=0.32). Анамнестические нарушения комплайенса различались в подгруппах пациентов, получавших типичные и атипичные нейролептики (ES=0.74). Была произведена объективация структуры мотивации пациентов к лечению: больные, принимавшие амбулаторно типичные антипсихотики, меньше опирались на собственные знания и навыки способов преодоления заболевания при принятии решения о лечении (ES=0.64) и характеризовались низкой интенсивностью терапевтической мотивации (ES=0.6). Вне зависимости от класса, прием антидепрессантов был связан с улучшением инсайта пациентов на заболевание, однако неспецифическая интенсификация мотивации к лечению происходила лишь на фоне получения антидепрессивной терапии в сочетании со стабилизаторами настроения (ES=0,64). Заключение: Длительная приверженность пациентов психофармакотерапии является не только социально-психологическим конструктом, но и биологическим процессом, подверженным влиянию назначаемых в клинической практике нейротропных препаратов.
Ключевые слова: комплайенс, мотивация к лечению, приверженность к лечению, психофармакотерапия, антипсихотики, антидепрессанты, социальные факторы
Введение. Общеизвестна распространенность медикаментозного нонкомплайенса среди пациентов с психическими расстройствами [1]. Систематизация причин нарушения больным приверженности медикаментозной терапии позволила выявить наиболее значимые из них. Факторами низкой приверженности лечению являются низкая критика к болезни, стигма, прогрессирующие нарушения психических функций в виде ухудшения мотивационно-волевой регуляции, нарастание социальной дезадаптации на фоне интенсивной психопродуктивной или негативной симптоматики [2]. Кроме того, полифармация и связанный с ней сложный режим медикаментозной терапии также способствует снижению комплайенса [3, 4]. В обзоре 402 исследований с 53463 участниками показано, что различия в эффективности 32 антипсихотиков незначительны и больше касаются развития побочных эффектов [5]. Вместе с тем, стратегии выбора врачами психофармакотерапии могут быть основаны не только на анализе симптоматики, течения заболевания и переносимости терапии, но и на парамедицинских факторах: трудовом и семейном статусе пациентов, их поле и возрасте, низком инсайте на заболевание, а также условиях оказания помощи и недобровольной госпитализации [6].
Ожидаемые в клинической практике эффекты психофармакотерапии зачастую опосредуются изменениями дофаминовой и серотониновой нейротрансмиции. За счет первых достигаются улучшения регуляции поведения человека, мотивационных процессов и обучения [7, 8]. Вторые связаны с реализацией исполнительских функций и, также, мотивации к ним [9]. При этом первичное обращение к врачу, целенаправленное поведение, связанное с приемом рекомендованного лечения, динамическое отслеживание его эффектов является сложным комплексом поведенческих реакций пациентов, однозначная оценка которых представляет существенные трудности. С одной стороны, регуляция поведения оказывается в перекрёстной взаимосвязи с назначаемой терапией, с другой стороны – длительный приём нейротропных препаратов, модулирующих мотивационные процессы, может определять изменения приверженности пациентов приёму антипсихотиков и антидепрессантов. Таким образом, натуралистические условия оценки приверженных и неприверженных терапии пациентов, а также сравнение их существенных характеристик представляют интерес для рассмотрения в качестве факторов, связанных с формированием комплайентного поведения пациентов на амбулаторном этапе лечения.
Гипотеза исследования состояла в предположении, что приверженность психиатрических пациентов лечению является биопсихосоциальным феноменом, компоненты которого доступны для объективной оценки.
Цель исследования.Изучение взаимосвязи получаемой пациентами психотропной терапии с предполагаемыми биологическими, психологическими и социальными факторами их приверженности лечению на момент обращения за стационарной психиатрической помощью. Задачи исследования включали: 1) исследование роли клинических факторов в приеме пациентами психофармакотерапии, 2) определение места социальных факторов в психофармакотерапии, которой пациенты длительно остаются привержены, 2) исследование связи психофармакотерапии с инструментальной оценкой мотивации пациентов к лечению, инсайтом на заболевание и поведением в ходе терапии.
Материалы и методы исследования. Тип исследования – обсервационное. Критериями включения в исследование были: 1) добровольное информированное согласие на участие в исследовании, 2) добровольная госпитализация в психиатрический стационар в связи с обострением психического состояния с целью подбора терапии, 3) нахождение на этапе становления ремиссии, 4) возраст от 18 до 70 лет. Критерии невключения: 1) невозможность пациента понять смысл и выполнять процедуры исследования в силу актуального психического статуса. В исследование были включены 83 пациента, госпитализированные в отделение интегративной фармако-психотерапии больных с психическими расстройствами НМИЦ ПН имени В.М. Бехтерева с период января 2017-го по декабрь 2018-го года.
Регистрация социо-демографических и анамнестических данных пациентов, в том числе проводившейся ранее психофармакотерапии проводилась по данным медицинской документации. Оценка мотивации к лечению была проведена с помощью оригинального самоопросника для пациентов (ОцМЛ), обладающего высокой надежностью (α Кронбаха 0.842) и продемонстрировавшего свою валидность [9-11]. Врачами заполнялась Шкала медикаментозного комплайенса [2], позволяющая, в частности, оценить особенности поведения пациентов в процессе психофармакотерапии, их инсайт на заболевание (п. 2.1), когнитивный статус (п. 2.8), а также выраженность продуктивной и негативной симптоматики, (пп. 2.2 и 2.3), уровень социальной дезадаптации (п. 2.7) по шкалам BPRS, SANS, GAF.
Использованы дескриптивные статистики, сравнение групп для параметрических данных – с использованием однофакторного дисперсионного анализа (ANOVA) и t-критерия Стьюдента; для непараметрических – H-критерия Краскела-Уоллеса и U-критерия Манна-Уитни; для номинальных шкал – х2 Пирсона. Параметры распределения данных оценивались по z-критерию Колмогорова-Смирнова. Результаты исследования представлены с указанием средних и их стандартных отклонений (M±S.D.) В случае выявления межгрупповых различий с уровнем достоверности p≤0,05 высчитывали также размеры наблюдаемых эффектов (Cohen’s d и Cramer’s V). Оценка размера эффекта проводилась по общепринятым критериям: слабый 0,10-0,29, умеренный 0,3-0,49, сильный ≥0,50. При сопоставлении номинальных признаков с более чем двумя градациями интерпретация размера эффекта проводилась с поправкой на число степеней свободы и указанием пороговых значений для слабого/умеренного/сильного эффекта.
Протокол исследования прошел экспертизу соответствия требованиям Хельсинкской декларации и одобрен к проведению Независимым этическим комитетом при НМИЦ ПН им. В.М. Бехтерева.
Результаты и их обсуждение.
Социо-демографическая и клиническая характеристика выборки.
Среди обследованных пациентов число мужчин составило 32 человека (39%), женщин – 51 (61%). Средний возраст участников исследования 36 ± 13 лет, длительность заболевания – 12 ± 11 лет, количество госпитализаций – 5 ± 4. Доля пациентов, имеющих среднее образование – 21%, профессиональное – 27%, высшее – 52%. Работающих – 44%, состоящих в браке – 39%, имеющих детей – 35%. В соответствии с МКБ-10 исследованная выборка включала пациентов с заболеваниями группы шизофрении (F2) – 67%, с аффективными расстройствами (F3) – 15%, невротическими и личностными (F4+F6) – 9%, а также органическими заболеваниями (F0) – 9%. Психопродуктивная симптоматика свыше 60 баллов по шкале BPRS была выявлена у 25% пациентов, от 40 до 60 баллов – у 58%, менее 40 – у 17%. Доля выборки в 31% имела выраженную негативную симптоматику с оценкой по шкале SANS более 60 баллов, умеренную (30-60 баллов) – у 33% пациентов, слабую (менее 30 баллов) – 36%. Выраженность социальной дезадаптации по шкале GAF более 60 баллов была у 30% выборки (“сохранные” пациенты), от 40-60 баллов – у 55%, еще 15% пациентов были наиболее дезадаптированы (менее 40 баллов).
Получали нейролептическую терапию 64 пациента (77%), причем 11 из них (13%) – сочетанную из препаратов 1-го и 2-го поколений. Арипипразол принимали 8 человек, кветиапин – 13, клозапин – 4, оланзапин – 6, рисперидон или палиперидон – 8, сульпирид – 5, галоперидол – 7, зуклопентиксол – 2, трифлуоперазин – 4, флупентиксол – 3, “малые нейролептики” (хлорпротиксен, тиоридазин) – 4. Антидепрессанты принимали 24 пациента (29%), в том числе 19 человек (23%) в комбинации с нейролептиками, 7 (8%) – с тимостабилизаторами. Антидепрессивная терапия включала трициклические антидепрессанты (8 пациентов, 10%), группу СИОЗС (11 человек, 13%), препараты с двойным механизмом действия (5 человек, 6%). При этом 17-ти пациентам, включенным в исследование, ранее не назначалась психотропная терапия, либо они прекратили ее прием по собственному решению до госпитализации.
Взаимосвязь клинических факторов и фармакотерапии.
Пациенты, получавшие один или два антипсихотика, в отличие от не принимавших нейролептики перед госпитализацией, имели различия в течении заболевания (рис. 1). Первые – дольше болели (Cohen’s d=0,68 и 0,76 соответственно, при p≤0,05) и ранее большее количество раз госпитализировались (Cohen’s d=0,87 и 1.43 соответственно, p≤0,05). При этом получение больными на амбулаторном этапе типичных и атипичных нейролептиков также было связано с достоверными различиями в длительности (Cohen’s d=0,68, p≤0,05) и количестве госпитализаций у них (Cohen’s d=0,47, p≤0,05). Эти сведения подтверждают известные данные о взаимосвязи антипсихотической полипрагмазии и характеристик течения заболевания пациентов [12, 13]

По оценкам лечащих врачей в соответствии со шкалой медикаментозного комплайенса выраженные когнитивные нарушения имела половина исследованной выборки. Снижение когнитивной продуктивности чаще встречалось среди пациентов, получавших арипипразол и кветиапин (50% и 20% соответственно), реже у принимавших оланзапин и сульпирид (по 30% среди когнитивно сохранных больных, х2=11,3; p=0,045). За исключением этих находок, не было выявлено зависимости между получаемой пациентами на амбулаторном этапе лечения психотропной терапией, количеством одновременно принимавшихся препаратов и выраженностью психопатологии (продуктивной и негативной симптоматики, а также социальной дезадаптации). С учётом того, что выбор антипсихотика врачом зачастую бывает мотивирован интенсивностью симптоматики пациента [14], полученные данные позволяют сделать предварительный вывод о сопоставимой эффективности длительного приёма разных препаратов, применяемых в России для коррекции как продуктивных, так и негативных симптомов.
Взаимосвязь социальных факторов и психофармакотерапии.
С равной частотой среди больных, амбулаторно не получавших антипсихотическую терапию и получавших один класс антипсихотиков, встречались как имеющие детей, так и бездетные пациенты: соответственно 47% и 53%, 39% и 61% (рис. 2). При этом сочетанную антипсихотическую терапию двумя нейролептиками получали только последние (Cramer’s V=0,32, размер эффекта при df=3 большой). Аналогичные пропорциональные соотношения были выявлены в отношении больных, состоявших и не состоявших в браке: 47% и 53%, 45% и 55%, 100% (Cramer’s V=0,39, размер эффекта при df=3 большой). Кроме того, антипсихотики 1-го поколения чаще получали пациенты, не вступившие в брак; напротив, вероятность приёма препаратов 2-го поколения была практически равной (73% и 27%, 46% и 54%, Cramer’s V=0,29). Выявленные ранее взаимосвязи социо-демографических параметров пациентов и паттернов проводимой им психофармакотерапии включали прежде лишь эффекты возраста и этнических различий [15, 16].

Среди пациентов, встречавших адекватное отношение к медикации со стороны своего окружения, чаще был распространен прием антидепрессантов, чем его отсутствие (75% и 25%). При отрицательном отношении друзей или семьи пациента встречались лишь не принимавшие антидепрессанты больные (х2=9,8; Cramer’s V=0,67, p=0,05). Таким образом, полученные сведения о приверженности пациентов медикаментозной терапии во взаимосвязи с фактором семьи дополняют известные данные об эффекте микросоциального окружения на приверженность антипсихотической терапии [17].
Взаимосвязь мотивационно-поведенческих характеристик и терапии.
Анамнестические нарушения комплайенса по-разному были представлены в подгруппах пациентов, получавших типичные и атипичные нейролептики (х2=10,9; Cramer’s V=0,74, размер эффекта при df=3 большой, p=0,03) (рис. 3). У первых встречались прием не рекомендованных врачом лекарств и самовольное снижение дозировок (67% и 33% соответственно). У вторых практически в равной степени были представлены как самостоятельные прекращения терапии, так и отсутствие нарушений комплайенса, соответственно 44% и 35%. Взаимосвязи паттернов поведения пациентов в ходе лечебного процесса и принимаемой ими фармакотерапии ранее описывалась в литературе [18], однако они касались лишь применения тимостабилизаторов и депо-препаратов, а также эффекта досрочных выписок из стационара.

По данным Шкалы медикаментозного комплайенса, среди больных, демонстрировавших критику к симптомам заболевания, преобладали принимавшие антидепрессанты (62,5%), реже встречались пациенты, не получающие психотропной терапии или получающие только тимостабилизаторы (25% и 12,5% соответственно). Аналогично, в пропорции 10%-40%-50%, фрагментарная критика определялась чаще среди пациентов без антидепрессивной терапии. Полное отсутствие инсайта встречалось только у пациентов, не получавших психотропной терапии (х2=9,8; Cramer’s V=0,47, размер эффекта при df=4 большой, p=0,045) (рис. 4). Взаимообусловленность инсайта на заболевание и психофармакотерапии многократно описаны в литературе, однако ранее преимущественное внимание уделялось связи с приёмом антипсихотиков [17, 19].

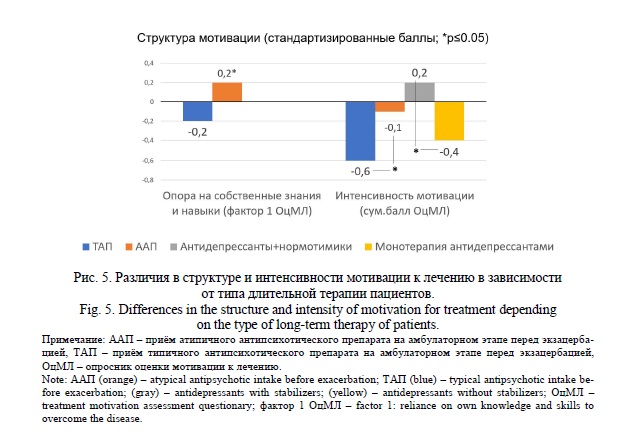
Наиболее существенным из полученных результатов была объективация структуры мотивации пациентов к лечению, сформированной на фоне конкретного варианта получаемой ими психофармакотерапии (рис. 5). Больные, принимавшие амбулаторно антипсихотики 1-го поколения по сравнению с получавшими препараты 2-го поколения имели искажения мотивационных установок: меньше опирались на собственные знания и навыки способов преодоления заболевания при принятии решения о лечении (фактор 1 ОцМЛ; Cohen’s d=0,64, p≤0,05). Это приводило к достоверному снижению у них суммарной интенсивности мотивации (суммарный балл ОцМЛ; Cohen’s d=0,6, p≤0,05). При этом существенно более высокие показатели мотивации к лечению демонстрировали также пациенты, получавшие сочетанную антидепрессивную и нормотимическую терапию по сравнению с принимавшими антидепрессанты без тимостабилизаторов (суммарный балл ОцМЛ; Cohen’s d=0,64, p≤0,05).
Интерпретация полученных данных.
Проведенное исследование подтвердило исследовательскую гипотезу. Специфика нейрохимического профиля нейротропных препаратов, наряду с социально-психологическими и клиническими характеристиками пациентов являются параметрами, взаимообусловливающими поведение, направленное на следование лечебной программе. В проведённом исследовании не учитывались потенциальные эффекты, связанные с различием доз принимавшихся препаратов. Однако все анализированные пациенты получали препараты в рамках диапазонов рекомендованных терапевтических доз, а более надёжная оценка фармакокинетики требовала бы проведения дорогостоящих фармакогенетических анализов и лекарственного мониторинга. В целом, ограниченность выборки и обсервационно-анамнестический характер исследования определяют его пилотный характер. Тем не менее, полученные результаты позволяют предварительно судить, что характер психопатологической симптоматики в случае развития обострения на фоне приёма поддерживающего лечения не определяется принимавшейся больными психофармакотерапией.
Виды нарушений медикаментозного комплайенса, выявленные у больных, длительно получающих антипсихотики 1-го поколения, связаны с их меньшей склонностью опираться на собственные знания и навыки способов преодоления заболевания. Эти мотивационные предиспозиции сочетаются у них не столько с приёмом не рекомендованных препаратов и снижением доз вопреки полученным от врача инструкциям, но и с общим снижением интенсивности терапевтической мотивации. Здесь важно учитывать, что длительное следование рекомендованному приёму препаратов 1-го поколения, а также комбинаций типичных и атипичных нейролептиков, вероятно, в значительной степени поддерживается клиническими и социальными факторами пациентов: их семейным положением, более тяжёлым течением заболевания и, возможно, низкой эффективностью относительно негативной симптоматики [5].
Особый тип взаимосвязи выявлен между мотивацией к лечению у больных психическими расстройствами и получаемой ими антидепрессивной терапией. В определенной степени это может быть связано с прокогнитивным эффектом и снижением ангедонии, опосредующими активацию части нейрохимических составляющих феномена мотивации [20, 21, 22]. Вне зависимости от класса, прием антидепрессантов связан с улучшением инсайта пациентов на заболевание, однако неспецифическая интенсификация мотивации к лечению происходит лишь фоне получения антидепрессивной терапии в сочетании со стабилизаторами настроения. В свою очередь, длительная приверженность тимоаналептической терапии также опосредуется социальными факторами, а именно адекватным отношением окружения пациентов к психофармакотерапии.
Заключение.Приверженность пациентов психофармакотерапии является биопсихосоциальным феноменом, поскольку в его реализации участвуют не только факторы течения заболевания, социальной поддержки больных, их психологических установок и поведенческих стереотипов, но и биохимическая природа назначаемой терапии. Таким образом, достижение удовлетворительного медикаментозного комплайенса требует от врача не только всестороннего анализа психосоциальных параметров пациента, но и понимания нейрохимических эффектов назначаемых классов психотропных препаратов в отношении мотивационных процессов пациента.
Информация о финансировании
Финансирование данной работы не проводилось.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.





















Список литературы