Фармакологический потенциал ар-турмерона и изучение экстрагирующего потенциала фторированных производных алканов для его изолирования из корневищ Curcuma longa L.
Aннотация
Актуальность:Ар-турмерон один из основных компонентов эфирного масла корневищ Curcuma longa L. Он обусловливает специфичность состава эфирного масла корневищ C. longa L. Перспективность настоящего компонента обусловлена целым набором важных фармакологических свойств. Поскольку ар-турмерон является компонентом эфирного масла, то для его экстракции используется целый ряд вариантов, характерных для эфирных масел: гидродистилляция, экстракция органическими растворителями, сжиженными газами, в том числе СО2. Меньше всего изучено влияние фреонов на экстракцию ар-турмерона. Использование этого типа растворителей имеет ряд существенных преимуществ перед вышеуказанными, в числе которых: нетоксичность, негорючесть и невзрывоопасность, низкая температура кипения, селективность, низкая вязкость. Указанный спектр качеств фреонов делает их очень перспективными для извлечения ар-турмерона. Цель исследования:Обоснование целесообразности использования фторхлорпроизводных алканов в качестве перспективных экстрагентов для выделения важнейшего терапевтического агента корневищ C. longa L. ар-турмерона. Материалы и методы:В качестве объекта исследования использованы корневища C. longa L., предварительно высушенные и измельчённые. В качестве экстрагентов выбраны метоксинонафторбутан (Novec 7100) и фторкетон (додекакафлуоро-2-метилпентан-3-он, Novec 1230), экстрагентом сравнения служил н-гексан. Для идентификации и количественной оценки ар-турмерона в анализируемых образцах использован метод газовой хроматографии – масс-спектрометрии. Хроматографирование проводили на газовом хроматографе – масс-спектрометре – GCMS-QP2010 Ultra, «Shimadzu», Япония. Ионизация осуществлялась с помощью электронного удара, детекция по полному ионному току (SCAN). Разделение проводилась на капиллярной кварцевой колонке в режиме программируемых температур. Результаты:В ходе анализа установлено, что во всех образцах, подвергшихся экстракции выбранными растворителями доминирующим компонентом, является ар-турмерон, содержание которого в зависимости от растворителя в полученных извлечениях колебалось в пределах от 35 до 40%. Наилучшей экстрагирующей способностью по отношению к ар-турмерону обладает метоксинонафторбутан. Заключение:Установлено, что оптимальным экстрагентом для ар-турмерона является метоксинонафторбутан; фторкетон показал меньшую экстрагирующую активность. Экстрагирующая способность метоксинонафторбутана по отношению к ар-турмерону оказалась выше таковой экстрагента сравнения – н-гексана. При его использовании в извлечение переходило максимальное количество анализируемого соединения, причём содержание ар-турмерона в полученном суммарном извлечении превышало 40%. Кроме того, метоксинонафторбутан по сравнению с н-гексаном нетоксичен, негорюч, имеет меньшую температуру кипения
Ключевые слова: ар-турмерон, экстракция фреонами, метоксинонафторбутан, газовая хроматография-масс-спектрометрия
Введение. (+)-(S)-ар-турмерон, компонент, найденный в некоторых представителях семейства Zingiberaceae и в первую очередь в корнях куркумы длинной – Curcumalonga L. По химической структуре настоящее соединение представляет собой ароматический сесквитерпеноид, имеющий структуру – 2-метилгептен-2-ен-4-она, замещённого 4-метилфенильной группой в положении 6 (Рис. 1).
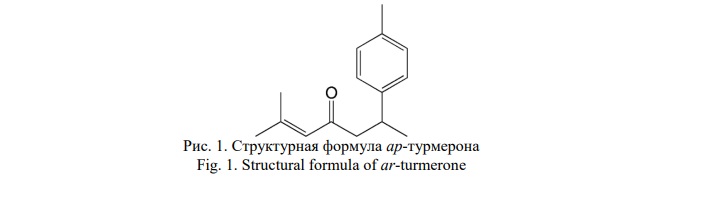
Ар-турмерон обусловливает специфичность состава эфирного масла корней C. longa L., наряду с такими маркерными составляющими, как: α-куркумен, α-зингиберен и курлон (Рис. 2).
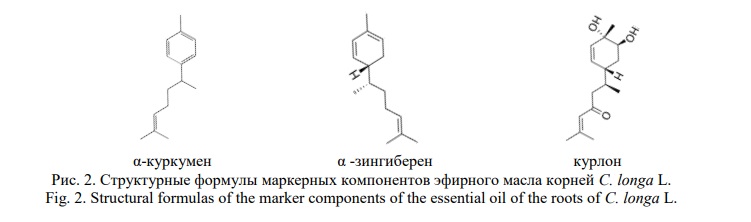
Однако, важным преимуществом настоящего соединения в отличие от других близких по структуре производных, является довольно специфический спектр фармакологической активности. В настоящее время накоплено обширное количество сведений о векторах фармакологической активности настоящего соединения.
В опытах invitro у ар-турмерона выявлена противомалярийная и цитотоксическая активность. Установлено, что данное соединение проявляло антиплазмодиальный эффект в отношении Plasmodiumfalciparum 3D7 (чувствительного к хлорохину) с помощью анализа лактатдегидрогеназы Plasmodium (pLDH) и цитотоксический эффект против клеток почек Vero млекопитающих. Эффекты ар-турмерона оказались сопоставимыми с эталонным противомалярийным препаратом хлорохина дифосфатом [1].
Ар-турмерон оказался эффективным нейропротектором, участвующим в угнетении дофаминергической нейродегенерации нейронов чёрной субстанции при болезни Паркинсона. Указанный эффект связан со способностью настоящего соединения оказывать противовоспалительное действие в клетках микроглии. Тем самым тормозится дофаминергическая нейродегенерация, вызванная активацией микроглии в культурах срезов среднего мозга. Кроме того, обнаружена способность ар-турмерона ингибировать дофаминергическую нейродегенерацию, вызванную нейротоксином – 1-метил-4-фенилпиридинием [2].
Продемонстрирована антиангиогенная активность ар-турмерона в опытах in vitro и in vivo, в том числе в клетках эндотелия микрососудов человека. Aр-турмерон ингибировал пролиферацию, трубкообразование и подвижность клеток HMEC-1 в нецитотоксических концентрациях. Поскольку ангиогенез необходим для роста опухоли, это позволяет свидетельствовать об этом соединении как о перспективном противоопухолевом агенте [3].
Обнаружена выраженная противоэпилептическая активность ар-турмерона на модели химически индуцированных судорог у лабораторных животных, вызванных пентилентетразолом [4].
Определено влияние ар-турмерона на воспалительный процесс. У данного компонента избирательно проявлялось мощное противовоспалительное действие за счёт подавления продукции воспалительных цитокинов IFN-γ и IL-2. При этом ар-турмерон не влиял на экспрессию интерлейкина 4 (IL-4). Настоящее соединение также снижало экспрессию IL-2 в CD4+, но не изменяло скорость их клеточного деления при стимуляции [5].
Ар-турмерон оказался эффективным в подавлении воспалительной реакции при псориазе, смоделированном у лабораторных животных. Ар-турмерон дозозависимо подавлял пролиферацию кератоцитов, облегчал апоптоз и снижал TNF-α-опосредованную продукцию интерлейкинов 6 и 8 [6].
Имеется ряд исследований, доказывающих активность ар-турмерона и куркуминоидов при диабете 2 типа. Данные компоненты подавляли повышение уровня глюкозы в крови у подопытных животных и стимулировали дифференцировку адипозоцитов человека [7].
Кроме того, выявлена превентивная активность ар-турмерона и бисакурона, выделенных из экстракта куркумы, в отношении повреждения гепатоцитов, вызванного этанолом [8].
Установлена высокая антиоксидантная и антибактериальная активность эфирного масла и спиртовых экстрактов из корневищ куркумы, причём наиболее выраженные антиоксиднтный и антибактериальный эффекты наблюдались в тех образцах, где содержание ар-турмерона было наибольшим [9].
Ар-турмерон вызывает уменьшение фотостарения кожи путём ингибирования экспрессии интерлейкина-1β и фактора некроза опухоли, что обусловливает его перспективность в качестве фотопротекторного соединения [10].
Установлены инсектицидные и репеллентные свойства ар-турмерона в отношении сельскохозяйственных насекомых-вредителей: рисовых долгоносиков – Sitophyluszeamais, осенней совки – Spodopterafruiperda и сдерживающую и ларвицидную активность для комаров [11, 12].
Поскольку ар-турмерон является компонентом летучей фракции корней куркумы, то есть входит в состав её эфирного масла, то для его извлечения из сырья используются самые разные варианты, характерные для эфирных масел: гидродистилляция, экстракция органическими растворителями, сжиженными газами, в том числе СО2 [13, 14]. Однако, по нашему мнению, для извлечения ар-турмерона наиболее целесообразно использовать экстракцию фреонами. Это связано с тем, что при гидродистилляции может происходить изомеризация и термическая деградация ар-турмерона, а извлечение органическими растворителями требует использования токсичных агентов и довольно длительного времени экстракции [15].
Цель исследования. Обоснование целесообразности использования фторхлорпроизводных алканов в качестве перспективных экстрагентов для выделения важнейшего терапевтического агента корневищ C. longa L. ар-турмерона.
Материалы и методы исследования. В качестве объекта исследования использованы корни C. longa L., предварительно высушенные и измельчённые. В качестве экстрагентов выбраны метоксинонафторбутан (Novec 7100) и фторкетон (додекакафлуоро-2-метилпентан-3-он, Novec 1230), экстрагентом сравнения служил н-гексан. Для извлечения эфирного масла из корневищ C. longa L. 0,1 г (точная навеска) сырья заливали 10 мл соответствующего экстрагента, плотно укупоривали и экстрагировали методом мацерации при комнатной температуре в течение суток. Щадящие условия экстракции необходимы для предотвращения процессов химической деградации и изомеризации искомого компонента. По истечении указанного времени полученные извлечения фильтровали через бумажный фильтр «синяя лента» в мерные колбы вместимостью 10 мл, недостающие объёмы восполняли соответствующими экстрагентами, доводя содержимое колб до метки. Полученные извлечения непосредственно использовали для хроматографирования.
Хроматографирование проводили на газовом хроматографе – масс-спектрометре – GCMS-QP2010 Ultra, «Shimadzu», Япония. Ионизация осуществляется в режиме электронного удара, детекция по полному ионному току (SCAN).
Поскольку эфиромасличный состав корневищ C. longa L. представлен моно-, сесквитерпенами и ароматическими производными, обладающими различной упругостью паров, то хроматографирование проводили в режиме программируемых температур.
Условия хроматографирования:
Колонка капиллярная кварцевая размером 30 mL × 0,25 mmID × 0,25 μm (ZebronZB-5MS);
Скорость газа-носителя (гелий) - 3,0 мл/мин;
Температура колонки от +100 С° (изотерма 2 мин) до 230 С° (изотерма 5 мин), со скоростью подъёма температуры 5 град/мин;
Температура испарителя + 250 С°;
Температура ионного источника + 250 С°;
Температура интерфейса + 250 С°;
Напряжение на детекторе – 0,88кВ;
Поток эмиссии – 60 µА;
Объём пробы – 1µl;
Диапазон сканирования от m/z 30 – 500 Da, (скорость сканирования 1000/0,5 сек).
Идентификацию компонентов проводили путём сравнения масс-спектров с таковыми, имеющимися в распоряжении электронной библиотеки Nist 11.
Статистическую обработку результатов количественного определения ар-турмерона в анализируемых извлечениях из корневищ C. longa L. проводили согласно ГФ XIV, ОФС 1.1.0013.15.
Результаты и их обсуждение. Хроматограмма разделения метоксинонафторбутанового извлечения из корневищ C. longa L. представлена на рисунке 3.
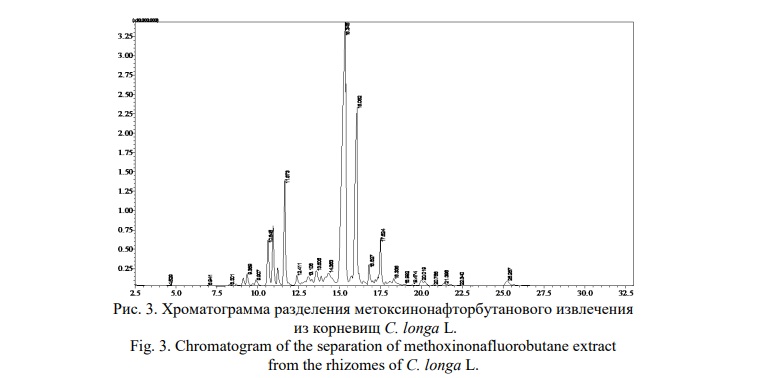
Как видно на приведённой хроматограмме, доминирует пик со временем удерживания 15,346 мин. Настоящий компонент идентифицирован как ар-турмерон, путём сравнения зарегистрированного масс-спектра с образцом из библиотечной базы данных NIST 11 (Рис. 4).
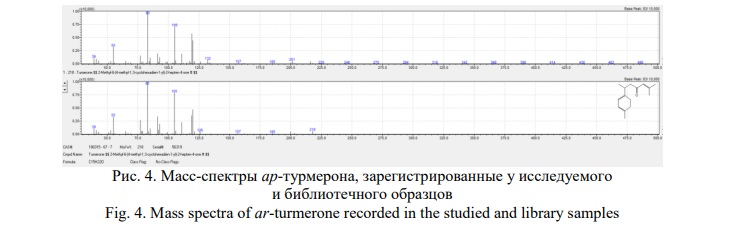
На рисунке 4 видно, что масс-спектры анализируемого и библиотечного образцов совпадают по присутствию основных характеристических пиков молекулярных ионов с зарядом m/z = 122; 105; 83; 55 и 39.
В таблице 1 приведены характеристики пика ар-турмерона, полученные при хроматографировании метоксинонафторбутановго извлечения.
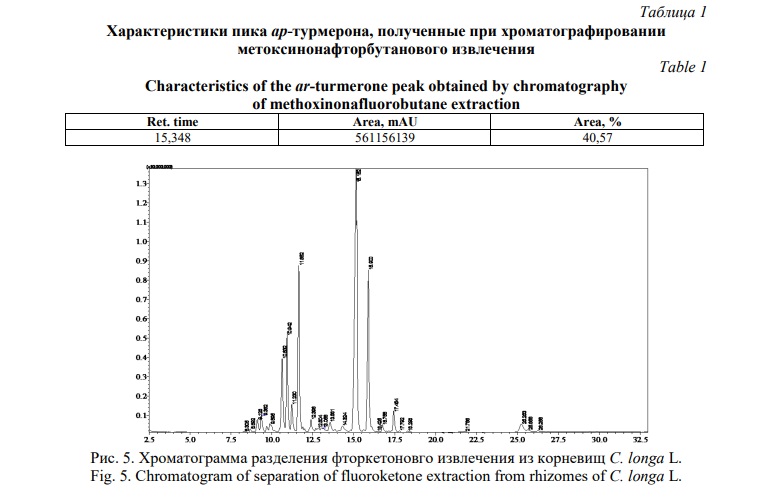
На приведённой хроматограмме также отмечается присутствие доминирующего компонента со временем удерживания 15,152 мин, соответствующего ар-турмерону.
В таблице 2 представлены характеристики пика ар-турмерона, полученные при хроматографировании фторкетонового извлечения.

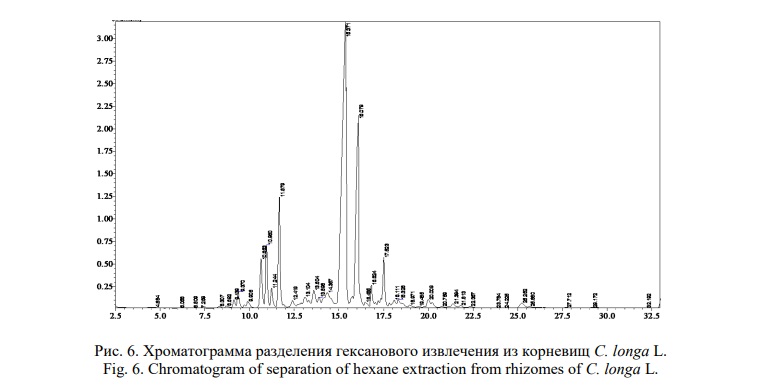
В таблице 3 представлены характеристики пика ар-турмерона, полученные при хроматографировании гексанового извлечения.

Сравнительный анализ площадей пиков ар-турмерона, полученных при хроматографировании анализируемых извлечений из корней C. longa L.представлен на рисунке 7.
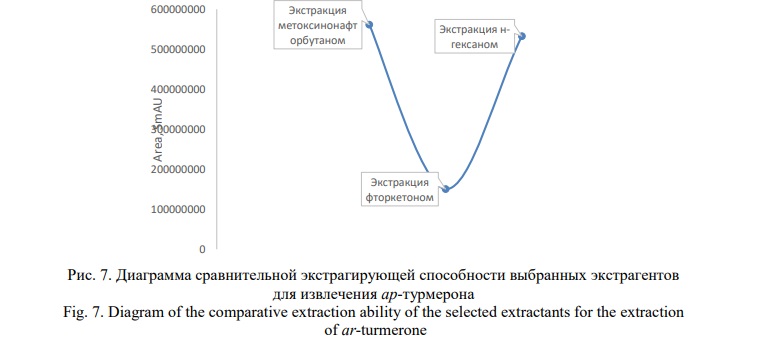
Согласно представленному рисунку, наилучшей экстрагирующей способностью по отношению к ар-турмерону обладает метоксинонафторбутан, при использовании которого площадь пика на хроматограмме оказывается наибольшей, по сравнению с другими взятыми экстрагентами. А содержание указанного компонента в сумме метоксинонафторбутанового извлечения составляет более 40%.
Заключение. В результате проведённых исследований показана перспективность использования фреонов для извлечения ар-турмерона из корневищ C. longa L. Установлено, что оптимальным экстрагентом для ар-турмерона является метоксинонафторбутан; фторкетон показал меньшую экстрагирующую активность. Экстрагирующая способность метоксинонафторбутана по отношению к ар-турмерону оказалась выше таковой экстрагента сравнения – н-гексана. При его использовании в извлечение переходило максимальное количество анализируемого соединения, причём содержание ар-турмерона в полученном суммарном извлечении превышало 40%. Кроме того, метоксинонафторбутан по сравнению с н-гексаном нетоксичен и негорюч, что позволяет использовать его в качестве безопасного экстрагента.
Информация о финансировании
Эта статья была поддержана Программой стратегического академического лидерства РУДН и исследовательским проектом № D.2-A/N-2023 департамента ветеринарной медицины Аграрно-технологического института РУДН (Москва, Россия) под руководством Ватникова Ю.А.





















Список литературы