Влияние саркопении на гемодинамику у пациентов с сердечно-сосудистой патологией при патологическом старении
Aннотация
Актуальность: С возрастом увеличивается количество пациентов с коморбидной патологией и гериатрическими синдромами, в частности – саркопенией. Для диагностики саркопении можно использовать метод биоимпедансного анализа с одновременной оценкой параметров гемодинамики, что важно для подбора антигипертензивной терапии в амбулаторных условиях. Цель исследования:Изучить особенности гемодинамики у пациентов с саркопенией и сердечно-сосудистой патологией для оптимизации тактики применения антигипертензивных препаратов. Материалы и методы:Обследовано 150 пациентов мужского и женского пола, разделенных на 2 возрастные группы: 40-59 лет и 60-74 года. Для диагностики АГ и ИБС использовались рекомендации Европейского (2018) и Российского кардиологического общества (2019, 2020.). Саркопению и ее стадии определяли по критериям EWSGOP 1 с рекомендациями EWSGOP 2. Показатели центральной (сердечный выброс (СВ), ударный объем сердца (УОС)), периферической гемодинамики (САД, ДАД, среднее и пульсовое АД) исследовали с помощью пульсовой волны на биоимпедансном анализаторе «MultiscanBC-OXi» (Россия). Результаты:Сравнительная характеристика пациентов по коморбидной патологии в двух возрастных группах показала, что они различались по распространенности ИБС и АГ, связанной с возрастом (p<0,05). Оценка показателей гемодинамики у пациентов зрелого и пожилого возраста в зависимости от наличия или отсутствия саркопении продемонстрировала, что у лиц с саркопенией отмечались более высокие цифры АД (САД, ДАД, ПАД, Ср. АД, р<0,05). Влияние саркопении также выражалось и в увеличении СВ и УОС как в зрелом, так и в пожилом возрасте, в сравнении с пациентами без саркопении (p<0,05), что является дополнительным показанием к назначению бета-блокаторов для уменьшение гиперсимпатикотонии. Заключение:Наличие саркопении у пациентов старше 40 лет влияет на параметры гемодинамики, что следует учитывать при назначении антигипертензивной терапии. Значения СВ и УОС у пациентов с саркопенией могут быть дополнительными показаниями для включения бета-блокаторов в комбинированную терапии АГ
Введение. Увеличение средней продолжительности жизни, связанное с прогрессом медицины, приводит к росту числа людей старших возрастных групп как в развитых, так и в развивающихся странах [1]. Пациенты старше 60 лет – это основной контингент стационаров и амбулаторных приемов. Помимо наличия коморбидной патологии, у пациентов старших возрастных групп часто встречаются и возраст-ассоциированные состояния, в частности, саркопения. Считается, что саркопения, заболевание, связанное с нарушением мышечной функции – один из пяти основных факторов риска заболеваемости и смертности у лиц старше 65 лет [2-7]. У пациентов этой возрастной группы наличие саркопении свидетельствует о патологическом старении в форме снижения функциональности.
В зрелом возрасте саркопения довольно часто встречается у пациентов с ожирением и является причиной преждевременного старения, которое также представляет собой форму патологического старения.При патологическом старении саркопения сочетается с полиморбидным фоном, основу которого составляют сердечно-сосудистые заболевания: АГ, ИБС, нарушения ритма, ХСН и др. Чтобы подтвердить диагноз саркопении необходимо оценить активную клеточную массу (или мышечную массу), жировую массу и их пропорции. Оценка данных показателей возможна с помощью биоимпедансного анализа (БИА) – метода, который позволяет оценить широкий спектр морфологических и физиологических параметров организма путем измерения электрического сопротивления, основанного на способности биологической ткани проводить слабые электрические токи [8-11].
В последнее время БИА часто используется в клинической медицине: его преимущество заключается в том, что он является малозатратным, неинвазивным, безопасным. С его помощью можно проводить диагностику различных заболеваний, в том числе и саркопении [12-16]. При помощи БИА возможна оценка параметров центральной и периферической гемодинамики, исходя из цифрового анализа пульсовой волны, что может иметь значение для подбора гипотензивных препаратов. Представляется актуальным изучение влияния саркопении на показатели гемодинамики у больных с сердечно-сосудистыми заболеваниями для оптимизации антигипертензивной терапии.
Цель исследования. Изучить особенности гемодинамики у пациентов с саркопенией и сердечно-сосудистыми заболеваниями для оптимизации тактики применения антигипертензивных препаратов.
Материалы и методы исследования. Исследование состояло из двух основных этапов. На первом этапе мы провели сравнительную характеристику пациентов по распространенности коморбидной патологии в зависимости от принадлежности к зрелому или пожилому возрасту. В исследование были включены 150 пациентов зрелого и пожилого, наблюдаемые на терапевтическом участке ОГБУЗ «Поликлиника №3» г. Смоленска, с ИБС (СН 1-4 ФК), АГ1-3 ст., сахарным диабетом (СД) 2 типа в стадии компенсации, ожирением 1-3 ст. Первую (1-ю) группу составили пациенты зрелого возраста(40-59 лет) (n=46, средний возраст 52,5±4,5 лет); вторую (2-ю) группу составили пациенты пожилого возраста (60 лет – 74 года) (n=104, средний возраст 69,7±3,7 года).
На втором этапе мы изучали влияние саркопении на состояние гемодинамики при сердечно-сосудистой патологии. Для этого пациенты 1-й и 2-й групп внутри каждой группы были разделены на две подгруппы в зависимости от наличия/отсутствия саркопении:
- я группа: подгруппа 1.1 (n=28, средний возраст 52,4±4,2 года) без саркопении, подгруппа 1.2 (n=18, средний возраст 52,6±5,1 года) с саркопенией;
- я группа: подгруппа 2.1 (n=63, средний возраст 69,7±4,4 года) без саркопении, подгруппа 2.2 (n=41, средний возраст 69,9±3,3 года) с саркопенией;
Исследование носило выборочный характер при проведении диспансеризации. От всех пациентов получено письменное информированное согласие на участие в исследовании.
Всем пациентам были проведены общеклинические методы исследования: оценка общего состояния, ЧСС, АД (офисные значения), ИМТ, ЭКГ в 12 отведениях, оценивали показатели общего анализа крови и мочи, биохимические показатели: глюкоза и общий холестерин. АГ диагностировали, используя данные рекомендаций Европейского (2018 г.) и Российского кардиологического обществ (РКО, 2019 г.). Диагностика ИБС проводилась по клиническим рекомендациям (РКО, 2020 г.). Диагноз сахарного диабета (СД) 2 типа верифицировали на основании показателей глюкозы крови натощак и суточного профиля глюкозы крови.
Наличие или отсутствие саркопения выявляли согласно критериям EWSGOP 1 с рекомендациями EWSGOP 2. Определение мышечной массы (ММ) проводилось c использованием биоимпедансного анализа, на аппарате «Multiscan BC-OXi» (Россия). Мышечную окружность плеча (МОП) измеряли с помощью сантиметровой ленты. За норму у мужчин принимали значение 21,1 см. и более, а у женщин – 19,9 см. и более; за норму окружности голени (ОГ) как у мужчин, так и у женщин принимали значение более 31 см. Мышечную силу (МС) оценивали методом кистевой динамометрии с использованием кистевого динамометра (TVES–DMER–120). Пороговыми значениями для диагностики снижения МС были: менее 27 кг для мужчин и менее 16 кг для женщин (EWSGOP 2) на доминантной руке. Мышечная функция (МФ) оценивалась при помощи теста «скорость ходьбы на 4 м», если скорость походки была менее 0,8 м/с, то данное значение учитывали как критерий саркопении. Стадии саркопении верифицировали по данным критериям в EWGSOP 1 (2010) c рекомендациями EWSGOP 2 (2018). Пресаркопения диагностировалась в случае, если было выявлено снижение только ММ, а МС и МФ были в норме, саркопения диагностировалась, когда были снижены ММ и МС или МФ, а тяжелая саркопения характеризовалась снижением и ММ, и МС, и МФ.
Определяли параметры центральной гемодинамики: сердечный выброс (СВ) и ударный объем сердца (УОС) с помощью анализа цифровой пульсовой волны с использованием биоимпедансометрии. За диапазон индивидуальной нормы принимали значения СВ от 4,2 до 5,2 L\min, а у УОС – от 60 до 90 мл. Также дополнительно анализировались следующие показатели: систолическое АД (САД), диастолическое АД (ДАД), пульсовое АД (ПАД), среднее АД (Ср.АД), полученные с помощью офисного измерения АД и данных биоимпедансометрии.
Для статистического анализа результатов исследования использовалась программа Microsoft Excel 2013. Для качественных данных описательная статистика приведена в виде относительных частот и абсолютных значений (%, n). Критерий Манна-Уитни использовался для сравнения количественных показателей между двумя группами. При p<0,05 различия считались статистически значимыми.
Результаты и их обсуждение. Сравнительная характеристика пациентов по распространенности коморбидной патологии в двух возрастных группах – 1 гр. (40-59 лет) и 2 гр. (60-74 года) в зависимости от гендерных различий представлена в таблице 1.
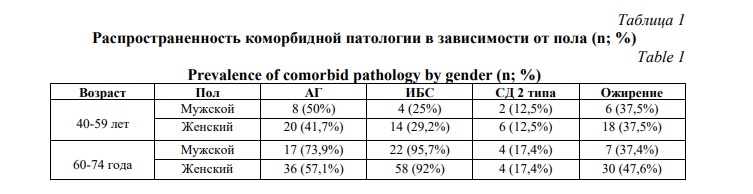
Сравнительная характеристика пациентов по распространенности коморбидной патологии в двух возрастных группах показала, что они различались по частоте встречаемости ИБС (29,2% в 1 гр., и 92% во 2 гр., соответственно, p<0,05,). АГ также встречалась чаще во 2 группе (50% в 1 гр. и 73,9% во 2 гр., соответственно, p<0,05), в то время как СД 2 типа в ст. компенсации и ожирение I-III степени встречалось с одинаковой частотой. Таким образом, из представленных данных видно, что пациенты 2 разных возрастных групп были сопоставимы по распространенности СД и ожирения. Частота встречаемости ИБС и АГ увеличивалась с возрастом.
Дальнейшее исследование показателей гемодинамики в зависимости от наличия саркопении (С+)/отсутствия саркопении (С-) продемонстрировало, что у пациентов с С+ в исследуемых группах были выявлены более высокие цифры АД – систолического АД (САД), диастолического АД (ДАД), пульсового АД (ПАД), среднего АД (Ср. АД), в сравнении с пациентами без саркопении (р<0,05) как у пациентов зрелого, так и пожилого возраста. Данные представлены в таблице 2.
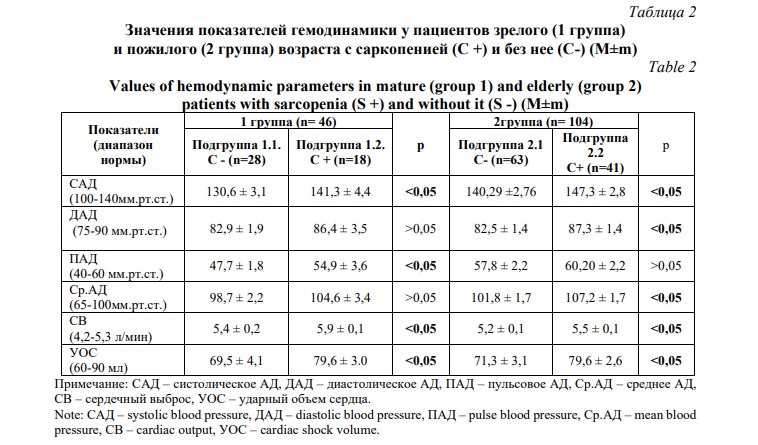
Анализ полученных данных показал, что у пациентов с саркопенией как в зрелом (подгруппа 1.2), так и в пожилом возрасте (подгруппа 2.2) отмечались более высокие цифры АД (САД, ДАД, ПАД, Ср АД, р<0,05), СВ и УОС (р<0,05). Таким образом, влияние саркопении выражалось в активации симпато-адреналовой системы (САС), что приводило к увеличению СВ и УОС как в зрелом, так и в пожилом возрасте. Известно, что активация САС является одним из ведущих патогенетических механизмов повышения АД, приводящее к поражению органов мишеней, повышению ЧСС и развитию эндотелиальной дисфункции, и, в конечном счете, развитию ХСН. Следует отметить, что, в основном, все исследования связанные с изучением влияния ингибиторов РААС и САС на предотвращение атрофии мышц были посвящены проблеме ХСН. В исследовании COPERNICUS была продемонстрирована способность карведилола предотвращать потерю веса у больных с сердечной недостаточностью, причем его способность увеличивать массу тела была наиболее выражена у лиц со сниженным ИМТ на исходном уровне. Все стратегии, направленные на сохранение мышечной массы и увеличение мышечной силы будут способствовать замедлению прогрессирования ХСН. Поэтому, как немедикаментозные методы (регулярные физические тренировки), так и медикаментозные (блокада РААС и САС, прием витамина D) остаются краеугольным камнем в терапевтических стратегиях в лечении этой нозологии.
Уменьшение гиперсимпатикотонии за счет снижения ЧСС и УОС достигается с помощью бета-блокаторов. Применение фиксированных комбинаций (ФК), в частности бета-блокатора и иАПФ, очень важно с целью вторичной профилактики, а также лечения ИБС, особенно у пациентов старше 40 лет с наличием АГ, т.к. в этой возрастной когорте увеличивается частота встречаемости ИБС. Основная проблема вторичной профилактики при ИБС – низкая частота использования ФК, содержащий бета-блокатор с иАПФ у пациентов с АГ в сочетании с ИБС, с учетом того, что это полиморбидная патология встречается до 80% случаев как в стационарных, так и в амбулаторных условиях. При наличии у пациента АГ и ИБС, а также ранее перенесенного инфаркта миокарда, патогенетически целесообразно назначения ФК (бета-блокатор + иАПФ), которые будут воздействовать на нейроэндокринные механизмы, приводящие к уменьшению ЧСС, расширению кровеносных сосудов и ряду других факторов, которые в конечном итоге приводят к достижению целевого уровня АД и к контролю стенокардии [16]. Однако, наиболее часто таким пациентам назначают ФК, содержащую диуретик в сочетании с иАПФ, а бета-блокаторы включают в схему в основном при особых показаниях, к которым относятся: ХСН, предшествующий инфаркт миокарда и фибрилляция предсердий.
Учитывая способность бета-блокаторов уменьшать гиперактивацию симпатоадреналовой системы, являющуюся ключевым патогенетическим механизмом развития АГ, они входят в 5 основных классов применяемых в антигипертензивной терапии [17]. Также для терапии ИБС и ХСН бета-блокаторы используются как основные препараты первой линии. В Российских и в европейских рекомендациях перенесенный инфаркт миокарда среди пациентов с АГ является основанием для назначения бета-блокаторов [18, 19]. Однако, важное значение в улучшении антигипертензивной терапии имеет и такой параметр как гемодинамический статус конкретного пациента, который может быть гипо-, эу- и гиперкинетическим. Исходя из этого, рекомендуется использовать бета-блокаторы у пациентов как с эукинетическими, так и гиперкинетическими гемодинамическими типами. Для определения параметров гемодинамики можно использовать БИА, который является простым, безвредным и удобным в амбулаторных условиях. Сущность применяемого подхода заключалась в коррекции гипотензивной терапии у пациентов с АГ и ИБС, с помощью определения показателей СВ и УОС, исходя из цифрового анализа пульсовой волны с использованием ФК содержащий бета-блокатор.
Высокие значения УОС и СВ – это дополнительные показания для использования бета-блокаторов. Метод БИА можно применять для расчета показателей гемодинамики, которые имеют определенную значимость для повышения эффективности антигипертензивного лечения при помощи анализа пульсовой цифровой волны. Бета-блокаторы действую на СВ, УОС и ЧСС уменьшают гиперсимпатикотонию и, соответственно, степень поражения органов-мишеней.
Заключение. Результаты настоящего исследования показали, что наличие саркопении у пациентов старше 40 лет влияет на параметры гемодинамики (приводит к увеличению показателей АД - САД, ДАД, ПАД, Ср. АД и показателей СВ и УОС), что следует учитывать при назначении антигипертензивной терапии. Значения СВ и УОС у пациентов с саркопенией могут быть дополнительными показаниями для включения бета-блокаторов в комбинированную терапии АГ.
Информация о финансировании
Финансирование данной работы не проводилось.





















Список литературы