Механизмы биологической эффективности ионных форм металлов переменной валентности в респираторной медицине
Aннотация
Актуальность: Вопросы разработки новых лекарственных препаратов, содержащих металлы переменной валентности, нуждаются в систематизации наших знаний, проведении экспериментальных и клинических исследований. Цель исследования:Изучение механизмов эффективности минерального комплекса, содержащего металлы переменной валентности, в лечении респираторных заболеваний, проведение доклинических испытаний и клинической апробации нового ингаляционного минерального раствора. Материалы и методы:Способность ионов церия (III) проявлять восстановительные свойства продемонстрирована путем проведения химических реакций хлорида и сульфата церия (III) с перманганатом калия в присутствии едкого натрия или серной кислоты (соответственно). Доклинические исследования острой токсичности проведены на лабораторных мышах и крысах с соблюдением правил биоэтики в соответствии с общепринятыми этическими нормами обращения с животными, на основе стандартных операционных процедур университета, которые соответствуют правилам, принятым Европейской Конвенцией по защите позвоночных животных, используемых для исследовательских и иных научных целей (Страсбург, 1986). Клиническая апробация двух форм минерального комплекса для ингаляций (1. раствор для ингаляций с применением небулайзера – Ренериум; 2. интраназальный спрей) проведена на 6 группах волонтеров с соблюдением прав человека и принципов проведения медицинских исследований с участием человека в качестве субъекта, декларированных на 18-й Генеральной Ассамблее Всемирной Медицинской Ассоциации (Хельсинки, Финляндия), добровольного информированного согласия, утвержденного локальным этическим комитетом. Результаты:Минеральный препарат для ингаляционной терапии больных острыми респираторными заболеваниями не проявляет острой токсичности в доклинических исследованиях на лабораторных животных. Механизм действия препарата, наиболее вероятно, связан с регуляцией окислительно-восстановительных реакций на уровне мембраны клетки, митохондрий и ядра клетки, что проявляется противовоспалительной и регенераторной активностью в области слизистой оболочки дыхательных путей и альвеолярного аппарата. Обе формы препарата хорошо переносятся. Отмечена выраженная клиническая эффективность препарата Ренериум в форме ингаляций через компрессорный ингалятор в случае курсового 5-и дневного лечения по 5 мл один раз в день. Заключение:Экспериментальные и клинические данные продемонстрировали выраженные противовоспалительные и регенераторные свойства нового минерального комплекса на основе церия (III), механизм которых обусловлен регуляцией окислительно-восстановительных реакций
Ключевые слова: металлы переменной валентности, ионы церия, окислительно-восстановительные реакции, доклинические исследования, клиническая апробация
Введение. Острые респираторные заболевания стабильно лидируют среди причин временной утраты трудоспособности [1]. По данным Роспотребнадзора ежегодно в России регистрируется более 52 млн. случаев острых респираторных заболеваний [2]. Особую актуальность данная проблема приобретает в период эпидемий и пандемии. В 2020 году количество дней временной утраты трудоспособности по причине заболеваний органов дыхания в России составило 123 881 555. Значительный вклад респираторных заболеваний отмечается и в структуре смертности населения, прежде всего, за счет хронической обструктивной болезни легких и пневмонии [3], что указывает на особую значимость разработки методов эффективной терапии. Повреждение эпителия различных уровней дыхательных путей имеет большое значение в развитии симптомов заболевания и нарушения вентиляционной функции, но общие вопросы этой проблемы остаются недостаточно изученными, рассматриваются в основном с позиции воспаления или врожденной цилиарной дисфункции [4, 5, 6]. Рекомендации в отношении повреждения эпителиальных структур состоят в регуляции реологических свойств мокроты и применении ингаляционных либо системных глюкокортикоидов [7, 8]. Препараты, обладающие антиоксидантными свойствами, нашли применение только при интерстициальных заболеваниях легких, в области решения проблем пересадки легких, но не имеют четких рекомендаций для лечения повреждения эпителия дыхательных путей в случае инфекционной патологии и многих других состояниях [9, 10, 11]. Недостаточно изученными остаются вопросы регуляции функций мембраны эпителиальных клеток, митохондриальной дисфункции, пролиферативной активности, включая скорость регенерации при вирусных и других острых респираторных заболеваниях [12]. Для решения ряда перечисленных проблем предложены минеральные комплексы, в том числе, содержащие металлы переменной валентности, способные оказывать влияние на содержание продуктов пероксидации и накопление АТФ в клетках. В отдельных клинических наблюдениях получены впечатляющие результаты редуцирования симптомов острого респираторного заболевания при ингаляционном применении препарата Ренериум, содержащего ионы церия, марганца, цинка и серебра. Механизм действия указанного комплекса недостаточно обсуждался в научной литературе, и требует дальнейшего изучения.
Цель исследования. Изучение механизмов эффективности минерального комплекса, содержащего металлы переменной валентности, в лечении респираторных заболеваний, проведении доклинических испытаний и клинической апробации нового ингаляционного минерального раствора.
Материал и методы исследования
Лабораторные методы изучения химических реакций
Исследовали окисление хлорида церия (III) и сульфата церия (III). В качестве окислителя использовали раствор KMnO4 (1 мг/100 мл). Исследования выполнены на базе ФГБОУ ВО ПГМУ им. академика Е.А. Вагнера (кафедра пропедевтики внутренних болезней №1) и ООО «Ренериум». Реакцию проводили путем смешивания растворов при комнатной температуре.
Раствор хлорида церия (III) готовили путем растворения химически чистого CeCl3 семиводного, производство ООО "Химкрафт", в дистиллированной воде или в 0,9% растворе хлорида натрия, готовили концентрацию 1 мг/л.
Раствор сульфата церия (III) готовили путем растворения химически чистого Ce2(SO4)3 восьмиводного, производство ООО "Химкрафт", в дистиллированной воде или в 0,9% растворе хлорида натрия, готовили концентрацию 1 мг/л.
Дополнительно использовали растворы 1H NaOH и 1H H2SO4 производства ООО «АО РЕАХИМ».
Исследования с участием лабораторных животных выполнены на базе вивария ЦНИЛ ФГБОУ ВО ПГМУ им. академика Е.А. Вагнера Минздрава России. Изучение острой токсичности выполнено на лабораторных белых мышах и белых крысах обоих полов. Общее количество животных составило 18 мышей и 18 крыс.
Использовали модель острого бронхита, сформированную у крыс путем ингаляции 1% раствора формалина [13]. В исследовании приняли участие 18 животных обоих полов. Камера для ингаляций представляла собой эксикатор, объемом 5 литров, имеющий трубки для поступающего воздуха и отведения воздуха из камеры. К трубке поступающей воздушной смеси подключали небулайзерный компрессорный ингалятор с испытуемым раствором. Ингаляцию проводили в течение 20 минут, используя 5 мл раствора исследуемого или контрольного раствора. Животные были разделены на две равные по количеству группы случайным образом. Контрольная группа получала только однократную ингаляцию 1% раствора формалина. Группа наблюдения после ингаляции 1% раствора формалина получала ежедневные ингаляции исследуемого раствора, содержащего ионы церия (0,35-0,50 мкг/л), марганца (10-20 мкг/л), цинка (5-7 мкг/л) и серебра (0,15-0,20 мкг/л) в 0,9% растворе NaCl. Лечебные ингаляции начинались в день формирования модели острого бронхита и выполнялись 1 раз в день на протяжении 5 дней. На 6-й день эксперимента животных взвешивали, проводили другие контрольные исследования и подвергали эвтаназии путем их помещения в камеру, содержащую пары этилового эфира для наркоза.
Исследования на здоровых и больных проводились на основании полученного положительного решения Этического комитета ФГБОУ ВО ПГМУ им. академика Е.А. Вагнера Минздрава России на проведение клинических испытаний нового лекарственного препарата (Протокол № 12 от 23.12.2021 г.). Исследования зарегистрировано в Министерстве здравоохранения Российской Федерации № 123062200020-2, выполнялись на базе ФГБОУ ВО ПГМУ им. академика Е.А. Вагнера Минздрава России и ГАУЗ ПК ГКБ №4 г. Перми.
План клинической апробации включал: 1) определение безопасности препарата на здоровых волонтерах (48 человек); 2) клиническую апробацию эффективности в форме сравнительного исследования с включением 101 пациента с острыми вирусными респираторными заболеваниями, внебольничной пневмонией, бронхиальной астмой, хронической обструктивной болезнью легких и хроническим деформирующим бронхитом с единичными цилиндрическими бронхоэктазами. Условием проведения клинической апробации было подписанное информированное согласие.
Клиническую апробацию выполняли на добровольцах в следующих клинических группах:
- Группа практически здоровых лиц в возрасте 19-61 лет, м 5, ж 16, получавших интраназальный спрей Ренериум А по 1 дозе 2 раза в день на протяжении 5 дней.
- Группа практически здоровых лиц в возрасте 19-61 лет, м 11, ж 16, получавших ингаляции препарата Ренериум через компрессорный небулайзерный ингалятор в объеме 5 мл на 1 ингаляцию 1 раз в день на протяжении 5 дней.
- Группа больных ОРВИ без идентификации возбудителя в форме ринита, фарингита, бронхита в возрасте 22-64 лет, м – 12, ж – 21, получавших интраназальный спрей Ренериум А по 1 дозе 2 раза в день на протяжении 5 дней.
- Группа больных ОРВИ без идентификации возбудителя в форме ринита, фарингита, бронхита в возрасте 21-67 лет, м – 9, ж – 11, получавших симптоматическое лечение назальными деконгестантами, а также интраназальный спрей 0,9% раствора хлорида натрия (контрольная группа).
- Группа больных, перенесших коронавирусную инфекцию в форме пневмонии с формированием постковидного синдрома при наличии умеренно выраженной гипоксической дыхательной недостаточности (SpO2 88-95%) и нарушении толерантности к физической нагрузке. Возраст 23-59 лет, м – 9, ж – 12. Больные получали ингаляции препарата Ренериум через компрессорный небулайзерный ингалятор в объеме 5 мл на 1 ингаляцию 1 раз в день на протяжении 5 дней на фоне стандартной терапии.
- Группа больных, перенесших коронавирусную инфекцию в форме пневмонии с формированием постковидного синдрома при наличии умеренно выраженной гипоксической дыхательной недостаточности (SpO2 88-95%) и нарушении толерантности к физической нагрузке. Возраст 19-63 лет, м – 11, ж – 16. Больные получали стандартную терапию ингаляционными глюкокортикоидами в комбинации с бета2-агонистами в средних терапевтических дозах, а также ингаляции 0,9% раствора хлорида натрия по 5 мл через компрессорный небулайзерный ингалятор 1 раз в день на протяжении не менее 5 дней (контрольная группа).
Применяли сравнительный, параллельный, рандомизированный, ослепленный дизайн клинического исследования.
Группа практически здоровых лиц, получавших ингаляционный препарат Ренериум, была представлена студентами ФГБОУ ВО ПГМУ им. академика Е.А. Вагнера Минздрава России, а также взрослыми здоровыми волонтерами 2-го зрелого возраста различных профессий. Всего обследовано 48 человек, из них 16 мужчин и 32 женщины в возрасте 19-61 лет. Все участники исследования подписали информированное согласие.
Критерии включения соответствовали наличию заболевания и подписанию добровольного информированного согласия на участие в исследовании, обозначенного для группы исследования. Критерии исключения: тяжелое течение острого респираторного заболевания, наличие острой дыхательной недостаточности, лихорадка выше 37,1 °С, клинические симптомы сердечной, почечной, печеночной недостаточности, синдромы цитолиза и холестаза, кахексии, психических или поведенческих нарушений, алкогольной или наркотической зависимости, нарушений сердечного ритма, хроническая болезнь почек, сахарный диабет, заболевания центральной нервной системы, эндокринных желез, иммунодефицитные состояния, когнитивные нарушения, наличие другой клинически значимой соматической патологии или мотивированный отказ от участия в исследовании, а также детский или старческий возраст.
Оценивали выраженность одышки по шкале Борга, интенсивность кашля по визуально-аналоговой шкале, толерантность к физической нагрузке на основании визуально-аналоговой шкалы, принимая за 10 баллов – способность переносить чрезмерные физические нагрузки, 0 – неспособность одеться и выйти из дома.
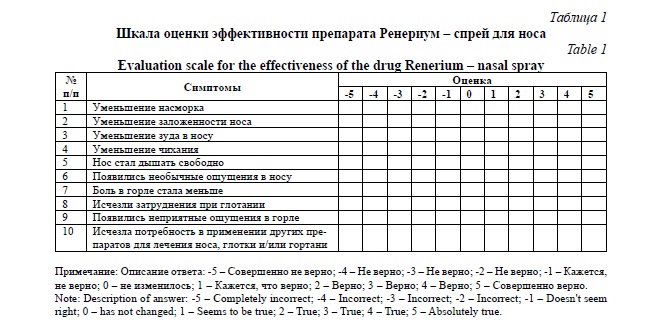
Оценка динамики симптомов проводилась на основе шкал Ликерта (Табл. 1, 2). Все больные, перенесшие коронавирусную инфекцию, обследованы в условиях стационара пульмонологического отделения ГАУЗ ПК ГКБ № 4 согласно Временным клиническим рекомендациям: профилактика, диагностика и лечение новой коронавирусной инфекции (Covid-19). Версия 15 (22.02.2022) и Временным методическим рекомендациям: Медицинская реабилитация при новой коронавирусной инфекции (Covid-19). Версия 2 (31.07.2020). [14, 15].

Дополнительно 10 пациентов основной группы и 11 из группы сравнения (группа 6, получавших ингаляции 0,9% раствора хлорида натрия) использовали смарт-часы Amazfit U Bip Pro с функциями оценки сатурации кислорода, ЧСС, дистанции пройденного пути, количества шагов, продолжительности и фазы ночного сна.
Исследуемые минеральные комплексы
Препарат Ренериум изготовлен ООО «Ренериум» в гепариновых флаконах по 5 мл прозрачной бесцветной жидкости, содержит раствор ионов церия (0,35-0,50 мкг/л), марганца (10-20 мкг/л), цинка (5-7 мкг/л) и серебра (0,15-0,20 мкг/л) в 0,9% растворе NaCl. Раствор стерильный, предназначен для ингаляций по 5 мл 1 раз в день. Курс лечения состоит из 5 ингаляций.
Интраназальный спрей (средство гигиены для ухода за полостью носа) имеет состав, близкий к ингаляционной форме с добавлением гидрокарбоната натрия (пищевой соды), сульфата магния (20-30 мкг/л), минимального количества эфирных масел можжевельника и отличается меньшим содержанием хлорида натрия. Жидкость бесцветная, прозрачная с легким запахом можжевельника, выпускается во флаконах-спрей по 10,0 мл или в пластиковых флаконах с капельницей по 10, 25 и 50 мл.
Препарат применялся в форме спрея в каждую половину носа не менее 2 раз в день (пациент мог самостоятельно регулировать количество раз применения препарата в зависимости от выраженности симптомов острого заболевания верхних дыхательных путей). Максимальная доза составила 5 мл препарата в сутки.
Для изучения роли каждого компонента препарата и их взаимодействия были изготовлены опытные партии моно- и двухкомпонентных препаратов, которые приготовлены в виде прозрачных бесцветных растворов по 10 мл во флаконах назального спрея. Клинические наблюдения выполнены на участниках научного коллектива, имеющих клинические симптомы нетяжелого острого респираторного вирусного заболевания с поражением верхних дыхательных путей без идентификации вируса на основании их добровольного согласия. Препарат вводили в обе половины полости носа по 1-2 дозы в каждый носовой ход многократно на протяжении суток так, чтобы суточная доза приближалась к 10 мл препарата.
Использовали раствор, содержащий CeCl3 (доза ионов Ce3+ 0,5 мкг/л), назальный спрей; ZnSO4 (доза ионов Zn2+ 5 мкг/л, назальный спрей), а также комбинированный препарата, содержащий раствор CeCl3 и ZnSO4 в указанных дозировках.
Статистическая обработка результатов клинической апробации проводилась с применением программного пакета Statictica 10.0. Частота выявления и динамики симптомов оценивалась относительной величиной в % к общему числу пациентов в группе. При обработке шкал Ликерта использовали подсчет среднеарифметического значения баллов. Сравнительный анализ проводили с использованием критерия Манна-Уитни.
Результаты. Лабораторные методы изучения химических реакций выполнены с целью определения характера взаимодействий микроэлементов переменной валентности в системе. Известно, что увеличение степени валентности элемента называется окислением, а снижение – восстановлением, что соответствует понятию окислительно-восстановительных реакций двух и более химических элементов, один из которых является окислителем, а другой восстановителем. В условиях воспалительной реакции и патологии слизистой оболочки респираторного тракта возникают реакции перекисного окисления, где одним из основных окислителей является супероксидный радикал O2-. При взаимодействии с водой супероксидный радикал способен образовать перекись водорода:
2 O2- + 2 H2O → 2 H2O2 + O2 (1)
В реакции перекисного окисления принимают участие и другие окислители, активность которых объясняется наличием неспаренного электрона на внешнем электронном уровне электронной оболочки атома кислорода: гидроксильный радикал (HO•); гидроксид-ион (HO-); триплетный кислород (O22•); пероксид-ион (O22-) и оксид азота (NO•).
100 мл раствора KMnO4 в качестве окислителя смешивали с исследуемыми растворами в стеклянном стакане. Установлено, что при смешивании растворов KMnO4 с CeCl3, в присутствии 1H NaOH, наблюдается химическая реакция, сопровождаемая изменением розового цвета раствора перманганата калия на бурый с выпадением осадка коричневого цвета. Реакция описывается уравнением:
3 CeCl3 + KMnO4 + 8 NaOH + 2 H2O = 3 Ce(OH)4 + MnO2 + KCl + 8 NaCl (2)
При смешивании растворов KMnO4 с Ce2(SO4)3, в присутствии 1H H2SO4, прозрачный малиновый раствор перманганата калия заметно светлеет, сохраняя розовый оттенок без выпадения осадка. Реакция описывается уравнением:
5 Ce2(SO4)3 + KMnO4 +H2SO4 = Ce(SO4)2 + K2SO4 + MnSO4 + H2O (3)
Одновременно с этим в присутствии раствора формалина (HCHO) в качестве субстрата, протекает реакция окислителей с молекулами формалина в кислой среде, например:
5HCHO + 4KMnO4 +6H2SO4=4MnSO4+2K2SO4+5CO2(газ)+11H2O (3.1)
Ионы Ce4+ также способны окислять молекулы формалина:
HCHO + 4CeCl4 + 2H2O = 4CeCl3 +4HCl + CO2 (3.2),
и в нейтральной среде эта реакция сопровождается подкислением раствора (HCl).
Описанные реакции делают возможным прямое окисление формалина или другого субстрата на внешней поверхности клеточной мембраны. При этом следует учитывать, что для полного окисления продуктов интоксикации необходимо предположить механизм постоянного восстановления окислителя. Такой механизм возможен, например, при реализации колебательной реакции окисления Ce (III).
Представленные результаты подтверждают возможность окисления соли церия (III) с образованием гидроксида церия (IV), образующего осадок (вместе с осадком MnO2). Во втором случае окисления соли церия (III) до сульфата церия (IV) сопровождалось изменением цвета раствора. В биологических объектах, на поверхности воспаленной слизистой оболочки бронхов и поврежденного эпителия с участием супероксид-аниона, а также других окислителей реакция приобретает вид, описываемый уравнениеv
Ce (IV) + O2 (4)
Изменение валентности ионов церия (III) на (IV) подтверждает восстановительные (антиокислительные) свойства ионов церия (III), и указывает на возможность клинического применения минеральных комплексов, содержащих ионы церия (III) в лечении воспалительных заболеваний респираторного тракта с поражением эпителиальных клеток.
Исследование острой токсичности с участием лабораторных животных на протяжении 14 дней не выявили, каких-либо изменений со стороны органов дыхания, так и со стороны внутренних органов мышей и крыс, включенных в эксперименты при превышении терапевтической дозы минерального комплекса Ренериум в 20 раз.
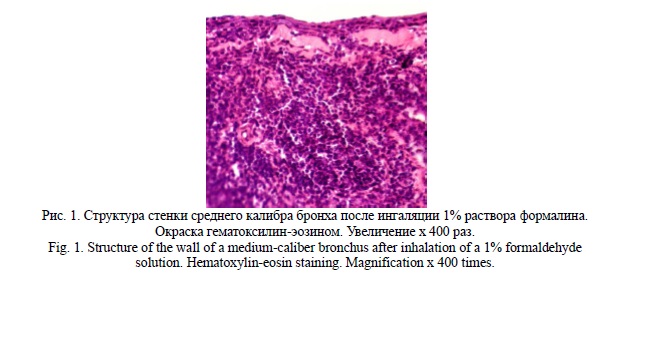
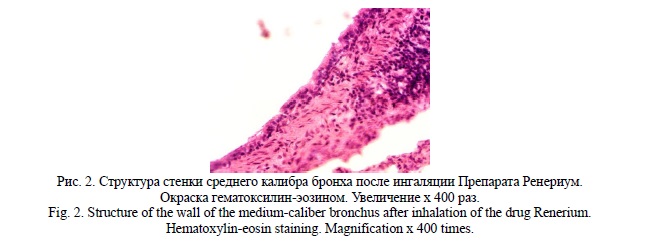
Результаты оценки эффективности терапевтической дозы препарата Ренериум в модели острого бронхита у крыс, вызванного ингаляцией 1% раствора формалина, показали активную регенерацию эпителия, уменьшение инфильтрации стенки бронхов и бронхиол, восстановление структуры базальной мембраны. (6-й день после начала терапии) по сравнению с группой животных с острым бронхитом, не получавших лечение (Рис. 1, 2).
Клиническая апробация
Группа 1 (практически здоровые лица). На момент обследования пациенты отрицали наличие острого респираторного заболевания, а также хронических болезней. Тем не менее, при интерактивном опросе у части обследованных выявлены единичные респираторные симптомы в виде кашля, а также легкие ограничения физической активности (среди лиц второго зрелого возраста). В процессе терапии препаратом интраназальный спрей Ренериум А статистически значимых изменений симптомов не установлено. В контрольной группе практически здоровых лиц, из 21 человека, только в 2-х случаях было отмечено появление небольших светлых выделений из носа на фоне применения препарата.
Группа 2 (практически здоровые лица). В процессе ингаляционной терапии статистически значимых изменений симптомов не установлено, но в одном случае отмечено появление слабоинтенсивного кашля с небольшим количеством мокроты белого цвета (не более 5 мл в сутки).
Результаты оценки респираторных симптомов в группе практически здоровых лиц под влиянием ингаляционного препарата Ренериум представлены в таблице 3.

Группа 3 (пациенты с острым респираторным заболеванием, получавшие интраназальный спрей Ренериум А). Оценка динамики симптомов заболевания в форме ответов на вопросы шкалы Ликерта представлены в таблищах 4, 4а.
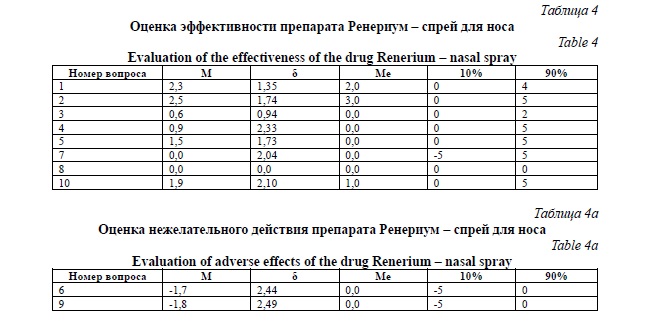
Результаты соответствовали утверждениям об уменьшении заложенности носа, насморка, уменьшении количества применяемых лекарственных препаратов для облегчения носового дыхания и ощущению свободы носового дыхания. При этом у большинства пациентов не возникало необычных ощущений в носу или в горле, а имеющиеся указанные побочные действия у 1 человека носили слабовыраженный характер (2 балла по 5-бальной шкале). Большинство пациентов пожелали повторно применить Ренериум А – спрей средство гигиены для ухода за полостью носа и рта, если вновь возникнут проявления острого респираторного заболевания. Вместе с тем, эффективность препарата была умеренной у большинства больных и только 4 пациента дали 5-бальные оценки эффективности из 5 возможных баллов (20% пациентов).
Группа 4 (группа контроля – пациенты с острым респираторным заболеванием, получавшие традиционную терапию). Результаты клинической эффективности представлены в таблицах 5 и 5а.
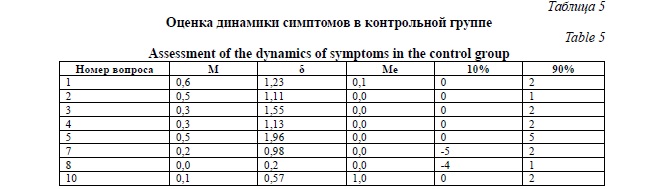
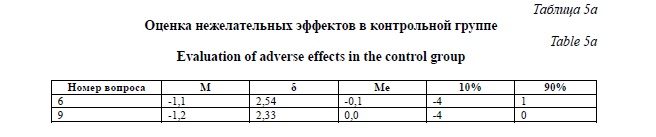
Результаты эффективности лечения в контрольной группе были сомнительными.
Группа 5. Основная группа больных имела проявления новой коронавирусной инфекции Covid-19 в форме пневмонии с визуальной оценкой КТ-картины грудной клетки 1-3 степени распространенности поражения в период максимальной выраженности симптомов заболевания. Имели место симптомы «матового стекла», а также единичные фокусы консолидации легочной ткани у отдельных пациентов. В период обследования больные находились на этапе реабилитации, имели нормальную температуру тела, дыхательную недостаточность, проявляющуюся различной степенью снижения сатурации кислорода в тканях при выполнении физической нагрузки в виде ходьбы по коридору, по лестнице. Клинические симптомы поражения верхних дыхательных путей на момент проведения реабилитационной программы были не выражены и наблюдались у отдельных больных. Динамика симптомов заболевания представлена в таблице 6.
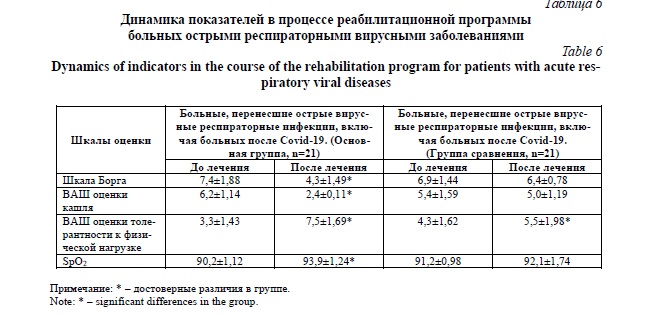
Новый ионный ингаляционный препарат уменьшал выраженность одышки и кашля, восстанавливал толерантность к физической нагрузке. Отмечены случаи прекращения кровохарканья у больных новой коронавирусной инфекцией Covid-19.
Динамика дополнительных параметров здоровья больных, полученных методом удаленного мониторинга с использованием смарт-часов Amazfit U Bip Pro, представлена в таблице 7.
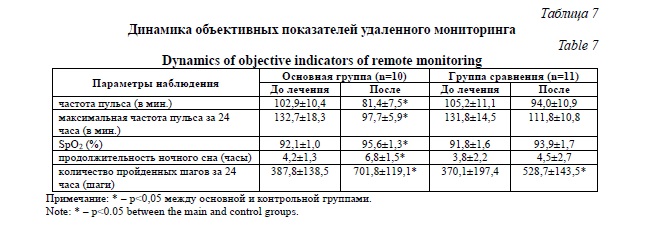
Представленные результаты объективного удаленного мониторинга демонстрируют существенное улучшение параметров здоровья у больных острыми респираторными заболеваниями, получавших препарат Ренериум в ингаляциях на этапе реабилитации.
Динамика рентгенологической картины органов грудной клетки по данным компьютерной томографии прослежена у 16 больных. Отмечается уменьшение объема поражения легочной ткани за счет теней по типу «матового стекла» и ретикулярных изменений. В случаях преобладания интерстициального фиброза, очагов консолидации существенной положительной динамики не выявлено. Наиболее выраженные положительные результаты лечения наблюдались у больных, имевших поражение легочной ткани 1-2 степени по данным КТ-исследования, при неубедительных результатах лечения больных, имевших 3 степень распространенности поражения легких после Covid-19.
Результаты применения шкалы Ликерта в группе больных, получавших ингаляции препарата Ренериум, представлены в таблицах 8 и 8а.
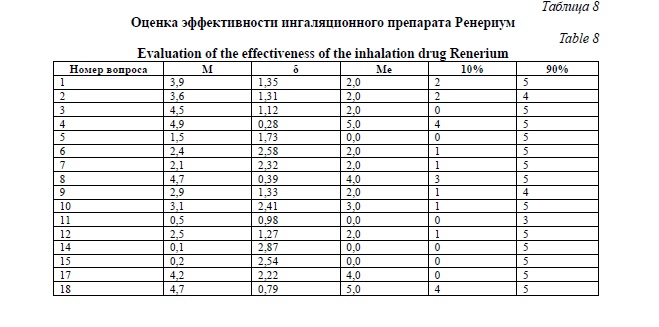
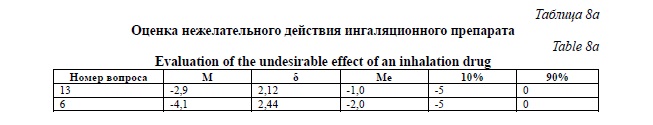
Результаты субъективной оценки эффективности и безопасности ингаляционного препарата Ренериум у больных острыми респираторными вирусными заболеваниями, внебольничной пневмонией, бронхиальной астмой, ХОБЛ и хроническим деформирующим бронхитом показали хорошую переносимость и отсутствие серьезных нежелательных действий, выявлены единичные случаи (3) неприятных ощущений в носоглотке. Клиническая эффективность характеризовалась: уменьшением чувства заложенности в груди, увеличение физической активности, уменьшением объема отделяемой мокроты, снижением интенсивности кашля и одышки, потребности в применении других препаратов для уменьшения симптомов респираторного заболевания, другими положительными сдвигами клинической картины заболевания.
Группа 6. Результаты лечения больных контрольной группы продемонстрировали низкую эффективность 5-и дневного курса ингаляционных глюкокортикоидов в сочетании с ингаляциями 0,9% раствора хлорида натрия при острых воспалительных заболеваниях органов дыхания.
Эффективность и безопасность отдельных компонентов препарата Ренериум
Препарат Ренериум имеет природное происхождение. Основными компонентами, определяющими эффективность препарата, являются ионы Ce3+, Zn2+, Mn7+ и Ag+. Для изучения роли каждого компонента препарата и их взаимодействия были изготовлены опытные партии моно- и двухкомпонентных препаратов, которые приготовлены в виде прозрачных бесцветных растворов по 10 мл во флаконах назального спрея. Клинические наблюдения выполнены на участниках научного коллектива, имеющих клинические симптомы нетяжелого острого респираторного вирусного заболевания с поражением верхних дыхательных путей без идентификации вируса, на основании их добровольного согласия. Препарат вводили в обе половины полости носа по 1-2 дозы в каждый носовой ход многократно на протяжении суток так, чтобы суточная доза приближалась к 10 мл препарата.
Результаты применения моносолевых препаратов в форме назального спрея (препарат CeCl3 (доза ионов Ce3+ 0,5 мкг/л), назальный спрей; ZnSO4 (доза ионов Zn2+ 5 мкг/л, назальный спрей), а также комбинированного препарата, содержащего CeCl3 и ZnSO4, наглядно показали, что клинический эффект пропорционален количеству компонентов солевого раствора, слабо выражен при использовании монокомпонентных препаратов, практически в 2,5-3 раза выше в случае применения комбинации солей церия и цинка. При сравнении с данными, представленными в табл. 4 и 4а с применением комплексного препарата, содержащего ионы церия, цинка, марганца и серебра, отмечается преимущество многокомпонентного препарата. Появление легких необычных ощущений в носу или неприятных ощущений в горле отмечено у единичных пациентов без различий между группами больных.
Обсуждение. Комплекс проведенных доклинических исследований и клинической апробации препарата Ренериум в форме ингаляций с помощью небулайзера и назальной формы убедительно продемонстрировали его противовоспалительные и регенераторные свойства в отношении респираторного эпителия. Клиническая эффективность показала влияние только минерального комплекса, но не отдельных его компонентов. Полученные результаты можно объяснить взаимодействием компонентов минерального комплекса друг с другом, а также с компонентами слизистой оболочки и секрета дыхательных путей. Как известно, ионы церия (III) проявляют восстановительные свойства в присутствие окислителя и в паре Ce3+/Ce4+ [16]. В том числе, способны к элиминации супероксид аниона и других окислителей. Регуляция процессов пероксидации может происходить в области клеточной мембраны, что влияет на состояние рецепторного поля клетки, на уровне митохондрий, где избыток кислородных радикалов подавляет синтез АТФ, и в области ядра клетки, где кислородные радикалы могут быть причиной ошибок редупликации ДНК [17, 18, 19].
Проведенные нами простые химические реакции с участием ионов церия подтверждают восстановительные свойства ионов церия (III). Предложенная гипотеза также соответствует полученным клиническим данным. Тем не менее, «быстрый» клинический эффект ингаляционной формы препарата, возможно, более выраженный, чем при использовании других антиоксидантов. Прямых сравнительных исследований не проводилось, но теоретическое обоснование такого эффекта заключается в случае реализации реакции Белоусова-Жаботинского (автоколебательных окислительно-восстановительных реакций) в системе химических элементов. Первый этап реакции катализируется ионами церия (III) с образованием ионов церия (IV) который затем может взаимодействовать с некоторыми субстратами (в наших исследованиях использован раствор формалина 1%), а также короткоцепочечными жирными кислотами, например, бромалоновой кислотой (CHBr(COOH)2), как это было показано в классических трудах А.М. Жаботинского [20]. Реакция может тормозиться накоплением ионов церия (IV) и требует его элиминации путем взаимодействия с другими субстратами или образованием оксида. Предположение о возникновении автоколебательных химических процессов с участием ионов церия допускает высвобождение электронов, необходимых для работы электрон транспортной системы внутренней митохондриальной мембраны, и накопления АТФ в клетке.
Предложенные минеральные комплексы для лечения респираторных заболеваний отличаются отсутствием острой токсичности и хорошей переносимостью с редкими нежелательными явлениями в виде необычных ощущений в носу или в горле, а также неинтенсивного кашля с небольшим количеством мокроты, которые по частоте возникновения не отличались от применения 0,9% раствора хлорида натрия, и наблюдались в 3-х случаях из 101, включая практически здоровых лиц, получавших исследуемые формы препарата Ренериум.
Заключение. Результаты комплексного, экспериментального и клинического, исследования продемонстрировали выраженные противовоспалительные и регенераторные свойства нового минерального комплекса в составе ионов церия (III), марганца, цинка и серебра, механизм которых обусловлен регуляцией окислительно-восстановительных реакций.
Информация о финансировании
Работа выполнена при поддержке гранта РФФИ_р_НОЦ_Пермский край № 20-415-596008.
Благодарности
Авторы благодарят проф., д.фарм.н. Вдовину Галину Петровну за проведение и описание результатов доклинических исследований с участием лабораторных животных, а также ООО «Ренериум» за изготовление препаратов «Ренериум» и «Ренериум А», предоставление необходимых реактивов и лаборатории для выполнения части химических экспериментальных исследований





















Список литературы