Обзор клинических испытаний перспективных биспецифических кандидатов в препараты клеточной CAR-T терапии
Aннотация
Актуальность: Терапия CAR-T (Chimeric Antigen Receptor T-Cell) клетками показала себя крайне эффективно в лечении онкогематологических заболеваний. В ключевых клинических испытаниях для лечения CD19-положительных опухолей (ZUMA-1, ZUMA-3, JULIET, TRANSCEND) полный ответ составил 58%, 51%, 40%, и 59%, соответственно. Тем не менее, успеху CAR-T терапии препятствуют две основные нерешённые проблемы: острые побочные эффекты и рецидивы онкологических заболеваний. С целью профилактики рецидивов разрабатываются стратегии модификации CAR-конструкта, улучшения экспансии и персистенции CAR-T клеток в организме. В связи с тем, что зачастую рецидивы развиваются на фоне потери экспрессии целевого антигена опухолевыми клетками, использование стратегии нацеливания на два и более опухолевых антигена может значительно снизить частоту рецидивов. Цель исследования:В данном обзоре собраны и проанализированы результаты клинических испытаний биспецифических CAR-T препаратов, проведено сравнение ключевых показателей клинического ответа перспективных CAR-T кандидатов с одобренными FDA препаратами данной терапии. Материалы и методы:Анализ литературы проводился па материалам баз данных PubMed, Scopus, Web of Science, на сайте международного реестра клинических исследований Национального института здоровья США (ClinicalTrials.gov). Результаты:Небольшая выборка клинических исследований с опубликованными результатами не позволила нам найти достоверные отличия по основным показателям CAR-T терапии. Тем не менее, выявлена тенденция к увеличению безрецидивной выживаемости пациентов при использовании биспецифических вариантов CAR-T по сравнению с монопрепаратами. Безрецидивная выживаемость составила 61-90% для CD19/CD20 и 40-85% для CD19/CD22 и 44-61% для моноспецифической анти-CD19 CAR-T терапии. Заключение:Рецидивы онкологического заболевания после CAR-T терапии часто возникают вследствие потери антигена опухолевыми клетками, результаты клинических исследований показывают, что стратегия нацеливания препаратов клеточной терапии на два и более антигена может стать эффективной для снижения риска рецидивов, не вызывая при этом ухудшения показателей иммуно- и нейротоксичности препаратов
Списоксокращений
БРВ – безрецидивная выживаемость;
ВКЛ – В-клеточная лимфома;
ВКР – В-клеточный рецептор;
B-ОЛЛ – острый лимфоцитарный лейкоз В-клеток;
ВЭБ – вирус Эпштейна-Барра;
ДBКЛ – диффузная В-крупноклеточная лимфома;
ИКАНС – синдром нейротоксичности, ассоциированной с иммунными эффекторными клетками (immune effector cell–associated neurotoxicity syndrome, ICANS);
ИЛ – интерлейкин;
ЛХ – лимфома Ходжкина;
МКЛ – мантийноклеточная лимфома;
НК – натуральные киллеры;
НХЛ – неходжскинская лимфома;
ОМЛ – острый миелоидный лейкоз;
СК – стволовые клетки;
МГНЗ – моноклональная гаммапатия неопределенного значения;
ММ – множественная миелома;
ПК – плазматические клетки;
ПМВКЛ – первичная медиастинальная (тимическая) В-крупноклеточная лимфома;
р/р – рецидивирующая / рефрактерная;
СВЦ – синдром высвобождения цитокинов;
ХЛЛ – хронический лимфоцитарный лейкоз;
ХМЛ – хронический миелоидный лейкоз;
ФЛ – фолликулярная лимфома;
ОВ – общая выживаемость;
ОО – общий ответ;
ПО – полный ответ.
Введение. Начиная с конца прошлого века в лечении онкологических заболеваний (ОЗ) стали появляться таргетные препараты, способные уничтожать опухолевые клетки путем нацеливания на специфические молекулярные мишени. Согласно данным Национального Института Онкологии (National Cancer Institute, NCI) одобрение Управления по контролю качества пищевых продуктов и лекарственных средств (Food and Drug Administration, FDA) США для терапии ОЗ получили более 300 препаратов таргетной терапии [1]. Изначально развивавшаяся как подтип таргетной терапии, иммунотерапия стала следующим рубежом в борьбе с опухолями. Моноклональные антитела, направленные на специфические мишени, показали свою эффективность против многих типов ОЗ [2]. Революционной формой иммунотерапии стала CAR-T клеточная терапия, в основе которой лежит использование химерного антигенного рецептора (CAR). Ниша CAR-T терапии на данный момент – пациенты на поздних стадиях ОЗ, резистентные к другим типам лекарственной терапии. CAR-Т клетки показали беспрецедентные результаты в лечении рецидивирующих и рефрактерных (р/р) гематологических злокачественных опухолей.
Гематологические злокачественные новообразования характеризуются неконтролируемым ростом гемопоэтических и лимфоидных клеток и составляют 6,6% всех случаев онкологических заболеваний во всем мире [3]. По состоянию на начало 2024 года одобрение FDA получили шесть CAR-T препаратов, два из которых направлены на лечение B-клеточных лейкозов, четыре - на различные подтипы лимфом, тогда как два препарата разработаны для лечения множественной миеломы (ММ) (Рис. 1).
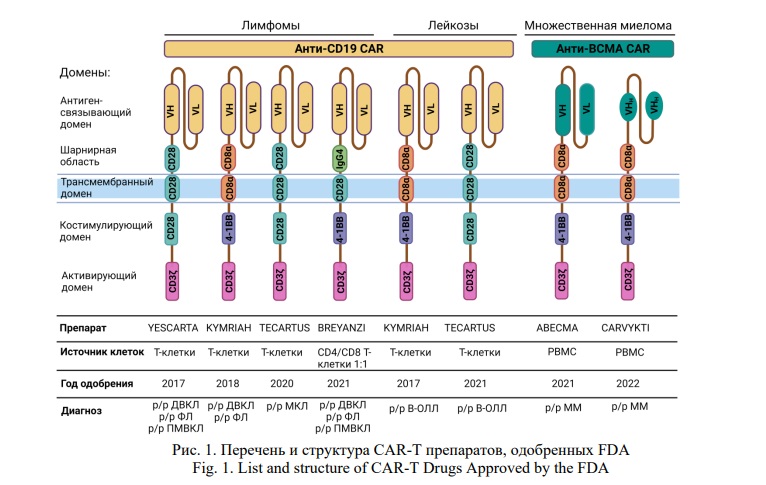
Во всех одобренных FDA препаратах, нацеленных на CD19, антигенсвязывающий домен CAR представлен одним и тем же фрагментом моноклонального антитела мыши FMC63. Препараты Yescarta (аксикабтаген цилолейсел) и Tecartus (брексукабтаген аутолейсел) имеют в своей основе одинаковый CAR, но отличаются технологией производства: в схеме получения Tecartus присутствует дополнительный этап по удалению из продукта лейкафереза злокачественных клеток. В препарате Kymriah (тисагенлеклейсел) CAR имеет другие шарнирные, трансмембранный и костимуляторный домены. Технология производства Breyanzi (лизокабтаген маралейцел) предполагает доставку определенного соотношения CD4+ к CD8+ Т-клеток. Антигенсвязывающий домен CAR в обоих препаратах против ММ нацелен на антиген созревания В-клеток (BCMA): в препарате Abecma (идекаптаген виклейцел) он представлен одноцепочечным вариабельным фрагментом мыши 11D5-3, тогда как в препарате Carvykti (цилтакабтаген аутолейцел) состоит из двух связанных между собой антигенузнающих участков однодоменных антител ламы (VHH). Kymriah, Breyanzi, Abecma и Carvykti имеют лентивирусную систему доставки, тогда как Yescarta и Tecartus используют ретровирусные вектора [4].
Перспективность CAR-T терапии подтверждается высоким клиническим ответом: при лечении неходжкинских лимфом общий ответ (ОО) на терапию Kymriah составил 52%, на Breyanzi – 61%, на Yescarta – 82%, на Tecartus – 85% [5], при лечении ММ общий ответ на терапию Abecma и Carvykti составил 72% [6] и 98% [7], соответственно. Однако все еще остро стоит проблема рецидивов для пациентов, достигших ремиссии после CAR-T терапии. Например, медиана безрецидивной выживаемости у пациентов, получивших Abecma, составляет 8,8 мес [8], у пациентов, получивших Breyanzi – 6,8 мес, у пациентов, получивших Yescarta – 5,9 мес [5].
Накоплено множество доказательств того, что успешность лечения онкогематологических заболеваний зависит от исходных параметров заболевания и от ответа на полученную ранее терапию [9]. Стратификация пациентов по таким параметрам как опухолевая нагрузка, наличие или отсутствие экстрамедуллярного заболевания, полученная ранее терапия позволит предсказать ответ на CAR-T терапию и увеличить продолжительность ремиссии [1]. Помимо учета индивидуальных параметров пациента, важно оптимизировать протоколы пре- и постинфузионного лечения, процесс производства CAR-T клеток и дизайн CAR-конструкта [4]. Для увеличения продолжительности ремиссии исследователи предлагают изменить каркас CAR в направлении оптимизации шарнирного, трансмембранного и костимуляторного доменов, а также нацелить CAR на несколько антигенов. В данном обзоре мы подробно разберем результаты клинических испытаний (КИ) моделей CAR-T, нацеленных на два и более антигена, и сравним клинические ответы моноспецифических и биспецифических CAR-T.
Цель исследования. Собрать и проанализировать результаты КИ биспецифических CAR-T, провести сравнение ключевых показателей клинического ответа с показателями одобренных FDA моноспецифических препаратов для CAR-T-терапии онкогематологических заболеваний.
Материалы и методы исследования. Для изучения механизмов резистентности к CAR-T-терапии и вариантов дизайна биспецифических CAR-T клеток проводился анализ литературы в базах данных PubMed, Scopus, WoS. Также был проведен поиск клинических исследований для оценки эффективности и безопасности биспецифических CAR-T-препаратов на сайте международного реестра клинических исследований Национального института здоровья США https://clinicaltrials.gov/. Статистическую обработку полученных данных проводили методом однофакторного дисперсионного анализа (One Way ANOVA) с помощью встроенного пакета в программе GraphPad Prism 8. Статистически достоверными считались значения при р≤0,05. Настоящая статья не содержит описания выполненных авторами исследований с участием людей или использованием животных в качестве объектов.
Результаты и их обсуждение
Причины возникновения рецидивов
Рецидивы возникают как из исходных CD19+ клеток, так и из CD19- клеток опухоли. CD19- -рецидивы (20-30% пациентов) являются следствием опухолевой гетерогенности и возникают в присутствии прекрасно функционирующих CAR-T клеток [10]. Так, у части пациентов с B-ОЛЛ (и взрослых, и детей) уже на момент постановки диагноза есть клоны клеток, в которых экспрессируются альтернативные формы CD19, например, дефектные по экзону 2, кодирующему эпитоп [11]. У таких пациентов после воздействия CAR-T клеток на CD19+ опухолевые клетки остается живым пул CD19- клеток, который продолжает существовать и в итоге становится доминантным [12].
К рецидивам от CD19+ клеток (70-80% пациентов) могут приводить недостаточная экспансия и персистенция CAR-T клеток, а также различные модификации антигена. Воздействие на антиген может быть следствием: (1) приобретенных мутаций в антигене или альтернативного сплайсинга мРНК антигена, (2) снижения уровня экспрессии антигена, (3) переключения фенотипа клеточной линии, (4) потери или маскировки эпитопа, (5) трогоцитоза (Рис. 2).
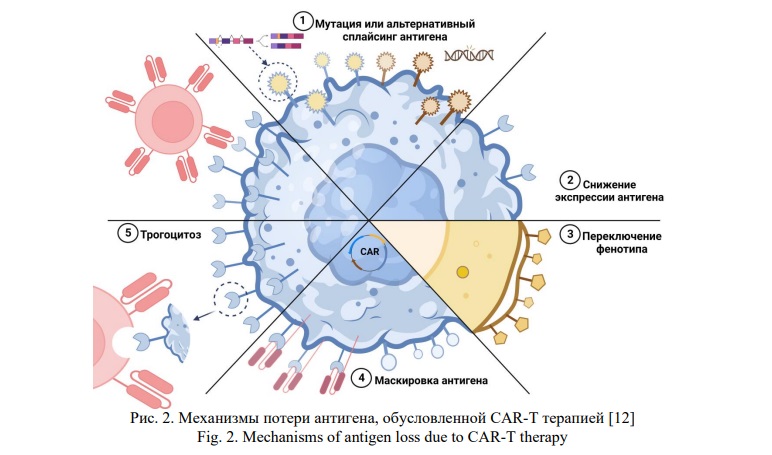
Основной причиной потери антигена CD19 считается альтернативный сплайсинг, в результате иммунного пресса под действием CAR-T терапии клетки с альтернативными формами CD19 становятся доминантными (Рис. 2(1)) [13]. Мутации и альтернативный сплайсинг приводят к изменению исходной мишени, модулируя связывание CAR-T и опухолевой клетки. При этом иногда образуются варианты таргетного белка, которые не позволяют ему выходить на поверхность, но сохраняют при этом часть своих функций [13]. Снижение экспрессии также является частой характеристикой, приобретенной в процессе терапии (Рис. 2(2)). Для приобретения устойчивости к CAR-T терапии опухолевым клеткам не всегда требуется полностью удалить антиген, иногда достаточно снизить его плотность ниже порогового уровня [14].
Также показано, что при длительном воздействии на организм, которое характерного для CAR-T клеток, возможно перепрограммирование В-клеточной линии в миелоидный фенотип, что сопровождается потерей множества лимфоидных маркеров (Рис. 2(3)) [15]. В клиническом исследовании по применению анти-CD19 CAR-T терапии для лечения В-ОЛЛ у 7 пациентов, имеющих транслокацию гена MLL, была достигнута полная ремиссия у всех пациентов. Однако, в течение 1 месяца после инфузии у 2 из 7 пациентов был диагностирован ОМЛ, клонально связанный с клетками В-ОЛЛ и отрицательный на CD19 [16]. Также описан случай переключения линий после лечения хронического лимфоцитарного лейкоза (ХЛЛ) с трансформацией по Рихтеру с помощью CAR-T клеток к CD19: спустя 6 месяцев у пациента возникла плазмобластная лимфома без остаточных маркеров В-лимфоидной дифференцировки [17]. Авторы указывают на то, что селективно воздействуя на CD19, можно изменить дифференцировку лимфоидной ткани или способствовать клональной экспансии опухолевых клеток со статусом дифференцировки, отличным от основного пула опухолевых клеток.
В статье Ruella etal. впервые был описан случай рецидива лейкоза после лечения CD19 CAR-T клетками вследствие экспрессии CAR опухолевой клеткой [18]. Последовательность CAR была непреднамеренно введена в опухолевую В-клетку во время производства Т-клеток, и его продукт связался с эпитопом CD19 на поверхности опухолевой клеток, маскируя его от распознавания и придавая устойчивость к CD19 CAR-T клеткам (Рис. 2(4)).
Интересным вариантом взаимодействия CAR-T и опухолевых клеток является трогоцитоз, при котором CAR-T клетки, контактируя с опухолевыми клетками, встраивают часть мембраны этих клеток с целевым антигеном CD19 на свою поверхность (Рис 2(5)). В результате этого снижается плотность антигена на опухолевых клетках, что приводит к неэффективному лизису опухоли. Кроме того, такие CD19+ CAR-T клетки сами становятся мишенями CAR-T клеток, на поверхности которых нет этого антигена [19].
Применение монотаргетной CAR-T терапии приводит к потере антигена вне зависимости от изначальной мишени терапии. Так, у пациентов с рецидивами после анти-CD19 CAR-T препаратов, возникшими из-за наличия CD19- клонов опухолевых клеток, в процессе применения анти-CD22 CAR-T были выявлены CD22- клетки лейкоза [20]. В противовес этому, одновременное воздействие на несколько антигенов может не только снизить риск возникновения рецидива в результате потери антигена, но и повысить продолжительность ответа и эффективность терапии [20]. Воздействовать на два и более антигена одновременно можно разными способами. Например, комбинируя CAR-T терапию с моноклональными антителами к другой мишени. Так, в КИ NCT04002401 исследуется комбинация Yescarta и ритуксимаба, моноклонального антитела к CD20 [21]. Биспецифические антитела и биспецифические CAR-T представляют собой другой вариант воздействия на две мишени в одном цикле терапии.
Варианты дизайна биспецифических CAR-T клеток
Принцип, лежащий в основе работы биспецифических CAR-T, заключается в том, что при снижении или потере одного антигена на поверхности опухолевых клеток, CAR-T клетки сохраняют способность узнавать и уничтожать опухолевые клетки за счет связывания со вторым антигеном. А при наличии на опухолевых клетках двух и более пан-В-клеточных маркеров (например, CD19 и CD20/CD22/CD123), значительно повышается эффективность CAR-Т терапии за счет воздействия на два антигена.
Есть несколько способов реализации биспецифических CAR-T (Рис. 3):
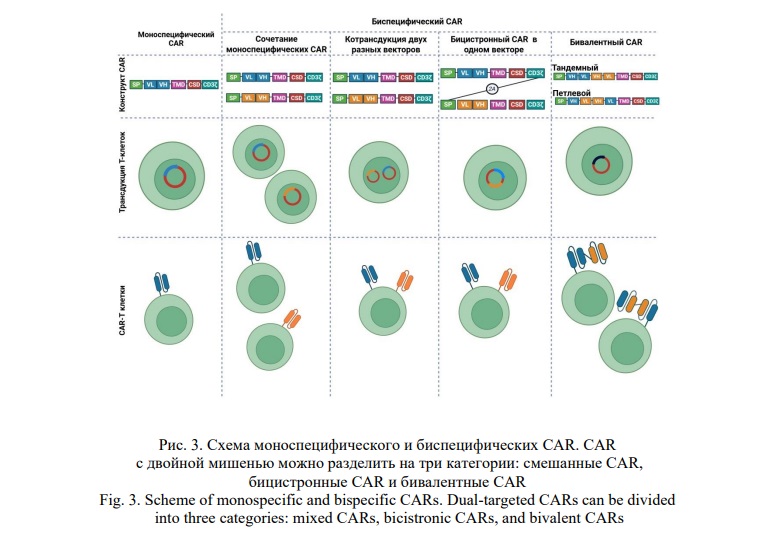
1) коктейль/последовательное использование двух продуктов моноспецифических CAR-Т клеток, индивидуально трансдуцированных двумя разными векторами;
2) биспецифические CAR-T клетки, полученные путем совместной трансдукции двух векторов, каждый из которых кодирует один индивидуальный CAR или путем трансдукции бицистронного вектора для введения двух отдельных CAR, каждый из которых имеет свой антигенсвязывающий домен;
3) биспецифические CAR-Т клетки, экспрессирующие один двухвалентный CAR с двумя антигенсвязывающими доменами. Бивалентный CAR можно разделить на две разные структуры, поместив тяжелую (VH) и легкую (VL) цепь антигенсвязывающего домена scFv в разном порядке, т.е. с VL-VH одного scFv, непосредственно связанного с VL-VH другого scFv, определенного как бивалентный тандемный CAR или с VL-VH одного scFv, разделенных VL-VH другого scFv, определяемого как двухвалентный петлевой CAR.
Наиболее оптимальный вариант получения биспецифических CAR еще предстоит определить, в данный момент разные варианты исследуются в КИ. При этом важно помнить, что при выборе антигенов для биспецифических CAR-T необходимо учитывать синергизм и комплементарность двух мишеней.
Мишени для CAR-T при В-клеточных и плазмоклеточных злокачественных заболеваниях в КИ
Первые CAR-конструкты, дошедшие до стадии одобрения FDA, имеют антиген-распознающую область антитела к CD19. Данный мембранный белок, принадлежащий к суперсемейству иммуноглобулинов, участвует в процессах дифференцировки и созревания В-клеток, его экспрессия теряется на стадии созревания до плазматических клеток (ПК). СD19 можно встретить на поверхности большинства В-клеточных злокачественных опухолей (включая ХЛЛ, B-ОЛЛ и многих НХЛ), что делает его хорошей мишенью для нацеливания CAR-T.
В таблице 1 представлены мишени, для которых инициированы КИ.
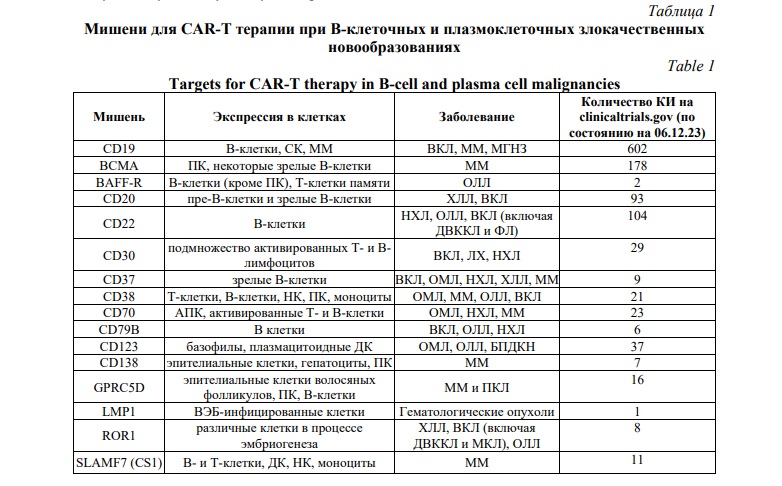
Мишени, указанные в таблице 1, рассматриваются как для создания моноспецифических, так и для разработки биспецифических вариантов CAR-T. Согласно данным международного реестра КИ Национального института здоровья США (clinicaltrials.gov) максимальное количество КИ зарегистрировано для комбинаций CD19/CD22, CD19/CD20 и CD19/BCMA.
CD22 (Siglec-2) представляет собой трансмембранный белок, который экспрессируется на ранних стадиях онтогенеза В-клеток и сохраняется до дифференцировки в ПК; на поверхности злокачественных B-клеток, особенно в маргинальной зоне, мантийных и фолликулярных B-клетках. Препараты на основе антител, нацеленных на CD22, такие как инотузумаб озогамицин и пинатузумаб ведотин, оказались успешными в лечении B-НХЛ и B-ОЛЛ.
Биспецифические CAR против CD19/CD22 при В-клеточных злокачественных новообразованиях исследуют для лечения ОЛЛ, НХЛ, ДBКЛ, МКЛ, ФЛ. Для данных мишеней на конец 2023 года зарегистрировано (clinicaltrials.gov) всего 55 КИ в 1 фазе и 37 КИ во 2 фазе. Результаты некоторых КИ, проведенных в Китае и США, представлены в таблице 2.
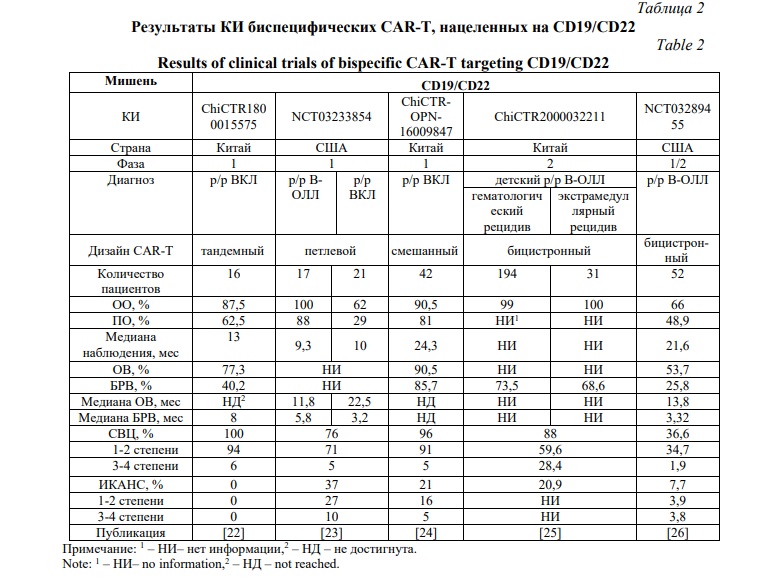
Исследование под идентификационным номером ChiCTR2000032211 – наиболее крупное из выявленных нами. В нем приняли участие 225 детей с р/р ОЛЛ: 194 – с гематологическим рецидивом и 31 – экстрамедуллярным рецидивом. ОО составил 99 и 100%, БРВ – 73,5 и 68,6 %, соответственно. У 28,4 % пациентов наблюдался СВЦ 3 степени и выше [25].
В других, описанных в таблице 2, КИ ОО варьировал от 62 до 100%, полный ответ (ПО) наблюдался у 29-88% пациентов [22-26]. Процент общей выживаемости варьировал от 53,7 до 90,5. БРВ – от 25,8 до 85,7%. СВЦ тяжелой степени наблюдался у 5-28% пациентов. Наиболее выраженная нейротоксичность наблюдалась в исследовании NCT03233854 и составила 37% [23]. В исследовании ChiCTR-OPN-16009847 наблюдалась лимфоцитопения четвертой степени у всех пациентов [24].
CD20 уже несколько десятилетий является мишенью для моноклональных антител и считается неотъемлемой частью лечения зрелых В-клеточных злокачественных опухолей [27]. Он представляет собой негликозилированный трансмембранный фосфопротеин массой 33-37 кДа, который экспрессируется только В-клетками [28]. Как и CD22, CD20 экспрессируется в большинстве В-клеточных лейкозов и лимфом, что делает его привлекательной мишенью для клеточной иммунотерапии [27]. Преимуществом CD20 как мишени для CAR-T является низкая частота потери этого антигена, несмотря на повторные циклы терапии, нацеленной на CD20 [29].
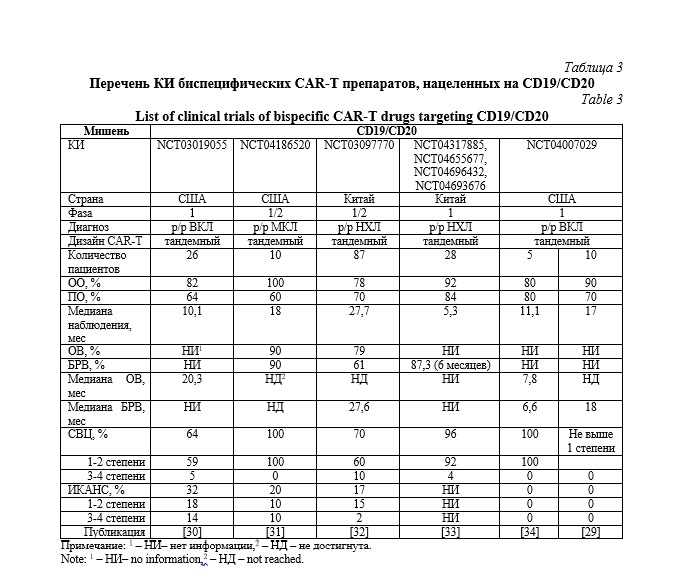
По данным Национального института здоровья США с комбинацией антигенов-мишеней CD19/CD20 на конец 2023 года было инициировано 39 КИ на 1 фазе и 21 КИ на 2 фазе. В таблице 3 собраны результаты шести исследований по CD19/CD20 CAR-T терапии. Наиболее крупное из них – NCT03097770 [32]. В нем приняло участие 87 пациентов. ОО составил 78%, ПО наблюдался у 70% пациентов. Общая выживаемость наблюдалась у 79% и составила 1 год, тогда как БРВ – у 61% и составила 1 год. У 10% испытуемых наблюдался СВЦ высокой степени, а у 17% – нейротоксичность 2 и более степени. Лейкопения наблюдалась у 81%, а тромбоцитопения – у 56% пациентов.
Согласно исследованиям, описанным в таблице 3, ОО на анти CD19/CD20 CAR-T терапию варьировал в среднем от 78 до 90%, полный ответ от 60 до 84% [30-34]. Медиана общей выживаемости в одном исследовании не достигла 8 месяцев, а в другом исследовании составила 20,3 месяцев. БРВ варьировала от 6,6 до 27,6 месяцев. Показатели СВЦ ≥3 степени были относительно низкими во всех исследованиях и не превышали 10%. Нейротоксичность ≥3 степени была максимальной в исследовании NCT03019055 и наблюдалась у 14% пациентов [30].
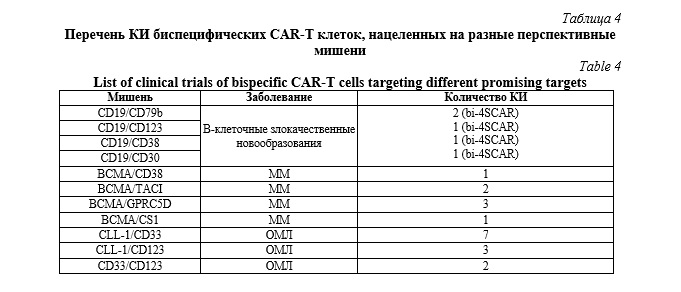
В таблице 4 представлено несколько вариантов других перспективных биспецифических CAR-T. Среди них результаты КИ доступны для мишеней BCMA/CD38, BCMA/CS1 и BCMA/TACI.
Для пациентов с ММ наиболее распространенной мишенью является антиген созревания В-клеток (BCMA, CD269, TNFRSF17). Экспрессия BCMA специфична для ПК и не была обнаружена в других тканях человека так же, как и на поверхности первичных CD34+ гемопоэтических клеток. BCMA присутствует практически на всех клетках ММ [35].
BCMA является членом суперсемейства рецепторов фактора некроза опухоли. Его связывание и стимуляция способствует росту и пролиферации ПК в костном мозге, его сверхэкспрессия имеет прогностическое значение при миеломе [36]. BCMA может находиться как в связанном с мембраной состоянии, так и в растворенной форме. Сывороточный уровень BCMA является диагностическим маркером при ММ [37]. Было показано снижение уровня растворимого BCMA в сыворотке крови после курса анти-BCMA CAR-T терапии и, наоборот, увеличение концентрации при прогрессировании заболевания.
Препараты CAR-T против BCMA отличаются высокой эффективностью. Тем не менее, проблема терапевтической устойчивости, которую связывают с гетерогенностью опухоли и потерей антигена, диктует необходимость разработки модификаций CAR, нацеленных на BCMA.
Новым подходом лечения ММ является использование анти-CD19 CAR-T клеток в виде монотерапии или в комбинации с анти-BCMA CAR-T клетками. В 2015 году пациенту с ММ после аутологичной трансплантации СК ввели CAR-T, нацеленные на CD19, что привело к полному ответу, отсутствию признаков прогрессирования и измеримого моноклонального белка в сыворотке или моче при наблюдении в течение 12 месяцев [38]. Были опубликованы результаты КИ NCT02135406, согласно которым анти-CD19 CAR-T терапия эффективна в лечении пациентов с р/р ММ, несмотря на отсутствие экспрессии CD19 в 99,95% неопластических ПК [39]. Авторы предположили, что данная CAR-T терапия воздействует на минорные субпопуляции клеток миеломы с фенотипом опухолевых стволовых клеток, которые экспрессируют CD19 [8]. Альтернативным объяснением эффективности такой терапии может быть то, что анти-CD19 CAR-T клетки воздействуют на незлокачественные CD19-положительные В-клетки, а они сами по себе могут воздействовать на противоопухолевый иммунитет, секретируя ростовые факторы [40]. Дальнейшие попытки использовать анти-CD19 CAR-T клетки для лечения ММ привели к противоречивым результатам. Например, в КИ NCT02135406 только у 2 из 10 испытуемых наблюдался положительный клинический ответ от применения анти-CD19 CAR-T терапии [41]. Это может быть следствием вынужденного использования более низкой дозы CAR-T, либо отсутствием CD19+ популяции у отдельных пациентов. Авторы указывают на то, что, вероятно, данный поверхностный иммунофенотип не является надежной прогностической характеристикой, поскольку варьирует от пациента к пациенту и зависит от истории самого заболевания.
Противоречивые данные были получены и в ходе исследования, описанного в статье Garfall et al., где была оценена безопасность и целесообразность комбинации анти-BCMA и анти-CD19 CAR-T, а также возможность использования CAR-T в более ранних линиях терапии (Табл. 5) [42]. Фрагмент антитела к CD19 в данном КИ был представлен гуманизированной формой - huCART-19. Ответ на CAR-T терапию сравнивали у пациентов после нескольких линий терапии (фаза А) и у пациентов с высоким риском после ответа на начальную терапию (фаза В). Пациенты фазы А получали анти-BCMA CAR-T совместно с анти-CD19 CAR-T, а пациенты фазы B получали либо только анти- BCMA CAR-T, либо совместно анти- BCMA и анти-CD19 CAR-T (Табл. 5). СВЦ был низкой степени тяжести, однако было установлено, что использование CAR-T клеток в ранних линиях терапии миеломы может дать лишь небольшие, а не трансформационные улучшения по сравнению с их применением в более поздних линиях терапии. Кроме того, авторы не обнаружили клинической эффекта от добавления huCART19 к анти-BCMA CAR-T, что возможно связано с тем, что CD19 не является значимой мишенью для большинства пациентов.
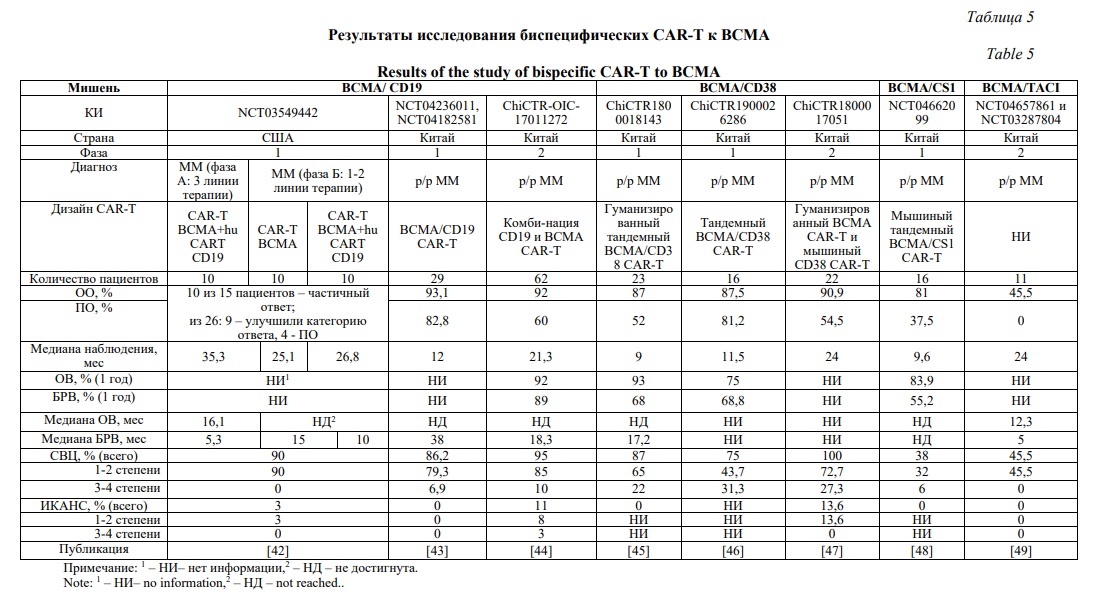
В публикации Du etal. представлены результаты по применению биспецифических CAR-T клеток, нацеленных на BCMA и CD19 [43]. ОО составил 93,1% (27/29), ПО – 82,8%, медиана БРВ – 38 месяцев (95% ДИ 11,8-НД). СВЦ наблюдался у 86,2% пациентов, у 6,9% в тяжелой степени. Нейротоксичность не была выявлена.
В работе Wang etal. была оценена эффективность и безопасность комбинации анти-BCMA и анти-CD19 CAR-T клеток среди пациентов с р/р ММ [44]. ОО составил 92% (57/62), а ПО наблюдался у 37 пациентов (60%). Медиана БРВ составила 18,3 месяца (95% ДИ от 9,9 до 26,7), а медиана общей выживаемости не была достигнута. СВЦ был выявлен у 95% пациентов, из них 10% пациентов были диагностированы с СВЦ 3 степени или выше. Нейротоксичность была выявлена у семи пациентов (11%), в том числе ≥3 степени тяжести у 3%.
CD38 относится к подтвержденным опухолевых антигенам при ММ. Также в качестве мишени его используют для лечения Т-клеточного ОЛЛ и ОМЛ (NCT03067571 и NCT03384654) [33]. Эффективны моноклональные антитела к CD38 (например, даратумумаб, изатуксимаб).
Анализ результатов тестирования CAR-T клеток, нацеленных на BCMA и CD38, представлен в таблице 5 на основании данных трех КИ [45-47]. Общая выживаемость варьировала от 87 от 90% в трех исследованиях. ПО наблюдался более чем у 52% испытуемых. ОВ для 1 года составляла 75-93%, БРВ – 55-68%. СВЦ тяжелой степени наблюдался у 22-30% испытуемых, получавших BCMA/CD38 CAR-T клетки. Нейротоксичность была зафиксирована в одном исследовании, характеризовалась легкой степенью и составила 13%. Цитопения наблюдалась у большинства испытуемых.
Однако следует отметить, что экспрессия CD38, как правило, наблюдается в небольшом количестве на клетках миеломы и снижается при прогрессировании заболевания [36]; таким образом, ожидаемо появление резистентности к анти-CD38 CAR-T. Кроме того, существует вероятность развития токсичности on-target/off-tumor, поскольку CD38 также экспрессируется на активированных Т-клетках, НК-клетках и нормальных клетках предстательной железы, нейронов и мышц.
Интерес к антигену CS1 вызван тем, что он часто гиперэкспрессируется в клетках миеломы, его используют для создания CAR-T клеток как в моноформе, так и для получения биспецифических CAR-T. В статье Li et al. приведены результаты тестирования анти-BCMA/CS1 CAR-T (NCT04662099) [48]. ОО составил 81%, строгий полный ответ – 37,5% при медиане наблюдения 9 месяцев медианы общей выживаемости и безрецидивной выживаемости не были достигнуты, у одного пациента был зафиксирован СВЦ высокой степени тяжести.
AUTO2 - CAR Т-клетка, предназначенная для одновременного воздействия на BCMA и TACI с помощью новой CAR-конструкции, использующей усеченную форму лиганда, индуцирующего пролиферацию (APRIL), в качестве домена, нацеленного на опухоль. В КИ 1 фазы были включены пациенты с р/р ММ в рамках эскалации дозы. В общей сложности 11 пациентов достигли минимального срока наблюдения и были оценены по конечным точкам безопасности. У пяти пациентов наблюдался СВЦ первой степени, а случаев нейротоксичности не было. Среди пациентов, получивших дозу ≥225×106 клеток, ОО составил 45,5 % в этой ранней фазе исследования [49].
Триспецифические CAR также вошли на стадию КИ. В работе Fousek et al. представлено сравнение двух моделей триспецифических CAR: первая модель (TriCAR) представляет собой три моновалентных CAR второго поколения, которые нацелены на антигены CD19, CD20 и CD22, вторая модель – два CAR, первый из которых нацелен на CD19, а второй (SideCAR) представляет собой бивалентный CAR, нацеленный на CD20 и CD22 [50]. В данном исследовании было показано, что триспецифические CAR являются более эффективными вариантами, чем моновалентный CAR в лечении CD19-негативных опухолевых клеток при ОЛЛ.
Сравнительный анализ эффективности биспецифических модификаций CAR-T
Для оценки эффективности биспецифических CAR-T нами был проведен статистический анализ основных показателей представленных КИ, включая ОО, ПО, БРВ, СВЦ в целом и 3-4 степени отдельно для модификаций CAR-T, направленных на элиминацию CD19+ клеток (данные не представлены). В ходе анализа было выбрано два варианта биспецифических CAR-T (CD19/CD20, CD19/CD22), которые в дальнейшем сравнивали с одобренными FDA анти-CD19 CAR-T препаратами (Рис. 4).
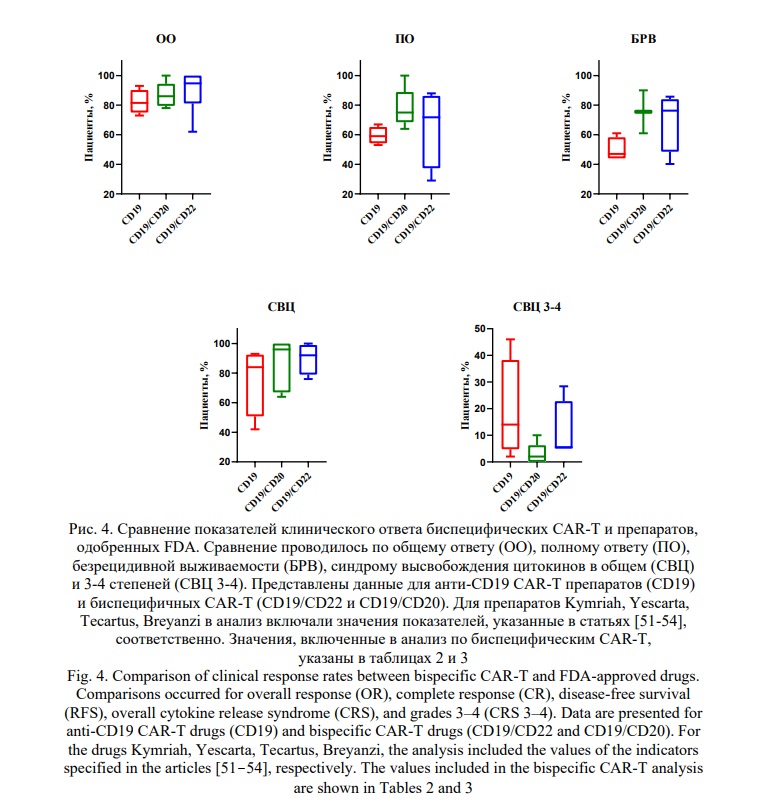
При анализе КИ мы не смогли обнаружить достоверные отличия по основным показателям CAR-T терапии. При этом стоит отметить, что БРВ пациентов, получивших биспецифические варианты CAR-T, составила 61-90% для CD19/CD20 и 40-85% для CD19/CD22 по сравнению с 44-61% для моноспецифической анти-CD19 CAR-T терапии.
Заключение. Несмотря на высокие показатели ремиссии, достигнутые при использовании CAR-Т клеток для терапии гематологических злокачественных новообразований, у значительной доли пациентов возникает рецидив заболевания. Результаты КИ показали, что снижение экспрессии антигена-мишени и ограниченная персистенция CAR-Т клеток являются основными причинами развития рецидива заболевания. Риск развития иммуно- и нейротоксичности после введения CAR-T клеток также является препятствием, которое необходимо преодолеть для улучшения показателей терапии.
Описанные задачи привели к созданию нескольких десятков стратегий оптимизации CAR-T препаратов. В данном обзоре мы рассмотрели один из вариантов модификации CAR-T терапии В-клеточных и плазмоклеточных злокачественных новообразований – биспецифические CAR-T. Мы собрали имеющиеся данные о результатах КИ биспецифических CAR-T, одной из мишенью которых является CD19 или BCMA. Для таких модификаций, как CD19/CD20 и CD19/CD22 была оценена их эффективность по сравнению с одобренными FDA препаратами. К сожалению, нам не удалось обнаружить достоверных отличий между группами, что связано с небольшим количеством КИ для каждой группы, однако БРВ имеет тенденцию на увеличение в группах с биспецифическими CAR-T по сравнению с монопрепаратами к CD19. А значит стратегия использования биспецифических CAR-T может стать эффективной для снижения риска рецидивов, связанных с потерей антигена. Данный подход может быть использован для расширения списка целевых опухолей и увеличения общего количества пациентов, направленных на СAR-T терапию.
Информация о финансировании
Работа выполнена за счет средств субсидии, выделенной Казанскому федеральному университету для выполнения государственного задания в сфере научной деятельности (Проект № FZSM-2022-0016).
Благодарности
Работа выполнена в рамках Программы стратегического академического лидерства (ПРИОРИТЕТ-2030) Казанского (Приволжского) федерального университета





















Список литературы
1. NIC [Электронный ресурс]. List of Targeted Therapy Drugs Approved for Specific Types of Cancer [дата обращения: 25.12.2023]. URL: https://www.cancer.gov/about-cancer/treatment/types/targeted-therapies/approved-drug-list
2. Hou J, He Z, Liu T, et al. Evolution of molecular targeted cancer therapy: mechanisms of drug resistance and novel opportunities identified by CRISPR-Cas9 screening. Frontiers in Oncology. 2022;12:755053. DOI: https://doi.org/10.3389/fonc.2022.755053
3. Sung H, Ferlay J, Siegel RL, et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. Ca-A Cancer Journal for Clinicians. 2021;71(3):209-249. DOI: https://doi.org/10.3322/caac.21660
4. Cappell KM, Kochenderfer JN. Long-term outcomes following CAR T cell therapy: What we know so far. Nature Reviews Clinical Oncology. 2023;20:359-371. DOI: https://doi.org/10.1038/s41571-023-00754-1
5. Crees ZD, Ghobadi A. Cellular therapy updates in B-cell lymphoma: the state of the CAR-T. Cancers. 2021;13(20):5181. DOI: https://doi.org/10.3390/cancers13205181
6. ABECMA [Электронный ресурс]. Proven CAR T Cell Therapy Power in the Patients You’re Likely to See [дата обращения: 25.12.2023]. URL: https://www.abecmahcp.com/efficacy
7. CARVYCTI [Электронный ресурс]. EFFICACY OUTCOMES FROM THE PIVOTAL CARTITUDE-1 STUDY [дата обращения: 25.12.2023]. URL: https://www.carvyktihcp.com/efficacy
8. Garfall A, Cohen A, Susanibar-Adaniya S, et al. CAR T cells targeting BCMA and CD19 for newly diagnosed and relapsed multiple myeloma patients responding to current therapy [Электронный ресурс]. Blood Cancer Discovery. 2022 [дата обращения: 25.12.2023]. URL: https://oak.novartis.com/id/eprint/47478
9. Jain A, Jain A, Malhotra P. Re-defining prognosis of hematological malignancies by dynamic response assessment methods: lessons learnt in chronic myeloid leukemia, Hodgkin lymphoma, diffuse large b cell lymphoma and multiple myeloma. Indian Journal of Hematology and Blood Transfusion. 2020;36:447-457. DOI: https://doi.org/10.1007/s12288-019-01213-7
10. Aparicio-Pérez C, Carmona M, Benabdellah K, et al. Failure of ALL recognition by CAR T cells: a review of CD 19-negative relapses after anti-CD 19 CAR-T treatment in B-ALL. Frontiers in Immunology. 2023;14:1165870. DOI: https://doi.org/10.3389/fimmu.2023.1165870
11. Fischer J, Paret C, El Malki K, et al. CD19 isoforms enabling resistance to CART-19 immunotherapy are expressed in B-ALL patients at initial diagnosis. Journal of Immunotherapy. 2017;40(5):187-195. DOI: https://doi.org/10.1097/CJI.0000000000000169
12. Xie D, Jin X, Sun R, et al. Relapse mechanism and treatment strategy after chimeric antigen receptor T-cell therapy in treating B-cell hematological malignancies. Technology in Cancer Research and Treatment. 2022;21:15330338221118413. DOI: https://doi.org/10.1177/15330338221118413
13. Sotillo E, Barrett DM, Black KL, et al. Convergence of acquired mutations and alternative splicing of CD19 enables resistance to CART-19 immunotherapy. Cancer Discovery. 2015;5(12):1282-1295. DOI: https://doi.org/10.1158/2159-8290.CD-15-1020
14. Fry TJ, Shah NN, Orentas RJ, et al. CD22-targeted CAR T cells induce remission in B-ALL that is naive or resistant to CD19-targeted CAR immunotherapy. Nature Medicine. 2018;24(1):20-28. DOI: https://doi.org/10.1038/nm.4441
15. Jacoby E, Nguyen SM, Fountaine TJ, et al. CD19 CAR immune pressure induces B-precursor acute lymphoblastic leukaemia lineage switch exposing inherent leukaemic plasticity. Nature Communications. 2016;7(1):12320. DOI: https://doi.org/10.1038/ncomms12320
16. Gardner R, Wu D, Cherian S, et al. Acquisition of a CD19-negative myeloid phenotype allows immune escape of MLL-rearranged B-ALL from CD19 CAR-T-cell therapy. Blood. 2016;127(20):2406-2410. DOI: https://doi.org/10.1182/blood-2015-08-665547
17. Evans A, Burack R, Rothberg PG, et al. Evolution to Plasmablastic Lymphoma (PBL) after CAR-T Cell Therapy in a Case of SLL/CLL with Richter’s Transformation. Blood. 2014;124(21):5660-5660. DOI: https://doi.org/10.1182/blood.V124.21.5660.5660
18. Ruella M, Xu J, Barrett DM, et al. Induction of resistance to chimeric antigen receptor T cell therapy by transduction of a single leukemic B cell. Nature Medicine. 2018;24(10):1499-1503. DOI: https://doi.org/10.1038/s41591-018-0201-9
19. Hamieh M, Dobrin A, Cabriolu A, et al. CAR T cell trogocytosis and cooperative killing regulate tumour antigen escape. Nature. 2019;568(7750):112-116. DOI: https://doi.org/10.1038/s41586-019-1054-1
20. Cronk RJ, Zurko J, Shah NN. Bispecific chimeric antigen receptor T cell therapy for B cell malignancies and multiple myeloma. Cancers. 2020;12(9):2523. DOI: https://doi.org/10.3390/cancers12092523
21. Strati P, Leslie LA, Shiraz P, et al. Axicabtagene ciloleucel (axi-cel) in combination with rituximab (Rtx) for the treatment (Tx) of refractory large B-cell lymphoma (R-LBCL): Outcomes of the phase 2 ZUMA-14 study. Journal of Clinical Oncology. 2022;40(16_suppl):7567-7567. DOI: https://doi.org/10.1200/JCO.2022.40.16_suppl.7567
22. Wei J, Zhang Y, Zhao H, et al. CD19/CD22 Dual-Targeted CAR T-cell Therapy for Relapsed/Refractory Aggressive B-cell Lymphoma: A Safety and Efficacy Study. Cancer Immunol Res. 2021; 9 (9): 1061–1070. DOI: https://doi.org/10.1158/2326-6066.CIR-20-0675
23. Spiegel JY, Patel S, Muffly L, et al. CAR T cells with dual targeting of CD19 and CD22 in adult patients with recurrent or refractory B cell malignancies: a phase 1 trial. Nature Medicine. 2021;27(8):1419-1431. DOI: https://doi.org/10.1038/s41591-021-01436-0
24. Cao Y, Xiao Y, Wang N, et al. CD19/CD22 Chimeric Antigen Receptor T Cell Cocktail Therapy following Autologous Transplantation in Patients with Relapsed/Refractory Aggressive B Cell Lymphomas. Transplantation and Cellular Therapy. 2021;27(11):910.e1-910.e11. DOI: https://doi.org/10.1016/j.jtct.2021.08.012
25. Wang T, Tang Y, Cai J, et al. Coadministration of CD19- and CD22-Directed Chimeric Antigen Receptor T-Cell Therapy in Childhood B-Cell Acute Lymphoblastic Leukemia: A Single-Arm, Multicenter, Phase II Trial. Journal of Clinical Oncology. 2023;41(9):1670-1683. DOI: https://doi.org/10.1200/JCO.22.01214
26. Roddie C, Lekakis LJ, Marzolini MA, et al. Dual targeting of CD19 and CD22 with bicistronic CAR-T cells in patients with relapsed/refractory large B-cell lymphoma. Blood. 2023;141(20):2470-2482. DOI: https://doi.org/10.1182/blood.2022018598
27. Marshall MJE, Stopforth RJ, Cragg MS. Therapeutic Antibodies: What Have We Learnt from Targeting CD20 and Where Are We Going? Frontiers in Immunology. 2017;8:1245. DOI: https://doi.org/10.3389/fimmu.2017.01245
28. Le Jeune C, Thomas X. Antibody-based therapies in B-cell lineage acute lymphoblastic leukaemia. European Journal of Haematology. 2015;94(2):99-108. DOI: https://doi.org/10.1111/ejh.12408
29. Larson SM, Walthers CM, Ji B, et al. CD19/CD20 bispecific chimeric antigen receptor (CAR) in naïve/memory T cells for the treatment of relapsed or refractory non-Hodgkin lymphoma. Cancer Discovery. 2023;13(3):580-597. DOI: https://doi.org/10.1158/2159-8290.CD-22-0964
30. Shah NN, Johnson BD, Schneider D, et al. Bispecific anti-CD20, anti-CD19 CAR T cells for relapsed B cell malignancies: a phase 1 dose escalation and expansion trial. Nature Medicine. 2020;26(10):1569-1575. DOI: https://doi.org/10.1038/s41591-020-1081-3
31. Shah NN, Furqan F, Szabo A, et al. Results from a Phase 1/2 Study of Tandem, Bispecific Anti-CD20/Anti-CD19 (LV20. 19) CAR T-Cells for Mantle Cell Lymphoma. Blood. 2022;140(Supplement 1):9318-9319. DOI: https://doi.org/10.1182/blood-2022-158695
32. Zhang Y, Wang Y, Liu Y, et al. Long-term activity of tandem CD19/CD20 CAR therapy in refractory/relapsed B-cell lymphoma: a single-arm, phase 1–2 trial. Leukemia. 2022;36(1):189-196. DOI: https://doi.org/10.1038/s41375-021-01345-8
33. Liang A, Zhou L, Li P, et al. Safety and efficacy of a novel anti-CD20/CD19 bi-specific CAR T-cell therapy (C-CAR039) in relapsed or refractory (r/r) B-cell non-Hodgkin lymphoma (B-NHL). Journal of Clinical Oncology. 2021;39(15_suppl):2507-2507. DOI: https://doi.org/10.1200/JCO.2021.39.15_suppl.2507
34. Ghafouri SN, Walthers C, Roshandell M, et al. Abstract CT007: CD19/CD20 bispecific chimeric antigen receptor (CAR) in naive/memory T-cells for the treatment of relapsed or refractory B-cell lymphomas. Cancer Research. 2021;81(13_Supplement):CT007. DOI: https://doi.org/10.1158/1538-7445.AM2021-CT007
35. Carpenter RO, Evbuomwan MO, Pittaluga S, et al. B-cell maturation antigen is a promising target for adoptive T-cell therapy of multiple myeloma. Clinical Cancer Research. 2013;19(8):2048-2060. DOI: https://doi.org/10.1158/1078-0432.CCR-12-2422
36. Teoh PJ, Chng WJ. CAR T-cell therapy in multiple myeloma: more room for improvement. Blood Cancer Journal. 2021;11(4):84. DOI: https://doi.org/10.1038/s41408-021-00469-5
37. Sanchez E, Li M, Kitto A, et al. Serum B‐cell maturation antigen is elevated in multiple myeloma and correlates with disease status and survival. British Journal of Haematology. 2012;158(6):727-738. DOI: https://doi.org/10.1111/j.1365-2141.2012.09241.x
38. Garfall AL, Maus MV, Hwang WT, et al. Chimeric antigen receptor T cells against CD19 for multiple myeloma. New England Journal of Medicine. 2015;373(11):1040-1047. DOI: https://doi.org/10.1056/NEJMoa1504542
39. Garfall AL, Maus MV, Lacey SF, et al. Safety and efficacy of anti-CD19 chimeric antigen receptor (CAR)-modified autologous T cells (CTL019) in advanced multiple myeloma. Journal of Clinical Oncology. 2015;33:8517-8517. DOI: https://doi.org/10.1200/jco.2015.33.15_suppl.8517
40. Shimabukuro-Vornhagen A, Schloesser HA, von Bergwelt-Baildon MS. Chimeric Antigen Receptor T Cells in Myeloma. New England Journal of Medicine. 2016;374(2):193-194. DOI: https://doi.org/10.1056/NEJMc1512760
41. Garfall AL, Stadtmauer EA, Hwang WT, et al. Anti-CD19 CAR T cells with high-dose melphalan and autologous stem cell transplantation for refractory multiple myeloma. JCI Insight. 2018;3(8):e120505. DOI: https://doi.org/10.1172/jci.insight.120505
42. Garfall AL, Cohen AD, Susanibar-Adaniya SP, et al. Anti-BCMA/CD19 CAR T cells with early immunomodulatory maintenance for multiple myeloma responding to initial or later-line therapy. Blood Cancer Discovery. 2023;4(2):118-133. DOI: https://doi.org/10.1158/2643-3230.BCD-22-0074
43. Du J, Fu WJ, Jiang H, et al. Updated results of a phase I, open-label study of BCMA/CD19 dual-targeting fast CAR-T GC012F for patients with relapsed/refractory multiple myeloma (RRMM). Journal of Clinical Oncology. 2023;41(16_suppl):8005. DOI: https://doi.org/10.1200/JCO.2023.41.16_suppl.8005
44. Wang Y, Cao J, Gu W, et al. Long-term follow-up of combination of B-cell maturation antigen and CD19 chimeric antigen receptor T cells in multiple myeloma. Journal of Clinical Oncology. 2022;40(20):2246-2256. DOI: https://doi.org/10.1200/JCO.21.01676
45. Mei H, Li C, Jiang H, et al. A bispecific CAR-T cell therapy targeting BCMA and CD38 in relapsed or refractory multiple myeloma. Journal of Hematology and Oncology. 2021;14(1):161. DOI: https://doi.org/10.1186/s13045-021-01170-7
46. Tang Y, Yin H, Zhao X, et al. High efficacy and safety of CD38 and BCMA bispecific CAR-T in relapsed or refractory multiple myeloma. Journal of Experimental and Clinical Cancer Research. 2022;41(1):2. DOI: https://doi.org/10.1186/s13046-021-02214-z
47. Zhang H, Liu M, Xiao X, et al. A combination of humanized anti-BCMA and murine anti-CD38 CAR-T cell therapy in patients with relapsed or refractory multiple myelomaю Leukemia and Lymphoma. 2022;63(6):1418-1427. DOI: https://doi.org/10.1080/10428194.2022.2030476
48. Li C, Wang X, Wu Z, et al. Bispecific CS1-BCMA CAR-T cells are clinically active in relapsed or refractory multiple myeloma: an updated clinical studyю Blood. 2022;140(Supplement 1):4573-4574. DOI: https://doi.org/10.1182/blood-2022-170686
49. Lee L, Lim WC, Galas-Filipowicz D, et al. Limited efficacy of APRIL CAR in patients with multiple myeloma indicate challenges in the use of natural ligands for CAR T-cell therapy. Journal for Immunotherapy of Cancer. 2023;11(6):e006699. DOI: https://doi.org/10.1136/jitc-2023-006699
50. Fousek K, Watanabe J, Joseph SK, et al. CAR T-cells that target acute B-lineage leukemia irrespective of CD19 expression. Leukemia. 2021;35(1):75-89. DOI: https://doi.org/10.1038/s41375-020-0792-2
51. Maude SL, Laetsch TW, Buechner J, et al. Tisagenlecleucel in children and young adults with B-cell lymphoblastic leukemia. New England Journal of Medicine. 2018;378(5):439-448. DOI: https://doi/10.1056/NEJMoa1709866
52. Neelapu SS, Locke FL, Bartlett NL, et al. Axicabtagene ciloleucel CAR T-cell therapy in refractory large B-cell lymphoma. New England Journal of Medicine. 2017;377(26):2531-2544. DOI: https://doi.org/10.1056/NEJMoa1707447
53. Wang M, Munoz J, Goy A, et al. KTE-X19 CAR T-cell therapy in relapsed or refractory mantle-cell lymphoma. New England Journal of Medicine. 2020;382(14):1331-1342. DOI: https://doi.org/10.1056/NEJMoa1914347
54. Abramson JS, Palomba ML, Gordon LI, et al. Lisocabtagene maraleucel for patients with relapsed or refractory large B-cell lymphomas (TRANSCEND NHL 001): a multicentre seamless design study. The Lancet. 2020;396(10254):839-852. DOI: https://doi.org/10.1016/S0140-6736(20)31366-0