Изучение эффектов фонтурацетама на модели хронического непредсказуемого умеренного стресса (CUMS) у крыс
Aннотация
Актуальность: Хронический стресс может приводить к таким неблагоприятным последствиям как развитие синдрома профессионального выгорания (СПВ). Учитывая социальную значимость заболевания и отсутствие общепринятых схем лечения, поиск средств терапии СПВ является актуальной задачей. Схожесть этиологии СПВ (хронический стресс), а также некоторых биохимических, поведенческих и когнитивных изменений у человека с СПВ и у животных с моделируемым стрессом делает возможным использование экспериментальных моделей стресса для изучения некоторых аспектов СПВ и оценки терапевтической эффективности препаратов. Цель исследования:Изучить терапевтическую эффективность препарата МНН: фонтурацетам (ООО «Гелеспон», Россия) на модели хронического непредсказуемого умеренного стресса (Chronic unpredictable mild stress, CUMS) у крыс для получения экспериментальных доказательств целесообразности применения препарата у пациентов с СПВ. Материалы и методы:CUMS моделировали на самцах крыс Wistar путем предъявления семи чередующихся стрессовых стимулов в течение 21 дня. Фонтурацетам (10 мг/кг, 30 мг/кг, 100 мг/кг) и препарат сравнения мезокарб (5 мг/кг) вводили внутрижелудочно на фоне моделируемого стресса ежедневно в течение 28 дней. В эксперимент были включены две контрольные группы: «интактные» нестрессированные крысы и крысы, подвергшиеся стрессу. Обе контрольные группы получали плацебо. Результаты:Терапия фонтурацетамом в дозах 10 мг/кг и 30 мг/кг улучшала процессы обучения и памяти стрессированных крыс в тесте «Распознавание нового объекта». У этих животных не наблюдалось поведенческих изменений, характеризующих развитие тревожного поведения (тест «Приподнятый крестообразный лабиринт»). В тесте Порсолта стрессированные крысы, получавшие фонтурацетам, демонстрировали стратегию поведения, которая характеризовалась высоким уровнем активного поведения. Фонтурацетам препятствовал повышению концентрации кортикостерона и кортизола в крови стрессированных крыс. Мезокарб в дозе 5 мг/кг оказал сопоставимый терапевтический эффект, за исключением влияния на когнитивные функции. Заключение:По совокупности полученных результатов наибольший фармакологический эффект в отношении коррекции нарушений, индуцированных хроническим стрессом у крыс, оказал фонтурацетам в дозах 10 мг/кг и 30 мг/кг. Полученные результаты позволяют рассматривать фонтурацетам как лекарственный препарат, снижающий выраженность поведенческих, нейроэндокринных и когнитивных нарушений, которые возникают на фоне хронического стресса и/или СПВ
Ключевые слова: хронический непредсказуемый умеренный стресс, синдром профессионального выгорания, депрессия, экспериментальные модели, фонтурацетам
Введение. Темп современной жизни требует от человека значительных физических и психологических усилий. Защитные нейроэндокринные механизмы позволяют организму справляться со сложными ситуациями. Но если индивидуум воспринимает вредный стимул как слишком интенсивный или как слишком длительный, возникающая стрессовая реакция может стать причиной различных заболеваний. Не все стимулы, вызывающие сильные нейроэндокринные реакции, являются настоящими стрессорами, а только те, которые превышают способность человека меняться и адаптироваться [1].
Если вызвавший стресс стимул сохраняется, активация гипоталамо-гипофизарно-надпочечниковой оси приводит к выбросу глюкокортикоидов. В ситуациях, когда стрессор является подавляющим и не может быть устранен, стресс становится хроническим. Последствиями хронического стресса могут стать общее ухудшение когнитивных способностей, увеличение риска нейродегенеративных заболеваний, развитие депрессии, а также развитие синдрома профессионального выгорания [1].
В настоящее время синдром профессионального выгорания (СПВ) признан медицинским расстройством и имеет собственный код Международной классификации болезней (МКБ) – МКБ-10 (Z73.0 – Burn-out, Переутомление) и МКБ-11 (QD85 – Burnout). В МКБ-11 СПВ определяется как синдром, являющийся результатом хронического стресса на рабочем месте, с которым не удалось справиться. Он характеризуется тремя проявлениями: 1) чувством истощения энергии или изнеможения; 2) повышенной психической дистанцированностью от работы или чувством негативизма или цинизма по отношению к работе; и 3) чувством неэффективности и отсутствия выполненного долга [2, 3, 4].
Выгорание рассматривалось изначально как явление, исключительно связанное с профессиональным контекстом. Но на сегодняшний день этот термин приобрел более широкое понимание, и выгорание определяется как истощение из-за длительного воздействия любой эмоционально сложной ситуации, которая может не быть связана с работой [5, 6].
Будучи по своей природе психологическим феноменом, СПВ, при длительном воздействии, приводит к ряду неблагоприятных последствий, затрагивающих и физиологические функции организма. Различные исследования связывают этот синдром с проблемами концентрации внимания, ухудшением памяти, трудностями в принятии решений, снижением способности справляться с возникшими сложностями, тревожностью, депрессией, неудовлетворенностью жизнью, низкой самооценкой, бессонницей, раздражительностью и повышенным потреблением алкоголя и табака [7-10].
В настоящее время обсуждается вопрос о том, что выгорание этиологически, клинически имеет много сходных с депрессией проявлений. В ряде исследований предполагается, что выгорание может являться формой депрессии [11-17]. Однако различия в определениях выгорания и методах его оценки затрудняют анализ имеющихся данных по изучению выгорания и депрессии и свидетельствует о важности разработки диагностических критериев [13, 18, 19]. Диагностика СПВ представляет определенные трудности в связи с общностью симптомов СПВ не только депрессии, но и тревожных расстройств [14].
Основным инструментом для постановки диагноза СПВ являются психодиагностические методики – опросники. Надежных биомаркеров СПВ на сегодняшний день не найдено [5, 20, 21].
Общепризнано, что функциональная активность гипоталамо-гипофизарно-надпочечниковой (ГГН) оси нарушается при СПВ [22]. Функция ГГН оси при выгорании в основном оценивается по изменению уровня кортизола. В ряде исследований отмечается увеличение уровня кортизола при СПВ, однако также есть данные, указывающие на отсутствие таких изменений [5, 23].
Хотя симптомы выгорания и депрессии во многом сходны, данные о нейроэндокринологических изменениях свидетельствуют о том, что биологическая основа этих расстройств различна. Именно на этом основании считается, что антидепрессанты не следует назначать для терапии СПВ, потому что препараты могут усугубить основную дисфункцию ГГН системы [24].
На сегодняшний день, в числе наиболее перспективных направлений лечения СПВ, рассматриваются различные психотерапевтические методики. Медикаментозная терапия может включать использование седативных средств, анксиолитиков, антидепрессантов, гормональных средств, витаминов, а также растительных адаптогенов (например, родиола розовая, обладающая стимулирующим центральную нервную систему действием) [24-27].
Можно предположить, что ноотропные препараты, оказывающие улучшающее когнитивные функции действие, умеренное психостимулирующее действие, повышающие работоспособность и снижающие утомляемость, могут иметь определенные терапевтические перспективы при СПВ. Одним из таких веществ может быть N-карбамоил-метил-4-фенил-2-пирролидона (МНН: фонтурацетам; торговые наименования: фенотропил, карфедон).
В связи с высокой индивидуальной вариативностью протекания СПВ, сложностями дифференциальной диагностики, в том числе между СПВ и депрессией, отсутствием однозначных биомаркеров состояния, наличием факторов предрасположенности к развитию СПВ, отсутствием стандартов медикаментозного лечения, особую сложность представляет разработка экспериментальной модели СПВ для оценки терапевтической эффективности лекарственных препаратов. Тем не менее, учитывая патогенез СПВ, который, как признает большинство исследователей, является результатом постоянного воздействия стрессовых факторов, а также общность ряда симптомов СПВ и депрессии, представляется возможным моделировать отдельные аспекты СПВ на модели, воспроизводящей депрессивно-подобные изменения у грызунов посредством постоянного воздействия стрессовых факторов.
Хронический умеренный стресс (CMS) является широко используемой моделью вызванных стрессом депрессивно-подобных расстройств на животных [28]. Патологические изменения возникают вследствие воздействия стрессовых факторов в течение определенного времени. Модель CMS была разработана в конце 1980-х годов на основе наблюдения, что у крыс, подвергшихся воздействию множества относительно сильных стрессоров, потребление сладкого раствора сахарозы или сахарина было снижено по сравнению с интактными животными [29]. Позже P. Willner с коллегами использовали набор более мягких стрессоров, при которых животные постоянно подвергались воздействию этих факторов непредсказуемым образом. Воздействие стрессовых факторов было продлено на срок до 3 месяцев [30]. Привлекательной особенностью модели хронического умеренного непредсказуемого стресса (chronic unpredictable mild stress – CUMS) является ряд поведенческих и физиологических изменений, наблюдаемых после воздействия стрессовых факторов, которые сходны с клиническими симптомами депрессии. Следует отметить, что модель CUMS позволяет также моделировать патологические изменения когнитивных функций (обучение, память), изменения социального поведения [31].
По CUMS накоплено большое количество данных о влиянии стресса на поведение грызунов, меньшее количество исследований посвящено клеточным и биохимическим изменениям, вызванных стрессом. Выявление биохимических изменений имеет важное трансляционное значение, поскольку данные изменения могут быть потенциальными биомаркерами депрессивно-подобных состояний. В частности, в экспериментах на крысах было показано, что CUMS приводит к повышению уровней кортизола и кортикостерона [32-35], а также к метаболическим нарушениям: повышению уровня инсулина, нарушению толерантности к глюкозе [33, 34], повышению уровня грелина, снижению лептина, снижению уровня триглицеридов и холестерина [34].
Общность ряда симптомов депрессии и СПВ, а также то, что в основе протокола CUMS лежит воздействие стрессовых факторов, позволяет рассматривать данную модель на животных как наиболее релевантную для моделирования отдельных аспектов СПВ с целью дальнейшей оценки терапевтической эффективности лекарственных кандидатов. Длительное воздействие стрессовых факторов (до 3 месяцев) может приводить к более выраженным патологическим изменениям, характерным для депрессии. Для моделирования аспектов СПВ с целью оценки эффективности лекарственных кандидатов целесообразно использовать наиболее короткий протокол с 21-дневным предъявлением стрессовых факторов.
Цель исследования. Изучить терапевтическую эффективность препарата МНН: фонтурацетам (ООО «Гелеспон», Россия) на модели хронического непредсказуемого умеренного стресса у крыс для получения экспериментальных доказательств целесообразности применения препарата у пациентов с СПВ.
Материалы и методы исследования. Эксперименты проведены на самцах крыс Wistar возраста 6-8 недель (питомник АО «НПО «ДОМ ФАРМАЦИИ»). Животных содержали в соответствии с Директивой 2010/63/EU Европейского парламента и совета Европейского Союза от 22 сентября 2010 г. по охране животных, используемых в научных целях, за исключением периода моделирования стресса. Животные случайным образом были разделены на 6 групп (12 самцов/группа). Контролем служили две группы животных – нестрессированные (далее по тексту: «интактные») и животные, подвергшиеся стрессу, не получавшие терапии.
Исследование рассмотрено на биоэтической комиссии на соответствие проекта исследования принципам «Трех R» и Директиве 2010/63/EU и одобрено для проведения (№ БЭК 1.7/22 от 02.03.2022 г.)
Для оценки терапевтической эффективности фонтурацетама были смоделированы отдельные аспекты симптомокомплекса СПВ с помощью модели хронического непредсказуемого умеренного стресса [36], с модификацией. Крысы подвергались 7 стрессорным факторам 3 раза, таким образом, общая продолжительность формирования патологии составила 21 день (Рис. 1).
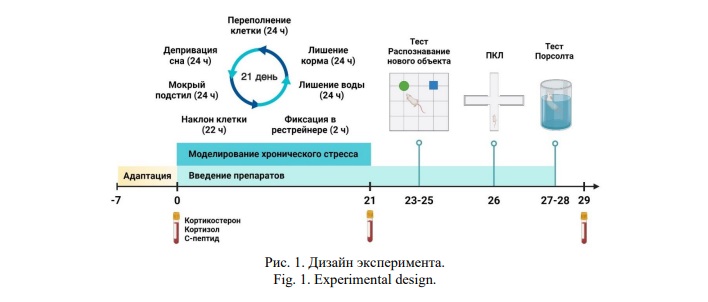
В данном исследовании были использованы следующие стрессорные факторы:
1. Переполнение клетки содержания (5 крыс в клетке, рассчитанной под индивидуальное содержание, на 24 ч). Животные были размещены таким образом, что в каждой клетке находилось по 1 особи из каждой группы. В таком же составе животные размещались вместе каждый раз, когда осуществлялось переполнение клетки.
2. Депривация сна (стресс по Жуве) в течение 24 ч. В клетку содержания помещали платформу-цилиндр высотой 6 см и диаметром 6,5 см. Затем клетку наполняли холодной водой на 3 см от дна. Крыс помещали на платформу, окруженную водой. Приспосабливаясь спать на платформе, животное в моменты расслабления мышц падает в воду, затем снова возвращается на платформу, в результате в течение суток лишается сна.
3. Мокрый подстил в течение 24 ч;
4. Наклон стандартной клетки содержания на 45 градусов в течение 22 ч;
5. Фиксация животного в рестрейнере на 2 ч;
6. Водная депривация в течение 24 ч;
7. Пищевая депривация в течение 24 ч.
Препараты и плацебо вводили животным внутрижелудочно в течение 28 дней, один раз в день, начиная с первого дня эксперимента. В период проведения поведенческих тестов препараты вводили примерно за 1 ч до проведения манипуляций. Субстанции препаратов растворяли в Полисорбате 80, затем полученную суспензию доводили водой очищенной до необходимых концентраций. Контрольные («интактные» и стрессированные, не получавшие терапии) животные получали 10% водный раствор Полисорбата 80. Объем введения составил 2 мл/кг. Фонтурацетам был изучен в трех дозах – 10 мг/кг, 30 мг/кг и 100 мг/кг. В качестве препарата сравнения использовали мезокарб, который вводили в дозе 5 мг/кг. Мезокарб – психостимулятор, среди показаний к применению которого разные виды астенических состояний, протекающих с вялостью, апатией, снижением работоспособности [37].
Массу тела у животных регистрировали на 1-й, 7-й, 14-й, 21-й и 29-й дни эксперимента.
Для оценки последствий стресса использовали методики поведенческого анализа и проводили биохимические исследования крови.
Тест «Распознавание нового объекта». Экспериментальная камера представляла собой бокс размером 80×80×30 см c непрозрачными бортами, дно которого не покрыто подстилочным материалом. Тест выполняли в 3 этапа: адаптация к экспериментальным условиям (10 мин, 23-й день эксперимента); ознакомление с двумя одинаковыми объектами (10 мин, 24-й день); предъявление старого и нового объектов (10 мин, тестовая сессия, 25-й день).
Тест начинался с помещения животного в центр установки. В первый день теста животных габитуировали к установке. На второй день теста в углах установки размещали 2 одинаковых объекта (стеклянные баночки высотой 11 см) для ознакомления. На третий день теста в тех же позициях был размещен знакомый объект (стеклянная баночка) и новый объект (бутылочка из непрозрачного пластика высотой 11 см). Чтобы избежать предпочтения места расположения объектов в тестовой сессии у половины животных каждой группы старый объект располагался в левом углу, новый объект – в правом углу, у остальной половины животных – наоборот.
В тестовой сессии фиксировалось общее время (в секундах), потраченное на изучение каждого объекта (обнюхивание, лизание, касание объекта или подход к нему на расстояние <1 см). Для оценки распознавания объекта был рассчитан индекс предпочтения [38] по формуле 1:
Tновый – это время, потраченное на изучение нового объекта, секунды;
Tстарый – это время, потраченное на изучение старого объекта, секунды.
В течение всех сессий теста также была оценена локомоторная активность животных (количество пересеченных квадратов; количество центровых посещений; количество свободных стоек; количество пристеночных стоек).
Тест «Приподнятый крестообразный лабиринт» (ПКЛ). Тест проводили на 26-й день эксперимента. Установка для проведения ПКЛ состояла из крестообразно расходящихся от центральной площадки под прямым углом 4-х рукавов: два противоположных, светлых, из прозрачного пластика, и два закрытых, темных. Центральная площадка и пол открытых рукавов прозрачны, тогда как пол и стенки закрытых рукавов окрашены в темный цвет. Процедура тестирования осуществлялась при обычном освещении с интенсивностью светового потока в 300 лк. Длительность теста – 3 мин. По истечении времени наблюдения животное извлекалось из установки и помещалось в клетку содержания. В случае если животное покидало лабиринт, его как можно скорее помещали в центр установки, время тестирования при этом было скорректировано (увеличено с учетом времени нахождения вне лабиринта). После каждого животного установку протирали 3% раствором перекиси водорода. Оцениваемые параметры: общая продолжительность пребывания в «темных» и «светлых» рукавах; число заходов в темные и светлые рукава; количество стоек в центральной части; количество болюсов дефекации; количество попыток покинуть установку.
Тест Порсолта (тест принудительного плавания). Тест проводили на 27-28-й дни эксперимента. Для тестирования были использованы 4 цилиндра из оргстекла (d = 20 см; h = 45 см), которые были заполнены водой (температура воды 24 ± 1°C) до глубины 30 см. Цилиндры были отделены друг от друга непрозрачными перегородками, не позволяющими животным видеть друг друга во время теста. После каждого теста проводили замену воды и мытье цилиндра, поскольку было показано, что вторичное использование воды может влиять на поведение животных из-за наличия ольфакторных «сигналов тревоги» [39]. Процедура представляла собой «классический» двухдневный протокол теста принудительного плавания [40]. В первый день (претест – этап выработки состояния «поведенческого отчаяния» [40] или пассивной копинг-стратегии [41]) крысы помещались в цилиндры с водой на 15 мин. Через 24 часа после первой посадки животным вводили препараты. Через 1 час после введения животных снова помещали в цилиндры с водой на 5 мин (тест – этап оценки стратегии поведения). В претесте (за первые 5 мин) и тесте (за 5 мин) анализировали следующие элементы поведения (продолжительность в секундах): неподвижность (дрейфование – отсутствие движений конечностями или выполнение мелких движений конечностями и хвостом для удержания головы на поверхности воды); плавание (ориентирование, сопровождающееся совершением движений всеми конечностями); гребля (ориентирование, перемещение с помощью ритмичных движений задних конечностей); залезание/карабканье на стенку (поведение избегания – тело крысы в вертикальном положении, интенсивные движения всех конечностей с выбросом передних лап над поверхностью воды с касанием стенки цилиндра); ныряние (поведение избегания – активное погружение под воду, перемещение по направлению ко дну цилиндра). В тесте также было подсчитано количество находящихся в воде болюсов дефекации (индекс эмоциональности).
Биохимический анализ крови. Кровь у животных была забрана на 3 точках: 1-й день (исходная точка), 21-й день (по окончании периода моделирования стресса), 29-й день (по окончании эксперимента). На всех точках кровь забирали в утренние часы (с 9:00 до 10:30) из хвостовой вены в объеме 1 мл, под общей ингаляционной анестезией с применением изофлурана. Изофлуран (вместо стандартной иммобилизации в рестрейнере) и габитуация были использованы для минимизации влияния острого стресса на определяемые показатели. В сыворотке крови определяли концентрации кортикостерона и кортизола (маркеры стресса), С-пептида (маркер нарушения метаболизма глюкозы), триглицеридов.
Концентрацию С-пептида и гормонов в крови определяли методом ИФА с помощью коммерчески доступных наборов. Для определения кортикостерона использовали набор «Corticosterone ELISA» (№ EIA-4164, lot 61K012, «DRG Instruments GmbH», Germany), аналитический диапазон методики 5–240 нмоль/л; кортизола – «Кортизол-ИФА-Бест» (№ Х-3964, серия 147, АО «Вектор-Бест», Россия), аналитический диапазон методики 12,5-1200 нмоль/л; С-пептида - «Elisa kit for C-Peptide» (№ CEA447Ra, lot L220615568, «Сloud-Clone Corp.», Китай), аналитический диапазон методики 0,124–10 нг/мл.
Образцы сыворотки крови крыс для определения кортикостерона перед анализом разбавляли в 100 раз 0,01М фосфатно-солевым буферным раствором (pH=7,4±0,2).
Анализ образцов выполняли в соответствии с инструкцией производителей. Оптическую плотность растворов измеряли на многофункциональном микропланшетном анализаторе «CLARIOstar» (BMG Labtech, Германия) при двух длинах волн 450 нм (основная длина волны) и 650 нм (референсная длина волны).
По окончании эксперимента животных эвтаназировали с применением СО2 с последующим перерезанием основных кровеносных сосудов.
Статистический анализ выполняли с помощью программы Prism 9 (GraphPad Software, США). Для оценки данных с признаками нормального распределения использовали однофакторный дисперсионный анализ (One-way ANOVA). Для оценки связанных данных использовали дисперсионный анализ c повторными измерениями (Repeated measures ANOVA). В случае обнаружения достоверного влияния исследуемого фактора последующие межгрупповые сравнения (post hoc analysis) проводили с использованием критерия Тьюки (Tukey`s test analysis) или критерия Даннета (Dunnett's test). Различия определяли при уровне значимости р≤0,05.
Результаты и их обсуждение
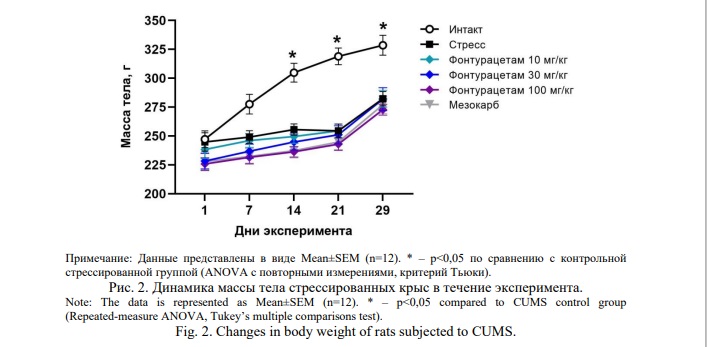
У контрольных «интактных» животных на протяжении всего эксперимента масса тела статистически значимо увеличивалась относительно исходного уровня. Хронический стресс привел к значительному замедлению прироста массы тела у стрессированных крыс, не получавших лечения. У стрессированных крыс, получавших фонтурацетам и мезокарб, значимого увеличения массы относительно исходного уровня, как и у контрольных стрессированных животных, не получавших терапии, не наблюдалось (Рис. 2). Отсутствие терапевтического эффекта, вероятно, обусловлено тем, что оба исследуемых препарата обладают анорексигенной активностью при курсовом применении [37]. Замедление динамики прироста массы тела у стрессированных животных, получавших препараты, может быть связано не со стрессогенным воздействием, а со снижением потребления корма.
Распознавание нового объекта
Из анализа были исключены животные, у которых суммарное время изучения обоих объектов составило менее 10 секунд, а также животные, которые не исследовали один из объектов, поскольку в таких случаях невозможно утверждать, что животные потратили достаточное количество времени на изучение объектов, чтобы различать их между собой [38].
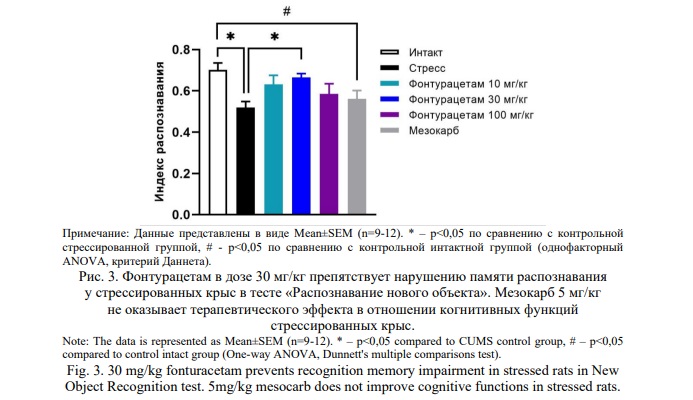
При анализе рассчитанных индексов распознавания нового объекта показано статистически значимое снижение распознавания нового объекта у контрольных стрессированных животных, не получавших терапию, по сравнению с контрольными «интактными» крысами (Рис. 3).
У группы, получавшей фонтурацетам в дозе 30 мг/кг, индекс распознавания был выше по сравнению с контрольными стрессированными крысами, не получавшими терапию (p<0,05). Та же тенденция наблюдалась в группе, получавшей фонтурацетам в дозе 10 мг/кг. Фонтурацетам в дозе 100 мг/кг не оказал выраженного терапевтического эффекта. У стрессированных крыс, получавших мезокарб, отмечено значимое снижение индекса распознавания относительно контрольных «интактных» животных (p<0,05), то есть мезокарб не способствовал улучшению процессов обучения и памяти стрессированных крыс (Рис. 3).
При оценке локомоторной активности крыс в рамках данного теста показано, что горизонтальная локомоторная активность контрольных стрессированных крыс, не получавших лечения, была, в целом, сопоставима с показателями контрольных «интактных» крыс. У стрессированных животных, получавших фонтурацетам в дозах 30 мг/кг и 100 мг/кг, на протяжении всех трех сессий теста наблюдалась выраженная тенденция к увеличению локомоторной активности по сравнению с «интактными» крысами (на 31-43%) и с контрольными стрессированными крысами (на 20-37%). У животных группы мезокарба локомоторная активность была так же выше по сравнению с контрольными группами (данные не представлены).
Таким образом, установлено, что фонтурацетам улучшает когнитивные функции (память, внимание, обучаемость) у стрессированных животных. Полученные на модели CUMS результаты, в совокупности с имеющимися клиническими данными о положительном влиянии фонтурацетама на когнитивные функции, позволяют прогнозировать наличие у данного препарата терапевтического действия, направленного на улучшение когнитивных функций у пациентов с установленным СПВ.
Приподнятый крестообразный лабиринт
При анализе времени пребывания в разных частях лабиринта выявлено влияние фактора «группа» на показатель «время пребывания в темных рукавах» (p<0,05; однофакторный ANOVA). Контрольные стрессированные крысы, не получавшие лечения, больше времени находились в темных рукавах по сравнению с контрольными «интактными» крысами (p<0,05), наблюдалась тенденция к снижению времени пребывания и количества заходов в светлые рукава и к снижению времени пребывания в центре. Поведение стрессированных крыс, получавших препараты, достоверно не отличалось от поведения контрольных «интактных» крыс (Рис. 4).
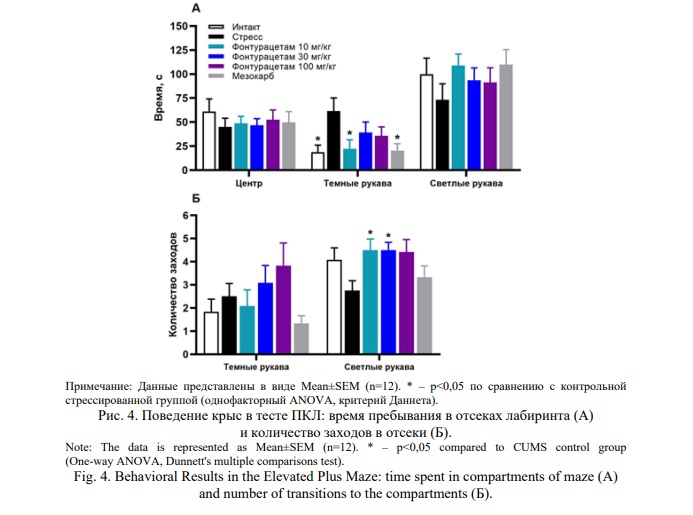
В ходе проведения теста у некоторых животных были зарегистрированы попытки покинуть лабиринт. Наибольшее количество попыток (суммарно 10) покинуть лабиринт и количество их совершавших животных (4 крысы), было зарегистрировано у контрольных «интактных» животных. Данное поведение можно рассматривать как повышение ориентировочно-исследовательских реакций, характеризующее низкий уровень тревожности у контрольных «интактных» животных. Контрольные стрессированные крысы, не получавшие лечения, не совершали подобных попыток вовсе. Важно отметить, что данное поведение было зарегистрировано в единичных случаях в группах, получавших фонтурацетам в дозах 30 мг/кг (1 крыса) и 100 мг/кг (1 крыса), а также в группе мезокарба (2 крысы).
Тесты на тревожность (ПКЛ, открытое поле, темно-светлая камера) основаны на конфликте между естественным стремлением грызунов исследовать новое и стремлением избегать неизвестное [42]. Животным предлагается выбор между аверсивными (исследование открытого/освещенного пространства) и неаверсивными (исследование закрытого/неосвещенного пространства) стимулами. Предпочтение крыс исследовать открытые пространства свидетельствует о сниженном уровне тревожности.
В данном эксперименте поведение контрольных стрессированных крыс, не получавших лечения, характеризировалось повышенным уровнем тревожности. В сравнении с контрольными «интактными» животными, стрессированные крысы, не получавшие лечения, не отдавали предпочтение светлым рукавам, больше времени проводили в темных рукавах, а также не совершали попыток покинуть лабиринт. Поведение стрессированных животных, получавших фонтурацетам, было в целом сопоставимо с поведением контрольных «интактных» животных. Животные, получавшие дозы 10 мг/кг и 30 мг/кг, чаще заходили в светлые рукава по сравнению с контрольными стрессированными крысами, не получавшими лечения (доза 100 мг/кг – аналогичная тенденция, p=0,059), совершали попытки покинуть лабиринт. Мезокарб оказал схожее влияние на поведение стрессированных крыс.
Полученные результаты на модели CUMS, в совокупности с имеющимися клиническими данными о анксиолитических эффектах фонтурацетама, позволяют предполагать, что фонтурацетам будет обладать анксиолитическим действием у пациентов с СПВ.
Тест Порсолта
Претест. Анализ выявил влияние фактора «группа» на все показатели (p<0,05; однофакторный ANOVA). У контрольных стрессированных крыс, не получавших лечения, соотношение подвижности и неподвижности было в большей степени смещено в сторону подвижности, чем у контрольных «интактных» животных. Увеличение подвижности контрольных стрессированных крыс, не получавших лечения, происходило за счет значимого увеличения времени поведения ориентирования (плавания и гребли). Уже на этапе претеста можно отметить различия в стратегии поведения двух контрольных групп. Контрольные «интактные» крысы при первом ознакомлении с условиями теста отдавали предпочтение реакциям активного избегания, контрольные стрессированные крысы, не получавшие лечения – поведению ориентирования (Рис. 5). Реакции борьбы у контрольных стрессированных крыс, не получавших лечения, были снижены относительно контрольных «интактных» животных.
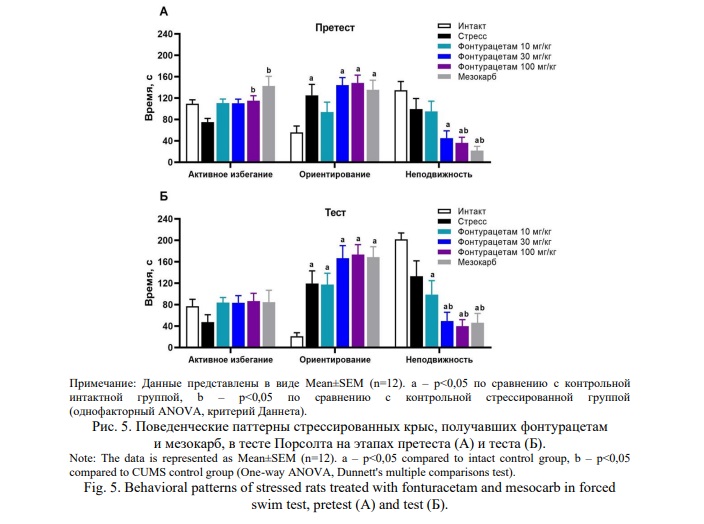
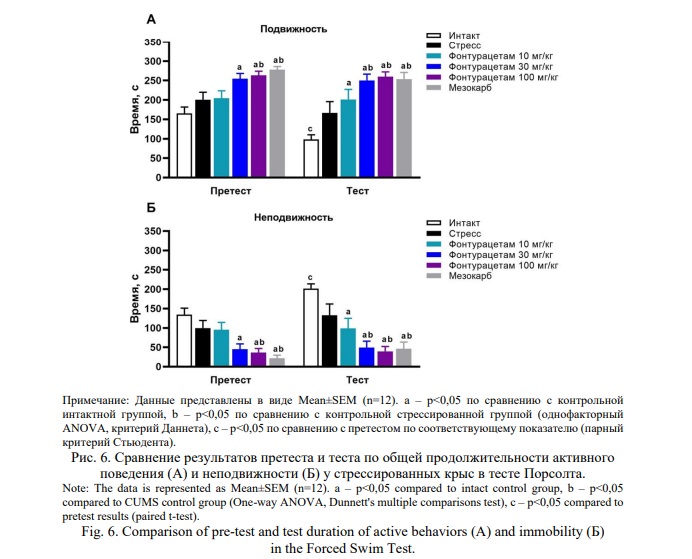
В группах, получавших фонтурацетам, наблюдалось дозозависимое увеличение времени подвижности и снижение времени неподвижности в сравнении с обеими контрольными группами. Описанное изменение в поведении стрессированных крыс, получавших терапию, достигало максимальной выраженности в группе, получавшей мезокарб (Рис. 6).
Тест. Влияние фактора «группа» выявлено на все показатели (p<0,05; однофакторный ANOVA), за исключением показателя «продолжительность активного избегания» (p>0,05).
Контрольная стрессированная группа, не получавшая лечения, характеризовалась высокой индивидуальной вариабельностью по показателям общей подвижности и неподвижности. В связи с этим увеличение общего времени подвижности и снижение неподвижности у контрольных стрессированных крыс, не получавших лечения, относительно контрольных «интактных» крыс отмечено только на уровне тенденции (p=0,07; критерий Даннета). Увеличение подвижности контрольных стрессированных крыс, не получавших лечения, происходило за счет значимого увеличения времени ориентирования относительно контрольных «интактных» животных (p<0,05; критерий Тьюки).
Стрессированные крысы, получавшие препараты, демонстрировали выраженное увеличение времени подвижности и снижение времени неподвижности относительно обеих контрольных групп. Увеличение подвижности в данных группах происходило за счет значимого увеличения времени ориентирования относительно контроля без патологии. Продолжительность активного избегания у стрессированных крыс, получавших терапию, была выше по сравнению с контрольными стрессированными животными, не получавшими лечения (тенденция) (Рис. 5).
По показателю «количество болюсов дефекации» (индекс эмоциональности) влияния фактора «группа» не выявлено (p>0,05; однофакторный ANOVA).
Дополнительно было проведено внутригрупповое сравнение данных претеста и теста. У контрольных «интактных» крыс продолжительность подвижности снизилась, а неподвижности – увеличилась в тесте в сравнении с претестом (p<0,05; парный критерий Стьюдента). У контрольных стрессированных крыс, не получавших лечения, продолжительность подвижности и неподвижности на тесте в сравнении с претестом не менялась. У стрессированных крыс, получавших препараты, продолжительность активного избегания уменьшалась, а время ориентирования увеличивалось от претеста к тесту (p<0,05; парный критерий Стьюдента). Общая продолжительность подвижности и неподвижности в данных группах не отличались между претестом и тестом (Рис. 6).
Ключевым отличием в поведении контрольных стрессированных крыс, не получавших терапии, от контрольных «интактных» животных, не подвергавшихся хроническому стрессу, является их стратегия преодоления стрессовой ситуации (копинг-стратегия) в условиях теста принудительного плавания. Контрольные «интактные» животные демонстрировали единую стратегию поведения: у всех животных из группы уменьшалось время подвижности и увеличивалось время неподвижности на тесте по сравнению с претестом. У данных животных наблюдался переход от активной стратегии на претесте к пассивной стратегии поведения в тесте: реакции борьбы (карабканье и ныряние) и поведение ориентирования (плавание и гребля) ко 2-му дню тестирования угасали и сменялись в сторону неподвижности. В настоящий момент смена активной стратегии на пассивную стратегию поведения в условиях неизбегаемого острого стресса (принудительное плавание в замкнутом пространстве) рассматривается исследователями как поведенческая адаптация и успешная копинг-стратегия, характеризующая память и процесс обучения, который способствует выживанию [43-46].
Контрольные стрессированные животные, не получавшие терапии, внутри группы принимали противоположные стратегии поведения: часть животных демонстрировала переход к пассивной стратегии, другая часть – наоборот, увеличивали время подвижности (за счет поведения ориентирования). Учитывая однонаправленную реакцию контрольных «интактных» крыс на условия теста, можно сказать, что у стрессированных крыс, не получавших терапию, отсутствует подобная адаптивная реакция.
У стрессированных крыс, получавших препараты, на обоих этапах теста наблюдалась активная копинг-стратегия, время неподвижности в целом не изменялось от претеста к тесту. В группах фонтурацетама продолжительность активного поведения нарастала, а продолжительность неподвижности уменьшалась с увеличением дозы, что свидетельствует о дозозависимости эффекта. У контрольных стрессированных крыс, не получавших лечения, отсутствовал выраженный переход к пассивной стратегии, который наблюдался у всех контрольных «интактных» животных. Сохранение активной копинг-стратегии у стрессированных крыс, получавших терапию, обусловлено фармакологическим эффектом исследуемых препаратов (стимулирующий эффект, повышение выносливости).
Зарегистрированное на модели CUMS изменение поведенческой стратегии, характерной для подвергшихся стрессу крыс, может свидетельствовать о потенциальном влиянии фонтурацетама на стратегии поведения, и о том, что фонтурацетам будет способствовать превалированию стратегий преодоления трудностей – копинг-стратегий. Полученные данные обосновывают применение фонтурацетама при снижении адаптационных возможностей организма и нарушении стратегии преодоления трудностей.
Биохимические исследования
Поскольку известно, что СПВ может вызывать метаболические нарушения и является предиктором диабета 2 типа [7, 8], в данном эксперименте было изучено влияние стресса и введения препаратов на концентрацию С-пептида и уровень триглицеридов в крови. Статистически значимых изменений концентрации С-пептида не было обнаружено (данные не представлены). Хронический стресс не привел к изменениям уровня C-пептида у контрольных стрессированных крыс, не получавших терапию, относительно показателей контрольных «интактных» животных. Препараты не оказали значимого влияния на уровень C-пептида.
По окончании периода моделирования стресса (21-й день) у контрольных стрессированных крыс, не получавших терапию, концентрация триглицеридов (0,61±0,054 ммоль/л) была статистически значимо ниже (p<0,05) по сравнению с контрольной «интактной» группой (1,18±0,141 ммоль/л) и относительно исходных значений (0,95±0,052 ммоль/л). В группах, получавших препараты, наблюдалось аналогичное снижение. Важно отметить, что фонтурацетам и мезокарб обладают анорексигенной активностью при курсовом применении [37]. Снижение массы тела у крыс приводит к снижению уровня триглицеридов. В данном случае снижение уровня триглицеридов у стрессированных животных, получавших препараты, может быть связано не столько со стрессогенным воздействием, а сколько со снижением потребления корма и замедлением прироста массы тела, вызванных введением фонтурацетама и мезокарба.
Также в ходе эксперимента оценивали динамику концентрация «гормонов стресса». Исходно концентрации кортизола и кортикостерона различались между группами. Для оценки влияния терапии на уровни гормонов стрессированных крыс был рассчитан и проанализирован процент от исходной концентрации каждого из гормонов на 21-й и 29-й дни эксперимента.
Уровни кортикостерона и кортизола контрольных стрессированных животных, не получавших терапию, значимо возрастали к 21-му дню эксперимента относительно контрольных «интактных» животных. У стрессированных крыс, получавших терапию, уровни обоих гормонов к 21-му дню эксперимента были сопоставимы с показателями «интактной» контрольной группы и статистически значимо отличались от показателей контрольных стрессированных крыс, не получавших терапию (Рис. 7). На 29-й день значимых различий между группами не установлено (данные не представлены).
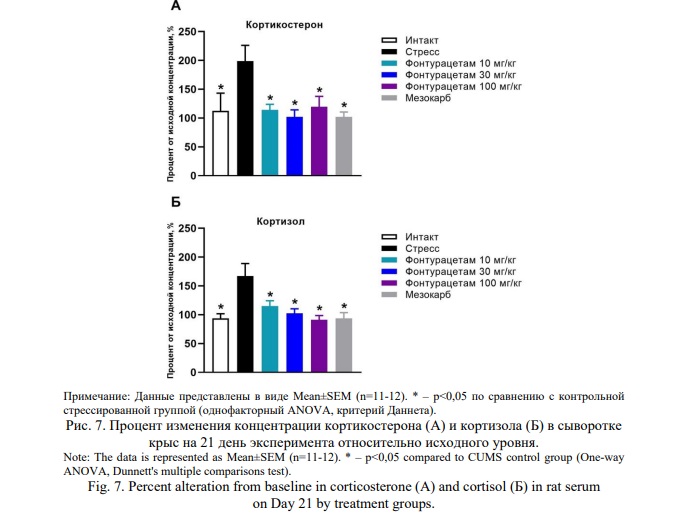
Таким образом, фонтурацетам во всем исследованном диапазоне доз (10-100 мг/кг) и мезокарб в дозе 5 мг/кг препятствовали повышению концентрации «гормонов стресса» – кортикостерона и кортизола в крови стрессированных крыс, что говорит о способности фонтурацетама предотвращать наблюдаемое на фоне стресса нарушение функционирования гипоталамо-гипофизарной оси и связанных с этим патологических изменений.
Физиологическая реакция на стресс также включает выброс анаболических гормонов с защитными и регенеративными свойствами. Наиболее часто изучаемым анаболическим гормоном является дегидроэпиандростерон (ДГЭА). Однако клинические результаты о взаимосвязи уровня ДГЭА и СПВ не однозначны [7]. В предыдущих пилотных экспериментах по отработке модели CUMS оценивали динамику ДГЭА, однако значимого влияния стресса на данный показатель не обнаружили, в связи с чем он не анализировался в данном эксперименте.
Следует отметить, что несмотря на широкое использование модели CUMS в течение нескольких десятилетий, воспроизводимость депрессивно-подобного синдрома, индуцированного CUMS, не является однозначной [47]. Классическими депрессивно-подобными изменениями поведения у крыс, стрессированных по протоколам CUMS, являются снижение потребления сахарозы (ангедония), снижение локомоторной активности, увеличение времени неподвижности («поведение отчаяния») в тесте Порсолта, тревожное поведение. В обзоре Strekalova T. и соавт. [31] обсуждаются «парадоксальные» поведенческие паттерны стрессированных крыс, такие как гиперлокомоция, увеличение времени активной борьбы и снижение неподвижности в тесте Порсолта, отсутствие ангедонии. Аномальное поведение авторы связывают с гетерогенностью популяции («устойчивые» и «восприимчивые» к стрессу крысы), с чувствительностью модели к методическим деталям (вариативность условий проведения тестов), а также с модификациями самого протокола (вариативность стрессорных факторов и продолжительности их воздействия). Принимая во внимание различия протоколов хронического стресса, авторы подчеркивают, что ключевым тестом в модели CUMS является тест предпочтения сахарозы, а развитие ангедонии у крыс – главным критерием валидности модели CUMS как модели депрессии.
В рамках данного проекта были проведены пилотные эксперименты, в которых были отобраны и подтверждены в плане воспроизводимости маркеры поведенческих и биохимических изменений, возникающих в результате хронического стресса. По результатам пилотных исследований не было выявлено ожидаемого снижения потребления раствора сахарозы у стрессированных животных (то есть признаков наличия ангедонии), что соотносится с результатами ряда исследований [31, 47], среди которых есть сообщения о противоречивых результатах, демонстрирующих увеличение потребления раствора сахарозы у стрессированных животных по сравнению с интактными [48, 49]. Это свидетельствует о том, что разработанный протокол не воспроизводит основной характерный для депрессии признак, что, возможно, обусловлено спектром и/или продолжительностью воздействия стрессовых факторов. Отсутствие ангедонии при воспроизведении других поведенческих альтераций (классических или парадоксальных), вероятно, можно рассматривать как признак, дифференцирующий стресс-индуцированные расстройства от депрессивного поведения. Таким образом, вариации модели CUMS, при которых не воспроизводится ангедония, вероятно, можно использовать для моделирования стресс-индуцированных состояний, отличных от депрессии.
Заключение. Моделирование СПВ на животных с помощью известных моделей депрессивно-подобных состояний и интерпретация полученных данных представляется трудной задачей. Тем не менее, схожесть этиологии заболевания делает возможным использование стрессорных моделей на животных для изучения некоторых аспектов СПВ и для поиска препаратов, обладающих терапевтическим потенциалом в отношении данного расстройства.
В проведенном исследовании моделируемый в течение 21 дня хронический непредсказуемый умеренный стресс привел к следующим физиологическим, поведенческим и биохимическим изменениям у крыс: значительному замедлению прироста массы тела, развитию когнитивных нарушений (по результатам теста «Распознавание нового объекта»), увеличению уровня тревожности (по результатам теста «Приподнятый крестообразный лабиринт»), поведенческой дезадаптации (по результатам теста Порсолта), повышению гормонов-маркеров стресса – кортикостерона и кортизола. Показано, что терапия с использованием фонтурацетама в дозах 10 мг/кг и 30 мг/кг была эффективна в отношении коррекции нарушений, индуцированных хроническим стрессом у крыс.
Полученные результаты позволяют рассматривать фонтурацетам как лекарственный препарат, снижающий выраженность поведенческих, нейроэндокринных и когнитивных нарушений, которые возникают на фоне хронического стресса, что может иметь терапевтическую перспективу при СПВ у человека.
Информация о финансировании
Финансирование данной работы не проводилось.





















Список литературы