Влияние саркопенического ожирения и зрительного дефицита на физическую функциональность пожилых пациентов
Aннотация
Актуальность: Саркопеническое ожирение и зрительный дефицит представляют широко распространённые функциональные дефициты, но несмотря на это не проводился анализ их значимости в изменении физической функциональности пожилых пациентов с саркопеническим ожирением и зрительным дефицитом. Цель исследования:Изучение влияния саркопенического ожирения и зрительного дефицита на физическую функциональность пожилых пациентов. Материалы и методы:На базе специализированного офтальмологического отделения обследовано 325 пациентов 60-74 лет с наличием саркопенического ожирения и зрительным дефицитом. Диагностика офтальмопатологии проводилась в соответствии с Клиническими рекомендациями, принятыми в Российской Федерации, и по результатам комплексного инструментального офтальмологического обследования. Выявление саркопенического ожирения выполнено с учётом рекомендаций, предложенных Европейской рабочей группой по шкале European working group on sarcopenia in older people (EWGSOP2, 2018г.). Физическая функциональность оценивалась по мышечной силе, скорости походки, ежедневной двигательной активности в доме/квартире, ежедневной двигательной активности вне дома/квартиры. Контролем служили 280 пациентов без саркопенического ожирения и зрительного дефицита аналогичного возраста. Результаты:У пациентов пожилого возраста с саркопеническим ожирением и зрительным дефицитом установлено снижение мышечной силы до 16,1±0,4 кг, скорости походки – до 0,8±0,06 м/сек, ежедневной двигательной активности в доме/квартире – до 1,8±0,05 час и ежедневной двигательной активности вне дома/квартиры – до 0,6±0,03 час против 21,6±0,5 кг, 1,1±0,05 м/сек, 2,2±0,07 час и 1,1±0,04 час соответственно в группе сравнения. Ассоциация саркопенического ожирения и зрительного дефицита с параметрами физической функциональности оказалась наивысшей для ежедневной двигательной активности вне дома/квартиры с отношением шансов 3,185 при 95% доверительных границах 2,963-3,458. Заключение:Саркопеническое ожирение и зрительный дефицит существенно ухудшают физическую функциональность пожилых пациентов
Ключевые слова: саркопеническое ожирение, зрительный дефицит, пожилые, мышечная сила, скорость походки, физическая функциональность
Введение. Саркопеническое ожирение представляет относительно новый и недостаточно изученный гериатрический синдром как в отечественной, так и зарубежной геронтологии [1-4]. Саркопеническое ожирение возникает, когда снижение мышечной массы тела сопровождается чрезмерным накоплением жировой ткани, особенно висцерального жира. Риск и частота возникновения саркопенического ожирения увеличиваются с возрастом [5]. Растущая частота возникновения саркопенического ожирения и его серьезные последствия делают его значительным бременем для здоровья стареющего населения из-за частоты возникновения серьезных осложнений. И ожирение, и саркопения характеризуются подострым хроническим провоспалительным состоянием (слабым воспалением), которое влияет на метаболические процессы, нарушая функционирование как жировой, так и скелетной мышечной ткани. Поэтому саркопеническое ожирение может вызывать гораздо более серьёзные последствия для здоровья, чем ожирение или саркопения по отдельности [6]. Таким образом, явления саркопении и ожирения могут усиливать друг друга в порочном круге потери мышечной массы и функций, роста висцерального жира и метаболических нарушений. К сожалению, в настоящее время не существует чёткого определения этого состояния [5]. Сосуществование ожирения с саркопенией ускоряет потерю мышечной массы и функций, снижает физическую работоспособность и повышает риск смертности [6].
Саркопения, то есть потеря мышечной массы и силы или нарушение физической функции, естественным образом возникает с возрастом. Саркопения усугубляет неблагоприятные последствия ожирения у пожилых людей, что приводит к саркопеническому ожирению. Саркопеническое ожирение можно охарактеризовать как сочетание двух эпидемий – старения населения и роста уровня ожирения [5]. Поскольку повышенный индекс массы тела, функциональные нарушения, повышенная смертность и снижение качества жизни связаны между собой, борьба с саркопеническим ожирением важна для предотвращения долгосрочной инвалидности у пожилых людей из группы высокого риска [6].
Ожирение обычно определяется как чрезмерное или аномальное накопление жира в организме, которое негативно влияет на здоровье [7]. Дисфункция жировой ткани при ожирении приводит к хроническому воспалению низкой степени тяжести, характеризующемуся активацией провоспалительных путей и смещением высвобождения адипокинов в сторону провоспалительного профиля. Это связано с развитием метаболических и сердечно-сосудистых заболеваний, а также некоторых видов рака. Распространённость ожирения увеличивается с возрастом и в стареющем обществе эта эпидемия ожирения становится всё более серьёзной проблемой здравоохранения [7].
Саркопеническое ожирение распространено среди пожилых в 0,3-9,9% случаев [3] и считается, что его частота будет увеличиваться по мере старения населения и роста численности населения пожилого и старческого возраста в демографической структуре многих государств. Саркопеническое ожирение является важнейшим компонентом синдрома старческой астении, приводит к синдрому падений, переломов, снижению физической активности [8], инструментальной активности в повседневной жизни со зрительным дефицитом [9].
Однако анализ саркопенического ожирения у пациентов со зрительным дефицитом проводится крайне редко, несмотря на то что саркопеническое ожирение и зрительный дефицит в пожилом и старческом возрасте представляют широко распространённые возрастные состояния. При этом предполагается, что патология органа зрения способствует формированию саркопенического ожирения [10], снижению функциональной активности пациентов [9]. Однако физическая функциональность среди пациентов 60-74 лет с наличием саркопенического ожирения и зрительного дефицита практически не рассматривалась в данном контексте отечественными и зарубежными исследователями, хотя у пациентов с саркопеническим ожирением без офтальмопатологии доказана важная роль низкой физической активности в развитии обсуждаемого гериатрического синдрома [3, 8, 11, 12].
В связи с этим зрительный дефицит, ограничивающий двигательную активность пациентов, может способствовать формированию саркопенического ожирения, а сочетание этих двух функциональных дефицитов – снижать физическую функциональность пациентов пожилого возраста. Поэтому научный и практический интерес представляет изучение ассоциации саркопенического ожирения и зрительного дефицита с параметрами физической функциональности пожилых пациентов.
Цель исследования. Изучение влияния саркопенического ожирения и зрительного дефицита на физическую функциональность пожилых пациентов.
Материалы и методы исследования. В клинических условиях специализированного офтальмологического стационара проведено обследование 325 пациентов пожилого возраста с саркопеническим ожирением и зрительным дефицитом по причине различных офтальмологических заболеваний – возрастная макулярная дегенерация, старческая катаракта, диабетическая ретинопатия, составивших основную группу исследования. Диагностика названных офтальмологических заболеваний проведена на основе комплексного осмотра с использованием современного инструментального оборудования, сертифицированного в Российской Федерации: щелевой лампы, оптической когерентной томографии, оптической когерентной томографии с функцией ангиографии, автоматического определения внутриглазного давления и остроты зрения без коррекции, периметрии.
Важно подчеркнуть, что определение остроты без коррекции осуществлялось объективными методами, а под остротой зрения без коррекции понималась реальная (фактическая) острота зрения, которая характерна для пациентов без средств коррекции (оптических линз, очков), но даже после коррекции указанными выше средствами, острота зрения (максимальная корригированная острота зрения) в силу возрастных изменений и других причин не равнялось единице. Понятие «острота зрения без коррекции» вовсе не означает, что зрение у пациентов не корригировалось врачами-офтальмологами и что это запущенные стадии офтальмопатологии. Корригированная острота зрения в силу ряда причин имеет свойство снижаться и не соответствовать 1,0.
Диагностика зрительного дефицита при изученных офтальмологических заболеваниях выполнялось в соответствии с Клиническими рекомендациями, принятыми в Российской Федерации [13, 14, 15].
Группу сравнения в количестве 280 человек составили пациенты такого же возраста с отсутствием саркопенического ожирения и зрительного дефицита, не имевшие соматических заболеваний в острой фазе или декомпенсированной форме.
Выявление саркопенического ожирения проводилось по критериям сниженной мышечной силы, сниженной мышечной массы, а также повышенного индекса массы тела с учетом рекомендаций, предложенных Европейской рабочей группой European working group on sarcopenia in older people (EWGSOP2, 2018 год) [5]. Мышечная сила определялась методом кистевой динамометрии – ручным динамометром «ДМЭР-120» и рассматривалась как низкая у мужчин менее 27 кг, а у женщин менее 16 кг. Сниженная мышечная масса соответствовала величине окружности икроножных мышц в области голени менее 31 см. Ожирением считался индекс массы тела ≥ 30 кг/м2. Скорость походки определялась по тесту 6-ти минутной ходьбы.
Дополнительно для оценки физической функциональности использовались предложенные нами показатели – двигательная активность в доме/квартире, связанная с приготовлением пищи, уборкой и другими бытовыми задачами; двигательная активность вне дома/квартиры, связанная с выполнением покупок, финансовых операций, почтовых отправлений, прогулок.
Сравниваемые клинические группы были практически сопоставимы по основным демографическим параметрам и коморбидному фону (Табл. 1).
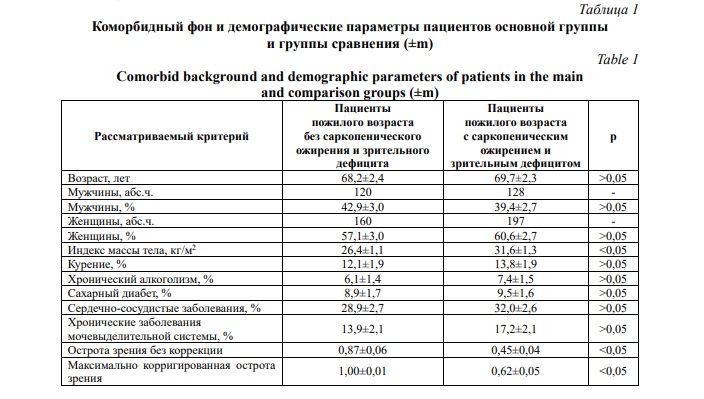
Пациенты рассматриваемых групп достоверно не отличались по возрастному и гендерному составу, коморбидному фону. Вместе с тем у пациентов в основной группе был достоверно выше индекс массы тела и высокий зрительный дефицит по остроте зрения без коррекции и максимально корригированной остроте зрения.
При проведении исследования соблюдались этические нормы и принципы, изложенные в Хельсинской декларации, а в исследование пациенты включались после получения письменного согласия.
При статистической обработке результатов исследования с применением программы «Statistica 15.0» рассчитаны средние и относительные величины, показатели отношения шансов по формуле, приведенной в отечественном руководстве [16]. Различие считалось статистически значимым при p<0,05.
Результаты и их обсуждение. По всем рассматриваемым критериям физической функциональности у пациентов пожилого возраста с наличием саркопенического ожирения и зрительного дефицита она оказалась статистически достоверно сниженной относительно представителей без саркопенического ожирения и зрительного дефицита (Табл. 2). Так, снижение мышечной силы среди пациентов с саркопеническим ожирением и зрительным дефицитом оказалось ниже в 1,34 раза против группы сравнения. Однако наиболее значимые различия между сопоставляемыми группами установлены по показателю ежедневной двигательной активности вне дома/квартиры, связанной с выполнением покупок, финансовых операций, почтовых отправлений и прогулок на улице (в парках, скверах). При этом различие по вышеназванному критерию физической активности составляло 1,83 раз и имело статистически достоверную значимость (p<0,01).
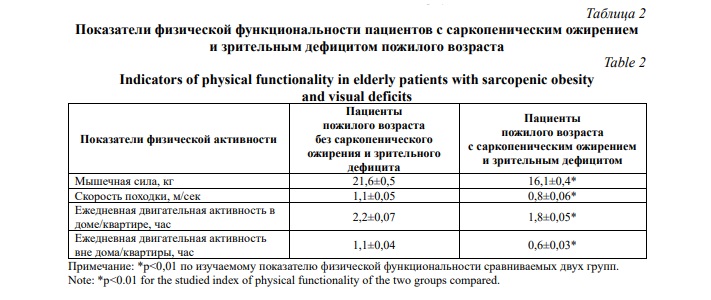
Среди пациентов пожилого возраста с саркопеническим ожирением и зрительным дефицитом статистически значимо ниже скорость походки, что свидетельствует о существенном влиянии исследуемых гериатрических синдромов на физическую функциональность пациентов основной группы. Снижение физической функциональности пациентов пожилого возраста с саркопеническим ожирением и зрительным дефицитом наблюдалось также и по двигательной активности в доме/квартире (p<0,01).
Для выявления ассоциаций параметров физической функциональности пациентов с саркопеническим ожирением и зрительным дефицитом проведен расчет величин отношения шансов, который показал доминирующее воздействие данных гериатрических синдромов на ежедневную двигательную активность вне дома/квартиры (Табл. 3), когда при наличии обсуждаемых дефицитов ежедневная двигательная активность вне дома/квартиры может быть снижена на 31,85%.
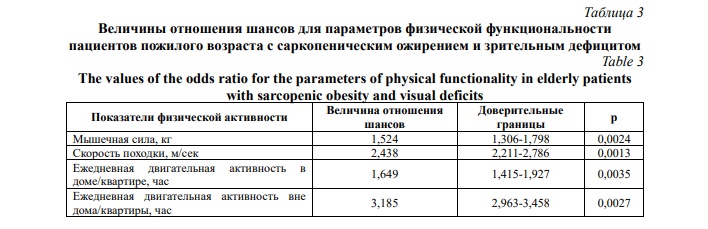
Существенная ассоциация характерна для скорости походки и саркопенического ожирения, сочетанного со зрительным дефицитом пациентов пожилого возраста. На 15,24% повышается вероятность снижения мышечной силы у пожилых пациентов на фоне саркопенческого ожирения и зрительного дефицита. Установлена также ассоциация снижения ежедневной двигательной активности в доме/квартире с саркопеническим ожирением и зрительным дефицитом. Приблизительно аналогичная сила влияния саркопенического ожирения и зрительного дефицита на снижение ежедневной двигательной активности в доме/квартире.
Саркопеническое ожирение в настоящее время среди пожилого населения встречается часто и рассматривается как гериатрический синдром высокого риска, наблюдаемый преимущественно у старшей популяции, подверженной риску синергических осложнений как от саркопении, так и от ожирения [4]. Взрослые в возрасте старше 65 лет составляют 13% мирового населения и являются самой быстрорастущей демографической подгруппой; ожидается, что к 2050 году эта группа достигнет 2,1 миллиарда человек. Среди этой группы населения наблюдается неуклонный рост ожирения и в США 38,5% мужчин и 43,1% женщин в настоящее время страдают ожирением. Во всем мире этот рост, предположительно, компенсировал увеличение продолжительности жизни, при этом ожидаемая продолжительность жизни с поправкой на возраст снизилась примерно на 0,17 года с 2014 по 2015 год [4].
Недостатком при определении точных показателей распространённости саркопенического ожирения является отсутствие единого определения саркопении или ожирения. Анализ восьми определений саркопенического ожирения показал, что показатели в зависимости от пола различаются в 19-26 раз [6]. Анализ показал, что определения саркопении сильно зависят от математических пороговых значений, эталонных групп и определений мышечной массы. Сравнение показателей саркопенического ожирения с использованием биоэлектрического импеданса для определения саркопении и процента жировой ткани для определения ожирения показало, что с возрастом показатели увеличиваются. В другом исследовании авторы выявили людей с ИМТ ≥35 кг/м2 и оценили распространённость саркопенического ожирения для определения жировой ткани у 120 преимущественно взрослых женщин (46,9±11,0 лет). Исследователи сообщили, что показатели варьировались от 0-84,5% у женщин до 0–100% у мужчин в зависимости от применяемого определения [17]. В когорте, сформированной на основе данных Национального обследования состояния здоровья и питания (NHANES) и применяющей вышеупомянутые критерии для оценки мышечной массы, частота саркопенического ожирения составила 12,6% у мужчин и 33,5% у женщин. Частота саркопенического ожирения увеличивалась с возрастом, достигая 48,0% и 27,5% у женщин и мужчин соответственно в возрасте старше 80 лет. В когорте участников Корейского исследования саркопенического ожирения в Южной Корее, продолжающегося эпидемиологического проспективного исследования здоровых добровольцев в возрасте от 20 до 80 лет, распространённость саркопенического ожирения составляла от 1,3 до 15,4% у мужчин и от 0,8 до 22,3% у женщин [6].
Саркопения вызывается сочетанием факторов, в том числе неврологических, связанных с потерей двигательных нейронов, потерей двигательных единиц мышц, эндокринными изменениями и изменениями образа жизни, связанными с малоподвижным образом жизни и плохим питанием [18, 19]. В организме существует динамический баланс между синтезом и распадом мышечных белков. Мышечная гипертрофия возникает, когда синтез белков превышает их распад, а атрофия скелетных мышц возникает, когда распад преобладает над синтезом. Механизмы развития саркопении разнообразны, сложны и до конца не изучены. На развитие саркопении у пожилых людей могут влиять несколько факторов, в том числе гормональный и цитокиновый дисбаланс, возрастное системное воспаление, дисбиоз микробиоты кишечника, нарушения микроциркуляции, метаболические нарушения, преимущественно ожирение и резистентность к инсулину [18]. Физическая активность, связанная с возрастом, а также количественное и качественное недоедание также способствуют этому процессу [19].
Физическая активность, как показало настоящее исследование, снижена у пациентов пожилого возраста с саркопеническим ожирением и зрительным дефицитом по анализируемым параметрам. Впервые установлено наибольшее влияние саркопенического ожирения и зрительного дефицита на ежедневную двигательную активность пациентов вне дома/квартиры. Основной причиной этого, на наш взгляд, является зрительный дефицит, представляющий и усложняющий, прежде всего, передвижение за пределами дома/квартиры.
Показано влияние саркопении, как составной части саркопенического ожирения, на снижение мышечной массы на 58,73% пациентов 50-95 лет (средний возраст 60,82±7,84 года), имеющих нарушение зрения и в 67,55%, имеющих нарушение зрения и депрессию, тогда как среди здоровых людей сниженная мышечная сила встречалась достоверно реже – в 38,03% случаев [20]. На основе этих данных авторами сделано заключение о негативном влиянии зрительного дефицита на развитие саркопении и повышенной распространённости её среди пациентов с зрительным дефицитом.
Эти данные также свидетельствуют о том, что нарушение зрения связано со значительно повышенным риском саркопении у пожилых женщин в Китае. На сегодняшний день существует лишь ограниченное количество исследований взаимосвязи между этими двумя состояниями. В одном крупном поперечном исследовании, в котором приняли участие взрослые в возрасте ≥ 65 лет из 6 стран с низким и средним уровнем дохода, сообщалось о росте распространённости саркопении с увеличением степени нарушения зрения на расстоянии [20]. Некоторые исследователи изучали связь между нарушениями зрения и силой захвата рук, которая тесно связана с диагнозом саркопения [21]. Как пациенты с саркопенией, так и люди с нарушениями зрения, как правило, демонстрируют сниженный уровень физической активности, что потенциально объясняет связь между этими состояниями, а уровень активности еще ниже у лиц с наиболее тяжелыми формами нарушений зрения [21].
Различные исследования подтверждают, что люди с нарушением зрения более склонны иметь физические нарушения [21, 22]. Полученные результаты указывают, что нарушение зрения может быть ранним фактором, определяющим начало и/или ухудшение физической активности у пожилых людей с саркопенией [22]. Связь между нарушением зрения и саркопенией у пожилых оказалась значимой даже после корректировки нескольких факторов – относительный риск составил 2,66 (95% доверительный интервал 1,29-5,48) [22]. Обнаружено, что самооценка нарушения зрения, хотя и подвержена некоторой предвзятости, особенно со стороны респондента со склонностью преувеличивать симптомы, независимо связана с саркопенией.
Неясно, какие основные механизмы лежат в основе связи между нарушением зрения и качеством физической функции [23]. Считается, что эта связь обусловлена тем, что люди с нарушением зрения, как правило, менее подвижны, чем люди без нарушений. Действительно, люди с нарушением зрения медленнее передвигаются и, следовательно, менее физически активны. Например, сообщалось, что нарушение зрения чаще всего приводит к замедлению движений, упадку сил, низкой физической активности и синдрому старческой астении. Какой бы ни была причина, недостаток физической активности может привести к снижению мышечной силы, подвергая человека большему риску саркопении [24].
В большинстве стран Африки к югу от Сахары нет учреждений для пожилых людей, находящихся на иждивении, и они представляют собой серьёзную ежедневную обузу для своих семей. Кроме того, в клинической практике нарушение зрения может быть ранним индикатором или предупреждающим признаком физических нарушений. Поскольку нарушения зрения чаще всего возникают из-за аномалий рефракции, коррекция аномалий рефракции может предотвратить или замедлить процесс разрушения, связанный с ослаблением организма [25]. Эти данные, по-видимому, свидетельствуют о том, что было бы важно проводить мероприятия по охране здоровья населения для раннего выявления и коррекции нарушений рефракции у пожилых людей, чтобы снизить риск возникновения у них физических нарушений или прогрессирования до состояния зависимости. Даже после коррекции зрения она по-прежнему была связана с саркопенией. Это может быть связано с двумя гипотезами: коррекция могла быть проведена неправильно или коррекция могла быть проведена после начала саркопении.
Вместе с тем слабой стороной этого исследования следует назвать оценку зрения путём опроса участников исследования о том, могут ли они чётко видеть в повседневной жизни, используя максимально скорректированное зрение. Возможные ответы включали: хорошее зрение практически не влияет на повседневную жизнь, например, можно чётко видеть телевизор или зрение лучше, чем раньше; плохое зрение негативно влияет на повседневную жизнь, например, можно видеть только общие очертания людей или хуже. В отличие от этого исследования нами выполнена объективная оценка зрительного дефицита с использованием различных офтальмологических методов и изучено влияние объективных параметров зрительного дефицита на формирование саркопенического ожирения – более сложного и тяжёлого гериатрического синдрома, чем саркопения.
Влияние саркопенического ожирения без оценки состояния зрения на мышечную силу показано в исследовании [26], согласно которому, показатель кистевой динамометрии был снижен до 15,4 кг относительно 23,4 кг у здоровых женщин 69-73 лет. При этом указанное снижение мышечной силы у пациентов с саркопеническим ожирением без учёта состояния зрения оказалось практически эквивалентным установленной нами величине одноимённого показателя у пожилых пациентов с саркопеническим ожирением и зрительным дефицитом без значимых различий.
Наши результаты показали высокую ассоциацию нарушения зрения с ежедневной двигательной активностью вне дома/квартиры, мышечной силой, но механизм посредством которого зрение и мышечная масса связаны между собой, до сих пор не ясен. Зрение также играет важную роль в контроле равновесия. Острота зрения предоставляет нервной системе обновлённую информацию о положении и движениях тела по отношению друг к другу и к окружающей среде [27]. Согласно предыдущему исследованию, в котором оценивались участники с дефектами центрального поля зрения, за которыми следовала возрастная дегенерация жёлтого пятна, зрение способствовало стабилизации позы, поскольку участники с ослабленным зрением испытывали трудности с поддержанием позы по сравнению с участниками с нормальным зрением. Способность ходить, не падая, зависит от интеграции множества компонентов, отвечающих за равновесие и походку. У пожилых людей с плохим зрением может нарушаться походка, и скорость их ходьбы снижается. Участники с возрастной острой макулопатией ходили медленнее и дольше раскачивались, проявляя высокую степень осторожности, по сравнению со здоровыми людьми из контрольной группы. Кроме того, изменения в равновесии и походке могут негативно влиять на уровень активности пожилых людей, усугубляя циклический характер физического старения [27].
Предыдущее когортное исследование показало, что ухудшение зрения влияет на функциональное состояние и самочувствие (измеряемое с помощью опросника об ограничениях физических функций), мешает социальной активности и вызывает нервозность, а также подавленное настроение. В частности, взрослые люди с ухудшением зрения сталкиваются с ограничениями в повседневной жизни из-за проблем со здоровьем [27]. Пожилые люди с плохим зрением могут испытывать трудности в общении в социальных сетях и реже заниматься досугом. Следовательно, чем менее физически активным становится человек, тем выше вероятность того, что его мышечная масса постепенно будет уменьшаться.
Нарушение остроты зрения – распространённое явление среди пожилых людей. Плохое зрение, которое многие пожилые люди воспринимают как должное, тесно связано с гериатрическим синдромом [27]. У пожилых людей хорошо известна взаимосвязь между снижением остроты зрения и повышенной частотой падений. Снижение зрительной активности является важным фактором риска падений и тесно связано с тенденцией к многократным падениям. Кроме того, у пожилых пациентов с сахарным диабетом нарушение зрения независимо связано с функциональными нарушениями. Снижение зрительных функций связано с ослаблением организма, которое можно оценить по скорости ходьбы, силе хвата, пиковой скорости выдоха и способности вставать со стула без опоры на руки. Согласно исследованию, проведенному в Китае с участием 2476 человек в возрасте 50-74 лет с функциональной пресбиопией, острота зрения вблизи положительно коррелировала с силой хвата. Более того, предыдущее обсервационное исследование, в котором оценивалась сила и мощность нижних конечностей, показало, что по сравнению с группой с нарушениями зрения у участников с нормальным зрением, сопоставимых по возрасту и полу, были значительно более высокие значения пикового крутящего момента и средней мощности в подколенных сухожилиях и четырёхглавых мышцах бедра [27]. Следовательно, ухудшение зрения у пожилых людей, вероятно, связано со снижением мышечной силы.
Среди пациентов старше 65 лет, проживающих в обществе, и страдающих саркопений и нарушением зрения средняя мышечная сила была на 1,1 кг ниже (17,47±0,5 кг), чем у женщин без нарушения зрения – 18,59±0,3 кг (p<0,05) [28]. Однако в отдельных публикациях [29, 30] сообщается об отсутствии значимой связи между снижением остроты зрения и мышечной силой у пациентов с саркопенией. Так, указанная ассоциация по величине отношения шансов оказалась слабой, составив -0,5 (95% доверительный интервал от -1,4 до 0,3; p<0,05) [29]. Никакой существенной связи не было обнаружено между снижением зрения и мышечной силой у пожилых с саркопенией, на что указывает отношение шансов, составившее 1,33 (95% доверительный интервал 0,83-2,13; p>0,05) [30].
Снижение мышечной силы, скорости походки ассоциировано с уменьшением общей двигательной активности среди пожилых пациентов с саркопеническим ожирением и зрительным дефицитом, установленное нами в данной работе, служит одной из причин снижения инструментальной активности в повседневной жизни [9]. Показано, что саркопеническое ожирение и возрастная макулярная дегенерация в большей степени снижают инструментальную повседневную активность (М=4,72±0,07 балла), чем только саркопеническое ожирение (М=5,91±0,09 балла) (p<0,001). Наибольшие различия между группами в ухудшении инструментальных действий наблюдали по таким видам, как совершение телефонных звонков – 0,57±0,05 балла у пациентов с саркопеническим ожирением и возрастной макулярной дегенерацией, 0,89±0,07 балла – у пациентов с саркопеническим ожирением – в 1,56 раза (p<0,001), совершение покупок – 0,62±0,06 и 0,76±0,08 балла (p<0,01), ведение финансовой деятельности – 0,48±0,05 и 0,61±0,04 балла (p<0,001) соответственно. По указанным ограничениям пациенты с саркопеническим ожирением и возрастной макулярной дегенерацией нуждаются в посторонней помощи.
Саркопеническое ожирение ухудшает выполнение действий, связанных с инструментальной активностью в повседневной жизни, и снижает их автономию [31]. Увеличению ограничений инструментальной активности в повседневной жизни у пациентов с саркопеническим ожирением может способствовать нарушение зрения, приводящее к формированию высокой (выраженной) зависимости от посторонних [31]. Однако как свидетельствует анализ отечественных и зарубежных публикаций на сегодняшний день проведено лишь ограниченное количество исследований взаимосвязи между этими двумя состояниями. Факторами, потенциально связывающими эти два состояния, могут быть окислительный стресс, хроническое воспаление , митохондриальная дисфункция и митохондриальные нарушения, обусловленные возрастными изменениям состава тела, за которые отвечают многочисленные факторы [12].
Так, количество жира в организме увеличивается до седьмого десятилетия жизни, а затем уменьшается. Сжатие позвонков приводит к уменьшению роста, что влияет на антропометрические показатели, такие как индекс массы тела. Мышечная масса снижается после пика, достигнутого в четвёртом десятилетии, так что вес в основном набирается за счёт жира, а не мышечной массы. Это возрастное снижение мышечной массы отчасти объясняет снижение скорости метаболизма в состоянии покоя. К другим этиологическим факторам, вызывающим снижение скорости метаболизма в состоянии покоя, относятся снижение физической активности, уменьшение объёма митохондрий и снижение окислительной способности. Возрастное снижение компонентов общего расхода энергии (таких как скорость метаболизма в состоянии покоя, термическое воздействие пищи и физическая активность) в значительной степени способствует постепенному увеличению количества жира в организме [12, 32].
При саркопеническом ожирении у пожилых ожирение активирует макрофаги, тучные клетки и Т-лимфоциты, вызывая низкоуровневое воспаление, которое приводит к секреции фактора некроза опухоли, лептина и гормона роста. Все эти изменения в секреции приводят к резистентности к инсулину, которая усиливается из-за катаболизма мышц, способствуя увеличению жировой массы и потере мышечной массы. Лептин усиливает выработку провоспалительных цитокинов IL-6 и TNF, что приводит к снижению анаболического действия инсулиноподобного фактора роста 1. Такое снижение, наряду с возрастным снижением уровня тестостерона, повышает вероятность развития старческой астении. Повышенный уровень цитокинов, наблюдаемый при гипогонадизме, связан с абдоминальным ожирением, которое усугубляет развитие саркопении. Адипонектин отрицательно коррелирует с возрастом и ожирением и противодействует эффектам лептина. Повышенный уровень TNF напрямую подавляет адипонектин, останавливая синтез мышечного белка и митохондриальные процессы. Ожирение также вызывает резистентность к лептину, способствуя снижению окисления жиров в мышцах и отложению жира в нетипичных местах [8].
Несмотря на неоднозначность и недостаточную изученность рассмотренных механизмов развития саркопенического ожирения, в том числе у пациентов пожилого возраста со зрительным дефицитом, установленным и доказанным последствием влияния саркопенического ожирения и зрительного дефицита, выявленного нами, является снижение физической функциональности таких пациентов. Поэтому, наряду с коррекцией зрительного дефицита, важным методом профилактики и замедления прогрессирования возрастного саркопенического ожирения является физическая активность [8, 33]. Значение физических упражнений для пациентов с саркопеническим ожирением подчёркивается Всемирной организацией здравоохранения в опубликованных рекомендациях по комплексной стратегии ухода за пожилыми людьми (ICOPE), информирующее врачей и исследователей о внутренней среде пожилого населения, предлагая оценку пяти областей: жизнеспособность, локомоторная, слуховая функция, зрительная функция, когнитивная функция и психологическая. Эти рекомендации поощряют комплексный взгляд на различные физические и физиологические характеристики, а также их изменения в процессе старения [34]. Данные рекомендации могут быть полезны для комплексной оценки пожилых женщин, особенно в контексте ожирения, саркопении и саркопенического ожирения. Это указывает на то, что пожилые люди с более высоким процентом жира в организме и более низкой функциональной физической работоспособностью также имеют худшую специфическую мышечную силу, что предполагает состояние саркопенического ожирения. Кроме того, когда саркопения сочетается с ожирением, у пожилых женщин наблюдается более низкая физическая работоспособность и удельная мышечная сила, показатели более выраженных метаболических осложнений, худшая функциональная независимость [35].
Заключение. Саркопеническое ожирение в сочетании со зрительным дефицитом в пожилом возрасте статически значимо ухудшает параметры физической функциональности. При этом наиболее существенно среди них снижена ежедневная двигательная активность вне дома/квартиры до 0,6±0,03 часов против 1,1±0,04 часов среди пациентов аналогичного возраста с отсутствием саркопенического ожирения и зрительного дефицита.
У пациентов 60-74 лет с саркопеническим ожирением и зрительным дефицитом установлено также снижение мышечной силы и скорости походки с достоверным различием к группе сравнения. Формирование саркопенического ожирения у пожилых со зрительным дефицитом в наибольшей степени ассоциировано с ежедневной двигательной активностью вне дома/квартиры, что указывает на необходимость социальной поддержки и реализации геронтологических мероприятий по улучшению двигательной активности таких пациентов.
Информация о финансировании
Финансирование данной работы не проводилось.





















Список литературы