Особенности кишечного микробиома у лиц с повышенной тревожностью
Aннотация
Актуальность: Тревога и тревожные расстройства являются одними из наиболее распространенных психических заболеваний во всем мире. Появляется все больше доказательств того, что микробиом кишечника играет определенную роль в развитии психических расстройств. Установлено, что кишечник человека содержит вторую по величине концентрацию нейронов после головного мозга, и он связан с ним двунаправленной «осью связи микробиом-кишечник-мозг». Цель исследования:Провести сравнительную оценку состава кишечной микробиоты между группами лиц, отмечавших у себя наличие повышенной тревожности с высоким баллом по опроснику Спилбергера-Ханина, с группой лиц, не отмечавших у себя наличие повышенной тревожности с низким или умеренным баллом по опроснику Спилбергера-Ханина, проживающих в европейской части России c последующим построением прогностической модели такого риска. Материалы и методы:В исследовании приняли участие 28 мужчин (средний возраст 37,5 лет) и 91 женщина (средний возраст 38 лет). Для оценки уровня тревожности использовали опросник Спилбергера-Ханина и анкетирование. Опытная группа составила 49 человек, группа контроля – 70. Выявление таксономического состава кишечной микробиоты проводили методом секвенирования генов бактериальной 16S рРНК с последующим биоинформатическим анализом. Статистическую обработку результатов исследования проводили с помощью линейного дискриминантного (LEfSe) анализа и критерия Уилкоксона. Для построения прогностической модели был использован метод линейной регрессии с вычислением показателя AuRoc. Результаты:Нами были получены значимые различия между опытной и контрольной группами на уровне типов, классов и родов бактерий. В опытной группе были повышены Actinobacteriota (p=0,008), Actinobacteria (p=0,014), Bifidobacterium (p=0,011), Subdoligranulum (p=0,031),Lachnospira (p=0,008), CAG_873 (p=0,014), Roseburia (p=0,019), Lactonifactor (p=0,02), Erisibelotrichacee UGG_003 (p=0,002), Eggerthella (p=0,021) и снижены Lactobacillus (p=0,030), Rothia (p=0,047),Caprociproducens (p=0,030), Desulfovibrio (p=0,041), Caprobacter (p=0,037). Расчетный показатель прогностической модели AuRoc составил 0,755. Заключение:Использование метода секвенирования генов 16S рРНК позволяет выявить особенности микробиома у лиц с повышенной тревожностью. Полученные данные могут быть полезны для понимания механизмов развития и коррекции данного состояния, а наличие тех или иных бактериальных таксонов может быть использовано в качестве маркеров при прогнозировании повышенной тревожности
Ключевые слова: личностная тревожность, тревога, микробиом, микробиом кишечника, 16S рРНК секвенирование, бифидобактерии, лактобактерии
Введение. Тревожные расстройства относятся к числу самых частых психических нарушений с высокой распространенностью во всем мире, для которых характерен рост в период социальных потрясений [1]. Во время эпидемии COVID-19 число людей, которые страдают депрессией и тревожностью, увеличилось на 25% [2]. Показано, что повышенная тревожность является фактором риска развития психосоматической патологии и других психических нарушений [3]. В состоянии тревоги происходит увеличение нагрузки на сердечно-сосудистую систему, а также угнетение работы пищеварительной системы [4]. Современные исследования показывают, что тревожные расстройства возникают под влиянием генетических, нейробиологический, эндокринных, социальных и психологических факторов [5].
Тревога и депрессия имеют высокую степень коморбидности и схожие соматовегетативные проявления, что в случаях сочетания тревожных и депрессивных симптомов усложняет раннюю диагностику [6]. В связи с этим, описание патогенеза двух состояний отдельно друг от друга становится достаточно сложной задачей [7]. Множество вопросов, касающихся диагностики, терапии и профилактики этих состояний остаются неизученными и требуют дальнейших исследований в области патофизиологии и этиологии депрессии и тревожности [8].
Изучение кишечной микробиоты имеют большой потенциал для практического использования в области профилактики и диагностики психических заболеваний. В особенности, такие исследования могут оказаться полезными в терапии депрессии и тревожных расстройств [9]. Кишечная микробиота связана как с гастроэнтерологическими заболеваниями, так и с психическими расстройствами, посредством двунаправленной связи, описываемой как «ось микробиом-кишечник-мозг» [10].
Совокупный вес всех микроорганизмов, населяющих человеческий организм составляет около 3-5 % от общего веса человека, причем их большая часть расположена в кишечнике, что позволяет рассматривать микробиом как отдельный орган [11]. Для установления состава микрофлоры используются различные методы. Метод, основанный на анализе последовательностей гена 16S рибосомальной РНК, обладает значительно большей информативностью, так как выявляет в том числе и некультивируемые виды бактерий [12].
Традиционно этиология тревоги фокусировалась на генетических факторах, но имеются данные, указывающие на то, что кишечная микробиота и ее метаболиты тесно связаны с центральной нервной системой хозяина посредством двунаправленной связи.
Несколько экспериментальных исследований показали, что потенциальные изменения в бактериальной экосистеме кишечника, известные как дисбиоз, и последующие хронические воспалительные процессы, могут влиять на начало расстройств настроения [13]. Кишечная микробиота тесно связана со здоровьем человека, включая иммунный ответ, пищеварительную функцию и передачу нервных импульсов [14]. Депрессия и тревога часто сопровождаются изменениями в состав кишечной микробиоты, что показано в результатах мата-анализа [15]. Кроме этого, выявлены бактериальные маркеры, характерные для пациентов с депрессией и тревожным расстройством [16]. Связь состава кишечных бактерий с повышенной тревожностью у человека имеет и другие убедительные доказательства. Как показано в исследовании Mason et al, снижение Bacteroides характерно для лиц с тревогой, а снижение Clostridia для лиц с депрессией [17]. Снижение Gemmiger, Ruminococcus, andVeillonella было показано для лиц с депрессией и тревогой [18]. При большой депрессии наблюдается снижение Bacteroidetes, Actinobacteria и Firmicutes [19].
До настоящего времени в России аналогичные работы не проводили. Учитывая то, что состав микробиома различается у представителей разных этнических групп [20] и существуют определенные национальные предпочтения тех или иных народов в выборе индивидуального питания и терапии, проведение подобного исследования в Российской Федерации представляется важным, что и определяет цель настоящего исследования как поиск маркеров повышенной тревожности посредством исследования особенностей состава кишечной микробиоты.
Цель исследования. Провести сравнительную оценку состава кишечной микробиоты между группами лиц, отмечавших у себя наличие повышенной тревожности с высоким баллом по опроснику Спилбергера-Ханина, с группой лиц, не отмечавших у себя наличие повышенной тревожности, с низким или умеренным баллом по опроснику Спилбергера-Ханина, проживающих в европейской части России c последующим построением прогностической модели такого риска.
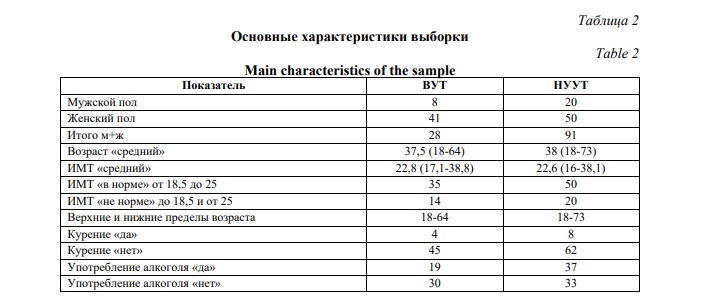
Материалы и методы исследования. В исследовании приняли участие 119 человек, 28 мужчин (от 18 до 64 лет, средний возраст 37,5 лет) и 91 женщина (от 18 до 73 лет, средний возраст 38 лет). Протокол исследования был одобрен этическим комитетом Санкт-Петербургского государственного университета №02-258 (РК115-03-20 от 23.11.2023). Уровень личностной тревожности устанавливался при помощи опросника Спилбергера-Ханина [21], а также при помощи анкетирования, в котором участники могли отметить у себя наличие повышенной тревожности (структура анкеты приведена в Таблице 1). Общая выборка была разделена на две группы. Опытная группа – лица, которые имели высокий балл личностной тревожности по опроснику и отмечали в анкете наличие повышенной тревожности (ВУТ-высокий уровень тревожности) (49 человек). Контрольная группа – лица, которые имели умеренный или низкий балл по психологическому опроснику и не отмечали у себя наличие повышенной тревожности (НУУТ-нормальный или умеренный уровень тревожности) (70 человек). Лица, имеющие высокий балл по опроснику, но не указавшие в анкете наличие повышенной тревожности, а также лица, имеющие низкий балл по опроснику, но указавшие наличие повышенной тревожности в анкете не были включены в исследование. Все испытуемые указывали в анкете, особенности питания, место проживания, длину и массу тела, статус курения и употребления алкоголя. Все испытуемые проживали на территории европейской части России в городской местности, исключали у себя наличие профессиональной вредности и прием лекарственных препаратов на постоянной основе. Из них русских – 110 человек, 9 человек других национальностей (татар – 3, башкир – 2, мордвинец – 2, грузин – 1, украинец – 1). Преимущественно всеядные (110 человек, 2 вегетарианца, 7 человек придерживались безглютеновой и безмолочной диеты). Испытуемые исключали использование пробиотиков и антидепрессантов в течение двух недель и антибиотиков в течение 6 месяцев до сдачи анализов. Так же от всех участников было получено добровольное информированное согласие на участие в исследовании.

Исследование образцов проводилось с декабря 2023 по апрель 2024 года. Забор кала производился пациентами самостоятельно на дому, используя прилагаемый набор для сбора биоматериала, который включал стерильный зонд – 2 шт., стерильные пробирки типа Eppendorf с 0,5 мл транспортной среды с муколитическим веществом на основе EDTA (ИнтерЛабСервис, Москва, Россия). Средняя объем образцов, не превышал 0,5 мл. Транспортировка биологических образцов заняла от 1 до 2 суток при температуре 4 °C с последующей процедурой выделения ДНК. Аликвоты ДНК были заморожены при температуре -80 °C для последующего хранения.
Общую ДНК выделяли из образцов суспензии кала, подвергнутых гомогенизации в лизирующем растворе, гомогенизированным методом гранулирования, с последующей экстракцией ДНК методом сорбционной колонки (Qiagen, Джермантаун, Мэриленд, США) в соответствии с рекомендациями производителя.
Библиотеки секвенирования 16S рРНК были подготовлены в соответствии с протоколом подготовки библиотеки 16S метагеномного секвенирования согласно протоколу Illumina (Illumina, Сан-Диего, Калифорния, США) (Part #15044223 Rev. B). Было использовано 5 нг. общей ДНК на образец, чтобы амплифицировать целевой фрагмент гена 16S рРНК с помощью рекомендуемых праймеров для региона V3–V4. Было проведено 25 циклов ПЦР с использованием KAPA HiFi HotStart ReadyMix (2×) (Roche Diagnostics, Цуг, Швейцария). После очистки продуктов ПЦР с помощью SPRI bins было проиндексировано 5 нг. полученных ампликонов с помощью KAPA HiFi HotStart ReadyMix (2×) (Roche Diagnostics, Цуг, Швейцария) и набора Nextera XT Index Kit (Illumina, Сан-Диего, Калифорния, США). Далее проводили 8 циклов индексной ПЦР в соответствии с протоколом Illumina. Полученные библиотеки были секвенированы с использованием платформы Illumina MiSeq.
Исследование кала пациентов методом секвенирования 16S рРНК проводились на базе Центра геномных технологий «Сербалаб» (Россия, Санкт-Петербург). Разработка и адаптация методики секвенирования проводилась совместно с Научно-Исследовательским институтом акушерства, гинекологии и репродуктологии им. Д.О. Отта. Статистическая обработка результатов проводилась совместно с Научно-исследовательским институтом акушерства, гинекологии и репродуктологии им. Д.О. Отта и Национальным исследовательским университетом ИТМО г. Санкт-Петербург.
Для статистической обработки полученных данных использовались следующие методы: для определения родов бактерий, которые были повышены или понижены у лиц с ВУТ, был использован метод линейного дискриминантного анализа размера эффекта (LEfSe) в составе программного комплекса QIIME 2 [22, 23]. Пороговое значение LDA score (log 10) больше 2 по модулю было установлено для определения статистически значимых различий в составе микробиома. Для проверки статистической значимости различий в составе кишечного микробиома между группами использовался критерий Уилкоксона (W). Значения p менее уровня значимости (p<0,05) считались статистически значимыми. Кроме этого, для оценки модели предсказывания развития ВУТ по анализу микробиоты была построена модель AuRoc методом регрессионного анализа. Взаимосвязь между уровнем тревожности и другими параметрами выборки определялась при помощи теста Хи-квадрат с поправкой Йейтса.
Результаты и их обсуждение. При выполнении настоящей работы нами было осуществлено секвенирование гена 16S рРНК бактериальной ДНК, выделенной из кала у 119 испытуемых, из которых 49 были определены в опытную группу ВУТ и 70 находились в контрольной группе НУУТ. Взаимосвязи исследуемого признака с другими показателями выборки, такими как пол (р=0,184), ИМТ (р=0,837), курение (р=0,785) или употребление алкоголя (p=0,185) выявлено не было.
Секвенирование всех образцов проводили в рамках одного запуска для исключения факторов лабораторного процесса и процесса обработки данных на вариативность полученных результатов. Все полученные нами в результате NGS секвенирования данные соответствовали критериям контроля качества, а именно имели не менее 10 000 прочтений на образец. Все образцы, содержащие менее 10 000 прочтений, были удалены из анализа, в соответствии с протоколом [24].
Сравнение таксономического разнообразия микробиоты кишечника у опытной и контрольной группы проводили после биоинформатической обработки полученных данных методом линейного дискриминантного анализа размера эффекта (LEfSe). В результате анализа были выявлены статистически значимые отличия на уровне типов, классов и родов. Так, тип (Phyla) Actinobacteriota (p=0,008) и класс (Class) Actinobacteria (p=0,014) были достоверно повышены в опытной группе. Установленный факт свидетельствует лишь об отличии между группами, но не позволяет нам сделать вывод об отличии количества данных бактерий в опытной группе в сравнении с нормой, ввиду отсутствия референсных баз данных нормофлоры.
В рамках настоящего исследования нами так же были найдены статистические значимые отличия на уровне родов (genus). Для пациентов с ВУТ характерно повышение содержания бактерий 8 родов, таких как Bifidobacterium (p=0,011), Subdoligranulum (p=0,031), Lachnospira (p=0,008), CAG_873 (p=0,014), Roseburia (p=0,019), Lactonifactor (p=0,02), ErisibelotrichaceeUGG_003 (p=0,002), Eggerthella (p=0,021). Для группы НУУТ, напротив, характерно преобладание количества 5 родов, таких как Lactobacillus (p=0,030), Rothia (p=0,047), Caprociproducens (p=0,030), Desulfovibrio (p=0,041), Caprobacter (p=0,037). Результаты линейного дискриминантного (LEfSe) анализа отличий в микробиоте на уровне родов представлены на Рисунке 1. Распределения представленностей таксонов в значимых классах бактерий – на Рисунке 2. Результаты обработки данных с помощью критерия Уилкоксона приведены в Таблице 3.
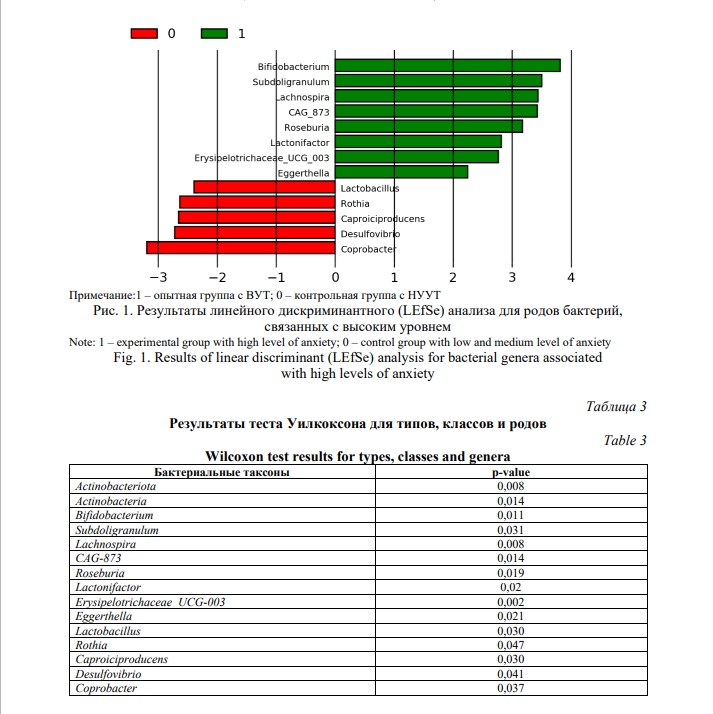
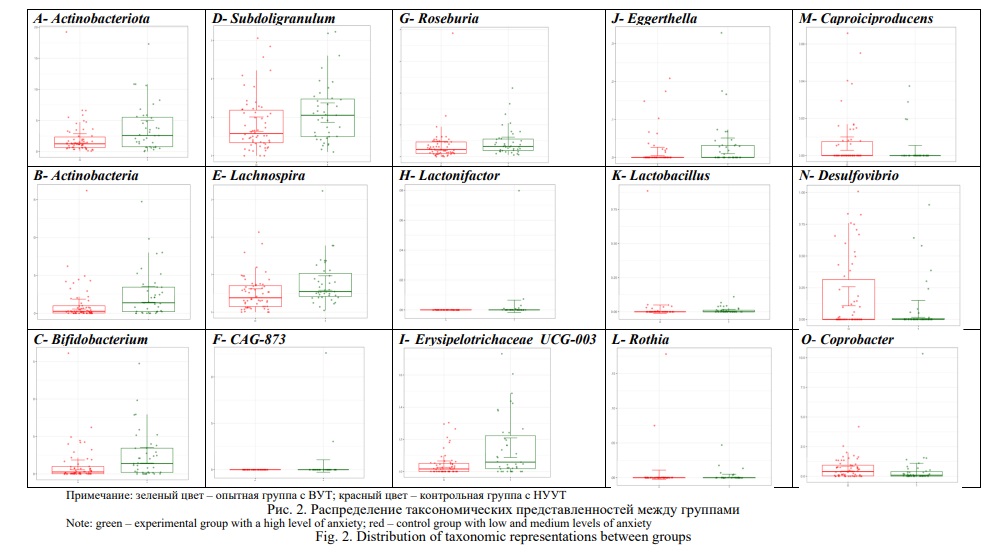
В рамках проведенного исследования большинство полученных нами данных согласуется с результатами других авторов. Так, было показано, что большинство родов, специфичных для пациентов с большой депрессией относилось к типу Actinobacteriota. [25]. Помимо этого, недавнее исследование продемонстрировало, что у лиц, страдающих депрессией, отмечается повышенное содержание Actinobacteria, что коррелирует с нашими данными о росте этого класса микроорганизмов в опытной группе [26].
При сравнении бактериального разнообразия между контрольной и опытной группой на уровне родов, мы получили противоречивые результаты. Так, род Bifidobacterium считается пробиотическим. Тем не менее в нашей работе повышение данного рода было характерно для лиц, страдающих высокой тревожностью с симптомами депрессии. В исследовании Durantietal., было использовано метагеномное секвенирование, которое выявило четкую корреляцию с повышенным содержанием Bifidobacteriumadolescentis у детей с субклиническими симптомами тревоги и депрессии. Авторами показано, что данный микроорганизм, как и другие виды Bifidobacterium являются основными продуцентами ГАМК в кишечнике [27]. Как известно, ГАМК является основным тормозящим нейромедиатором, и нарушения метаболизма ГАМК связаны с тревогой и депрессией [28]. Таким образом, Bifidobacterium может изменять концентрацию ГАМК, влияя на ось кишечник-мозг.
Как показано в недавнем исследование, род Subdoligranulu показал ассоциацию с симптомами депрессии, что согласуется с полученными нами данными [29]. Об этой связи говорят и более ранние исследования [30]. Lachnospira была снижена у пациентов с тревогой/депрессией и язвенным колитом [31], хотя в нашем исследовании данная бактерия оказалась повышенной в опытной группе. Обилие Roseburia наблюдалось в группе пациентов с подростковой депрессией, что согласуется с полученными нами данными [32]. Представители Erysipelotrichaceae были связаны с воспалением и дисбиозом, но не показали корреляции с депрессией или тревогой [33].
Относительно бактерий CAG-873 и Lactonifactor,Caproiciproducens в контексте интересующей нас проблематики информации найти не удалось.
Род Eggerthella, бактерии типа Actinomycetota, так же ассоциированы с тревогой и депрессией [29, 15]. Полученное повышение данного рода в нашей работе согласуется с результатами многих исследований. В проведенном Nikolova и соавт. мета-анализе авторы отмечают, что Eggerthella была повышена в 10 из 11 исследований, посвященных биполярному расстройству, психозу, тревоге и депрессии. Eggerthella связана с воспалением желудочно-кишечного тракта [15]. Так же показано повышение данного рода при большой депрессии [34].
В нашей работе повышение таких бактерий как Lactobacillus, Rothia, Caproiciproducens, Desulfovibrio, Coprobacter было характерно для контрольной группы без наличия тревоги или депрессии. Соответственно, данные бактерии снижены в опытной группе.
Имеется достаточного много доказательств того, что прием пробиотиков, содержащих Lactobacillus значительно снижает симптомы депрессии и тревоги [35, 36] и др. В данном исследовании род Lactobacillus был снижен в опытной группе. Таким образом, можно предположить, что снижение данного рода имеет отношение к патофизиологии тревожности.
У пациентов с большим депрессивным расстройством было выявлено уменьшение рода Rothia, но после лечения антидепрессантами численность была увеличена [37]. В нашем исследовании род Rothia был снижен в опытной группе, по сравнению с контрольной группой.
Повышение количества Desulfovibrio характерно при болезни Паркинсона [38], Desulfovibrio vulgaris был повышен при большой депрессии [34]. Однако в некоторых исследованиях показано и их снижение при психических нарушениях, как и в нашей работе. Кроме этого, данный род был повышен у пациентов с депрессией и язвенным колитом [39].
Относительно рода Coprobacter в исследовании Gonzalez-Mercado etal, была выявлена отрицательная корреляция с симптомами депрессии, как и в нашем исследовании относительно тревоги [40].
Для оценки прогностической значимости полученных данных для наиболее описанных в литературе бактерий, нами была построена модель AuRoc методом линейного регрессионного анализа. Для этого сначала была найдена «точка отсечения» для каждого рода, выявленного в результате проведения линейного дискриминантного (LEfSe) анализа. Значения больше «точки отсечения» для бактерий, ассоциированных с опытной группой, а также значения меньше «точки отсечения» для бактерий, ассоциированных с контрольной группой, рассматривались как факторы риска. Факторы риска и «точки отсечения» по бактериальным маркерам представлены в Таблице 4. ROC кривая модели показана на Рисунке 3. Основные ее характеристики приведены в Таблице 5. В частности, были отражены такие показатели как чувствительность, специфичность, эффективность, прогнозная ценность положительного результата, прогнозная ценность отрицательного результата, которые составили 91,67%, 53,06%, 72,36%, 58,93% и 89,66%, соответственно. Показатель AuROC составил 0,755.
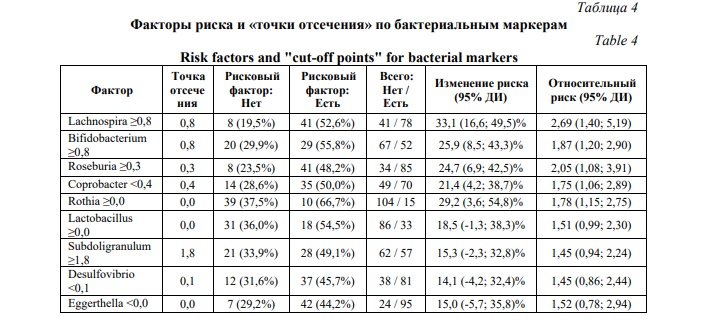
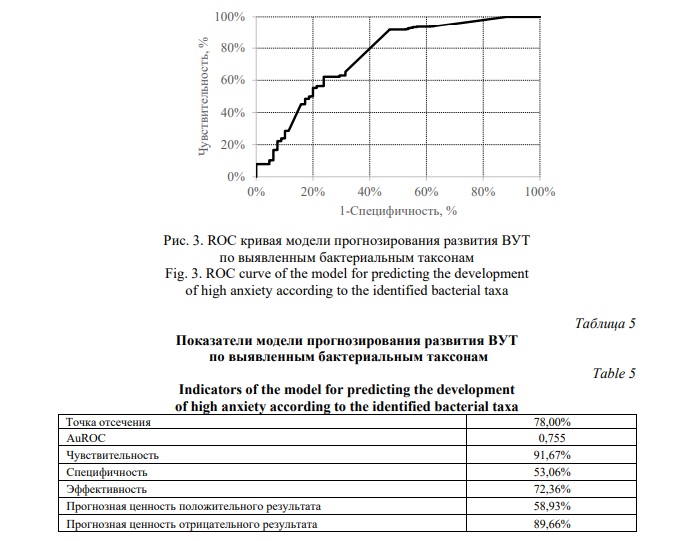
Таким образом, построенная модель линейной регрессии показывает возможность использования выявленных в результате линейного дискриминантного анализа бактериальных таксонов как прогностических маркеров в диагностике и предсказании рисков развития повышенной тревожности.
Ограничением настоящего исследования является отсутствие проверки данных 16S рРНК секвенирования в более крупной выборке с исключением других психических нарушений. Несмотря на это, наше исследование подтверждает имеющиеся данные о том, что бактерии кишечника могут участвовать в психоэмоциональных процессах в организме человека.
Заключение. На сегодняшний день имеется множество доказательств существования двунаправленной связи между кишечником и мозгом, что подтверждается и в настоящем исследовании. В данной работе мы использовали метод секвенирования генов 16S рРНК и выявили статистически значимые различия в микробиоте лиц с ВУТ. Большая часть полученных результатов, а именно повышение Actinobacteriota, Actinobacteria, Subdoligranulu, Eggerthella, Roseburia и снижение Lactobacillus, Rothia, Caprociproducens, Desulfovibrio, Caprobacter в группе лиц с ВУТ согласуется с литературными данными. В отношении бактерий Bifidobacterium, Lachnospira, Erysipelotrichaceae нами были получены противоречивые результаты, что требует дальнейшего изучения. Значимые ассоциации были получены также для родов CAG-873 и Lactonifactor,Caproiciproducens, но информации, относительно их связи с психическими нарушениями найти не удалось.
Полученные данные позволили нам построить модель прогнозирования риска развития повышенной тревожности по микробиомным маркерам, которая обладает высокой чувствительностью, в тоже время ее специфичность недостаточная. Проведенное исследование подтверждают тот факт, что кишечный микробиом, выступает перспективным объектом изучения и имеет предпосылки для терапевтического влияния при патологической тревожности. Требуются дополнительные исследования для изучения роли выявленных бактериальных маркеров в патогенезе депрессии и других, связанных с тревогой, психических нарушений.
Информация о финансировании
Финансирование данной работы не проводилось.





















Список литературы