Современные достижения генной терапии пигментного ретинита с применением аденоассоциированного вируса (обзор)
Aннотация
Актуальность: Пигментный ретинит представляет собой группу наследственных заболеваний сетчатки, характеризующихся прогрессирующей дегенерацией фоторецепторов и пигментного эпителия. Это приводит к необратимой потере зрения, что существенно снижает качество жизни пациентов. Современные методы лечения, включая витаминную терапию, антиоксиданты и имплантацию электронных устройств, не способны остановить прогрессирование заболевания, а лишь частично компенсируют его последствия. В связи с этим разработка эффективных методов лечения, направленных на устранение первопричины заболевания, остается актуальной задачей современной офтальмологии. Генетическая терапия с использованием вирусных векторов открывает новые перспективы в лечении наследственных дегенеративных заболеваний сетчатки. Цель исследования:Обзор современных подходов к лечению пигментного ретинита с использованием генетической терапии, анализ эффективности и безопасности доставки терапевтических генов в клетки сетчатки, а также оценка перспектив дальнейших исследований в данной области. Материалы и методы:Проведен анализ данных научных исследований и клинических испытаний, посвященных использованию аденоассоциированных вирусов для доставки генетического материала в клетки сетчатки. Поиск источников осуществлялся в базах данных рецензируемой литературы по ключевым словам, связанным с генетической терапией пигментного ретинита. Результаты:Эффективность генной терапии при пигментном ретините зависит от серотипа AAV-вектора, типа клетки-мишени и способа введения. Наиболее стабильную экспрессию генов RHO, RPGR, RP2, PDE6α и PDE6β обеспечивают серотипы AAV2/5 и AAV8 при субретинальном введении. Для подавления мутантного RHO и его замещения эффективны двойные векторы с кшРНК и резистентной к ней кДНК, а для RPGR доказана необходимость кодон-оптимизации изоформы RPGRORF15. В случае RP2 использование самокомплементарного AAV обеспечивало экспрессию в 90% фоторецепторов и восстанавливало структуру наружного ядерного слоя, однако высокая доза вызывала токсический эффект. При терапии PDE6α и PDE6β показана эффективность не только векторной доставки, но и систем редактирования CRISPR и прайм-редактирования. Заключение:Генетическая терапия с использованием аденоассоциированных вирусов является перспективным направлением в лечении наследственных заболеваний сетчатки. Однако остаются нерешенные вопросы, связанные с длительностью эффекта, возможностью иммунного ответа и ограниченной вместимостью вирусных векторов. Дальнейшие исследования направлены на улучшение методов доставки, повышение эффективности экспрессии терапевтических генов и разработку новых подходов, позволяющих лечить широкий спектр наследственных ретинопатий
Ключевые слова: сетчатка, пигментный ретинит, дегенерация, генная терапия, аденоассоциированный вирус, вирусный вектор
Введение. Возрастные и генетически обусловленные заболевания сетчатки – одна из основных причин ухудшения зрения и слепоты в мире [1, 2]. Пигментный ретинит (RP) – тяжелое заболевание сетчатки, поражающее более 1,5 миллионов человек ежегодно и значительно снижающее качество их жизни. Эта форма дистрофии сетчатки относится к наследственным гетерогенным ретинопатиям и характеризуется гибелью фоторецепторов и дегенерацией пигментного эпителия, приводя к куриной слепоте и туннельному зрению [3, 4, 5]. RP проявляется в трех типах наследования: аутосомно-доминантном (ADRP), аутосомно-рецессивном (ARRP) и X-сцепленном (XLRP). Выявлено более 60 генов, связанных с RP, но точные механизмы дегенерации сетчатки до конца не изучены [6].
Традиционные методы лечения, включая хирургию и фармакотерапию, чаще всего лишь замедляют прогрессирование болезни, не устраняя ее причину [7]. В связи с этим генная терапия становится перспективным направлением для лечения генетических заболеваний сетчатки [8].
Аденоассоциированный вирус (AAV) зарекомендовал себя, как один из наиболее безопасных и эффективных инструментов доставки генетического материала в клетки-мишени [9]. Этот вирус обладает уникальными характеристиками, такими, как низкая иммуногенность, способность к долгосрочной экспрессии целевых генов и возможность инфицировать как делящиеся, так и неделящиеся клетки [10]. Более того, многочисленные модификации AAV позволили значительно улучшить их специфичность, тропизм и эффективность доставки, что делает их во многом идеальным вектором для генной терапии заболеваний сетчатки [11, 12].
За последние годы накоплен значительный объем данных о применении AAV в лечении многих наследственных заболеваний, таких, как дистрофия Штаргардта, врожденный амавроз Лебера и других нарушений, связанных с генетическими мутациями. Клинические исследования продемонстрировали успешную доставку трансгенов в клетки сетчатки, восстановление их функции и значительное улучшение зрения у некоторых пациентов [13].
Цель исследования. Целью данного обзора является анализ современных подходов к генной терапии пигментного ретинита с использованием аденоассоциированных вирусов, оценка их эффективности и безопасности, а также выявление перспективных направлений дальнейших исследований. В работе рассматриваются механизмы действия различных терапевтических стратегий, включая подавление экспрессии мутантных генов, их замещение функциональными аналогами и редактирование генома. Особое внимание уделяется сравнительному анализу вирусных векторов, применяемых в клинических испытаниях, а также ограничениям, связанным с их упаковочной емкостью и иммунным ответом организма.
Материалы и методы исследования. Настоящий обзор обобщает результаты исследований и клинических данных по использованию AAV в генной терапии RP. Рассматриваются методы использования AAV для подавления и редактирования генов-мишеней, напрямую ассоциированных с развитием различных форм данного заболевания, а также новые подходы и разработки в этой области. Поиск публикаций проводился в базе данных электронных информационных ресурсов PubMed и Google Scholar по ключевым словам AAV, adeno-associated virus, gene therapy, retinitis pigmentosa, RHO, RP2, RPGR, PDE6. В анализ включены научные статьи в рецензируемых журналах, опубликованные в период с 1997 по 2025 годы. Нижняя граница временного интервала обусловлена тем, что именно в этот период были ранние попытки генной терапии ретинопатий с использованием AAV.
Критерии отбора статей включали: публикации в рецензируемых научных журналах; наличие оригинальных экспериментальных данных in vivo; фокус на генной терапии пигментного ретинита с использованием AAV-векторов; указание на конкретные гены-мишени.
Результаты и их обсуждение
Вектор AAV как платформа для доставки трансгена
На сегодняшний день наиболее успешными вирусными векторами в генной терапии являются ретровирусы, лентивирусы и аденовирусы (Табл. 1). Многие из них имеют ряд недостатков, таких, как высокий риск иммунного ответа и генетических мутаций. В этом отношении AAV считается самой безопасной платформой для доставки трансгенов in vivo [14].
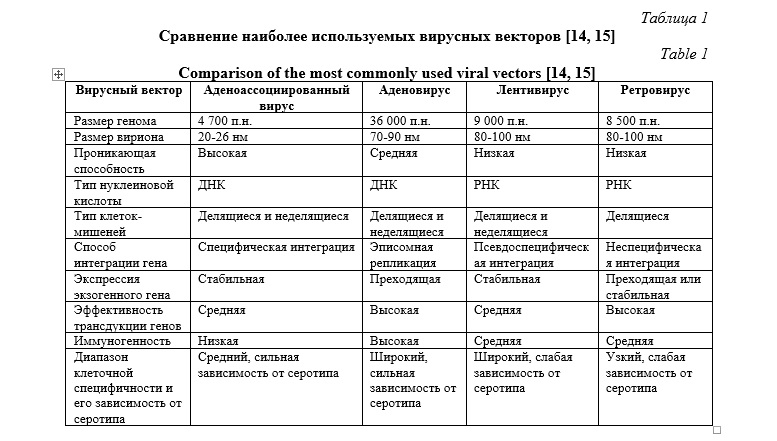
Одной из ключевых особенностей AAV является его непатогенность, связанная с неспособностью к репликации в клетке-хозяине без вируса-сателлита, например, аденовируса [16, 17]. Неизвестны штаммы AAV, самостоятельно вызывающие заболевания у человека, и научное сообщество пришло к консенсусу по этому вопросу [17]. Однако в 2023 году была обнаружена связь коинфекции AAV2 с гепатотропными вирусами и тяжелым течением острого гепатита у детей. Авторы подчеркивают, что прямая причинно-следственная связь не подтверждена, и требуются дальнейшие исследования [17].
Вирусная частица AAV имеет капсид диаметром 20-26 нм, что облегчает ее проникновение в клетки-мишени. Дикий тип AAV способен интегрироваться в геном клетки в локус AAVS1 19-й хромосомы благодаря сходству последовательностей AAVS1 и инвертированных концевых повторов вируса. После инфицирования AAV переходит в латентное состояние [18]. Геном AAV содержит две открытые рамки считывания, кодирующие гены REP и CAP. Ген REP обеспечивает синтез четырех белков для репликации вируса, а CAP кодирует три субъединицы капсида: VP1, VP2 и VP3. В этом же участке, но в другой рамке считывания, кодируется белок AAP, участвующий в сборке вирусных частиц [15]. В 2019 году был идентифицирован белок MAAP, облегчающий инкапсуляцию генетического материала в вирион [19].
Размер одноцепочечного генома AAV составляет около 4 700 п.н. [16]. Компактность генома обеспечивается альтернативным сплайсингом и перекрывающимися рамками считывания. Это ограничивает использование AAV как вектора, так как малая емкость генома требует тщательного проектирования трансгена и регуляторных элементов, а также делает невозможной доставку генов размером более 4 800 п.н. в одиночном векторе [10]. Решением проблемы может стать расщепление кодирующей последовательности на различные векторы AAV [4]. Для одновременного подавления гена и его замещения трансгеном используются двойные векторы, увеличивая упаковочный лимит до 8 900 п.н. [20]. На данный момент большие успехи в генной терапии RP касаются лишь генов с кДНК, не превышающей 4 700 п.н.
Тканевая специфичность AAV зависит от его серотипа, который в большей степени определяется особенностями молекулярного взаимодействия капсида и рецепторов клетки-мишени (Табл. 2). На данный момент выделено 13 природных серотипов с различным тканевым тропизмом. Векторы природных серотипов AAV обладают более низкой специфичностью по сравнению с rAAV [15].
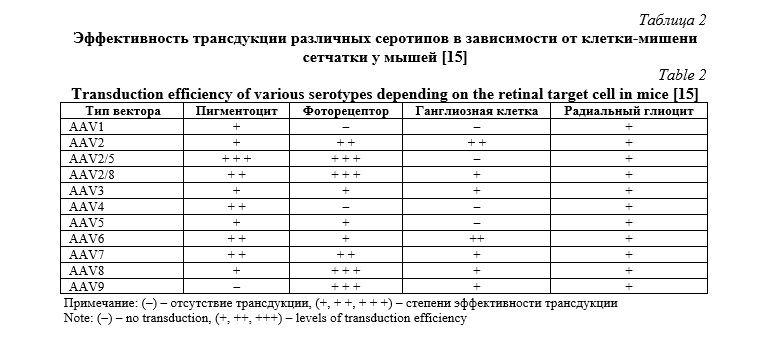
Благодаря высокой тропности некоторых серотипов (например, AAV2, AAV5 и AAV8) к клеткам пигментного эпителия и фоторецепторам их использование позволяет доставлять трансгены непосредственно в клетки сетчатки [12]. Разработка векторов с оптимизированным тропизмом, а также их доставка путем интравитреального или субретинального введения, остаются важными аспектами клинических исследований в области генной терапии сетчатки [11].
В генной терапии RP эталонными векторами считаются AAV5 и AAV8. В двойных векторах в капсиды AAV5 и AAV8, как правило, инкапсулируется геном AAV2, аналогично специфичный к пигментному эпителию. Кроме того, AAV2 – один из наиболее изученных векторов для генной терапии ретинопатий и других наследственных заболеваний [21].
Вектор AAV5 наиболее генетически отличается от всех других серотипов, поскольку был выделен непосредственно из клинических образцов человека. Капсид AAV5 в сочетании с векторным геномом AAV2 обеспечивает эффективную трансдукцию в фоторецепторах и долговременную экспрессию в течение жизненного цикла клетки [15]. Выделенный из ткани макак-резуса вектор AAV8, напротив, обладает высокой степенью гомологичности c другими серотипами – к примеру, структурное сходство между капсидами AAV8 и AAV2 составляет 83% [14].
Подавление и замена гена родопсина RHO
Мутации в гене родопсина человека RHO являются причиной наибольшей части наследственных дегенераций сетчатки [22]. Одной из наиболее частых причин ADRP у людей является мутация RHOP23H. При этом у пациентов с одной и той же формой RP и генетической мутацией скорость прогрессирования заболевания может значительно различаться [4, 23]. Размеры кДНК RHO по данным GenScript равняются 1 400 п.н.
Первые эксперименты по подавлению мутантного гена RHO проводились на модели мышей RHOP23H. Для этого использовался двойной вектор AAV2/5, включающий кшРНК, что обеспечило подавление мутантного гена более чем на 85%. Замещающий RHO экспрессировался с использованием кДНК, устойчивой к кшРНК [24]. Несмотря на увеличение толщины наружного ядерного слоя сетчатки (ONL), восстановление ее функции не было достигнуто, что можно объяснить низкой экспрессией замещающего гена. Более поздние исследования in vivo подтвердили эффективность подхода [25, 26].
Современные исследования модифицируют двойные векторы для повышения их эффективности. Разработан вектор AAV-RS301, содержащий кДНК RHO и кшРНК для деградации мутантной мРНК RHO. Эксперименты на мышах RHOP23H показали сохранение структуры и функции сетчатки [27]. На модели собак с той же мутацией аналогичный подход с использованием AAV2/5 привел к значительному подавлению мутантного гена, стабилизации фоторецепторов и восстановлению их функции. Долгосрочный эффект подтвержден через 8 месяцев [28].
Недавно был предложен мутационно-независимый подход к редактированию RHO с использованием AAV-Cas9 и технологии Homology-Independent Targeted Integration (HITI) [29]. В этом методе редактирование гена осуществляется в 5'-нетранслируемой области RHO, что позволяет избежать влияния на кодирующую последовательность белка.
Исследователи использовали две гидовые РНК, нацеленные на Kozak-последовательность, и систему SpCas9 для редактирования генома фоторецепторов. Инъекции двойных AAV2/8-векторов, несущих SpCas9 и донорную последовательность, привели к эффективной интеграции нового гена в 5'-нетранслируемой области у 43% клеток сетчатки и значительному улучшению структуры и функции фоторецепторов у мышей RHOP23H/wt. ЭРГ показала повышение амплитуды α- и β-волн на поздних стадиях дегенерации, что свидетельствует о сохранении фоточувствительности палочек. Долгосрочные наблюдения (до P480) подтвердили стойкий терапевтический эффект с сохранением экспрессии RHO в сетчатке даже спустя 16 месяцев после введения вектора [29]. Такой подход позволяет подавлять экспрессию мутантного RHO без риска синтеза нефункционального белка, что делает его крайне перспективной стратегией для генной терапии ADRP.
Генная терапия RPGR-ассоциированного RP
Мутации в гене RPGR (кДНК 2 500 п.н.) являются причиной развития ХLRP в 70-90% случаев и 10% всех случаев заболевания [20]. Белок RPGR существует в нескольких изоформах: RPGRex1-19, который участвует в развитии фоторецепторов, и RPGRORF15, распространенная в сетчатке форма, участвующая в поддержании целостности и стабильности наружных сегментов палочек и колбочек. Мутации в изоформе RPGRORF15 ответственны за 80% случаев развития ХLRP [30].
Первые исследования генной терапии ХLRP были проведены в 2012 году с использованием вектора AAV2/5-hRPGR у собак с моделями заболевания XLPRA1 и XLPRA2. После субретинальной инъекции вектора отмечалась сохранность ONL, фоторецепторных сегментов и нормализация экспрессии RPGR в палочках и колбочках. У модели XLPRA1 сетчатка демонстрировала относительную целостность, у XLPRA2 дегенерация была равномерной, но более выраженной в центральной сетчатке. Уменьшалась глиозная реакция, предотвращались изменения в наружном плексиформном слое, характерные для поздних стадий заболевания [31].
Одной из ключевых проблем в разработке генной терапии для RPGRORF15 является его сложная посттранскрипционная обработка, включающая множественные варианты сплайсинга. Эписомальные трансгены AAV, как правило, лишены интронов, что может приводить к непреднамеренному сплайсингу на уровне первичного транскрипта РНК. Дополнительной проблемой является субтерапевтическая экспрессия трансгенов после доставки в сетчатку, что может ограничивать эффективность терапии [32]. Для решения этих проблем была оптимизирована кодирующая последовательность RPGRORF15 и создан стабильный и эффективный вектор для генной терапии ХLRP. Эксперименты in vitro и in vivo подтвердили, что оптимизированный вектор обеспечивает высокую экспрессию RPGRORF15 без потери функциональности белка. Тестирование на мышах RPGR−/− и C57BL/6Jrd9 показало значительное восстановление функции фоторецепторов, что подтверждается данными ЭРГ. Анализ безопасности продемонстрировал отсутствие токсических эффектов от использования оптимизированного вектора [32].
Практически в то же время был исследован вектор AAV2/5-GRK1-hRPGR с промотором GRK1, активный как в палочках, так и в колбочках. Введение вектора собакам с мутацией RPGR на 5-й и 12-й неделе способствовало долговременному сохранению фоторецепторов в течение более 2 лет. Результаты подтвердили более высокую эффективность больших доз вектора. Сравнение стабилизированной версии hRPGRstb и кодон-оптимизированной версии hRPGRco показало, что оба варианта предотвращали дегенерацию сетчатки, но hRPGRco продемонстрировал небольшое преимущество. Подтверждением этому является нормальная морфология фоторецепторов и локализация RPGR в наружных сегментах палочек. Долгосрочные наблюдения не выявили серьезных побочных эффектов, а функция сетчатки сохранялась более 2 лет, подтверждая перспективность AAV2/5-GRK1-hRPGR для клинического применения при RPGR-ассоциированном ХLRP [33].
В настоящее время проводится сразу несколько клинических испытаний различных векторов для терапии RPGR (Табл. 3). В фазе III клинического испытания, спонсируемого MeiraGTx, тестируется препарат Botaretigene Sparoparvovec с вектором AAV2/5-GRK1-RPGRORF15, содержащим укороченную версию трансгена и промотор GRK1. В 2020 году MeiraGTx представила промежуточные результаты фаз I/II (на 6, 9 и 12 месяцах). Параллельно 4D Molecular Therapeutics в 2020 году запустила испытания фаз I/II для оценки безопасности и переносимости вектора [34].
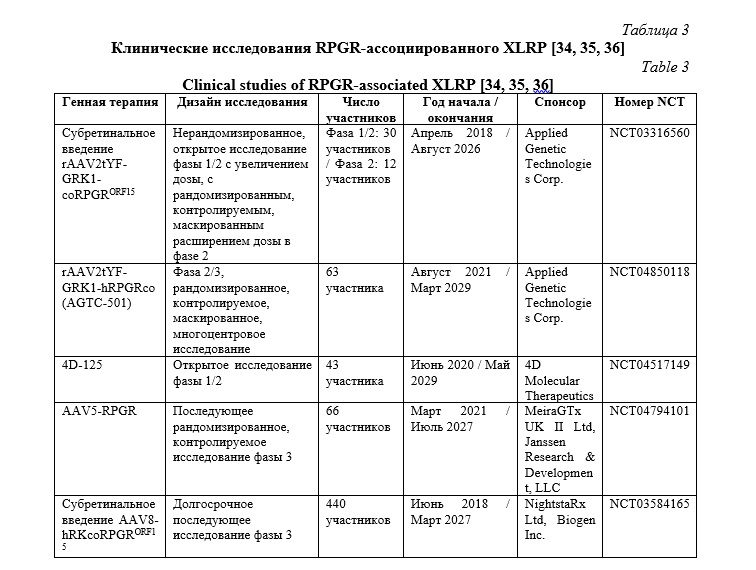
Дополнительно разработан вектор AAV2/8-GRK1-coRPGRORF15, созданный NightstaRx Therapeutics Ltd. (ныне Biogen Inc.) и Оксфордским университетом [35]. Он содержит оптимизированную версию RPGRORF15 под контролем промотора GRK1 и упакован в капсид AAV8, что обеспечивает быструю и эффективную экспрессию в фоторецепторах после субретинального введения. Первое клиническое исследование с этим вектором началось в 2017 году, а его первоначальные результаты были опубликованы в 2020 году [35]. Клинические испытания имели весьма впечатляющий результат – терапевтический эффект в виде улучшения поля зрения наблюдался через месяц после введения AAV8-coRPGR и сохранялся на протяжении 6 месяцев. При более высоких дозах у некоторых пациентов возникали воспалительные реакции, разрешавшиеся после курса кортикостероидов [34, 35].
Компания Applied Genetic Tech Corp разработала генно-терапевтический вектор на основе оптимизированного кодонами человеческого RPGRORF15, который демонстрирует 99% идентичность последовательности, используемой Biogen Inc. Этот ген экспрессируется под контролем промотора GRK1 и упаковывается в вариант капсида AAV2. Стратегия оптимизации кодонов обеспечивает стабильность последовательности в ходе производственного процесса, предотвращая внесение мутаций, которые могли бы изменить или нарушить функцию белка RPGR [36]. Кроме того, Applied Genetic Tech Corp разработала усовершенствованный вектор rAAV2tYF с модифицированным капсидом, который повышает эффективность трансдукции.
Первые попытки терапии RP2-ассоциированного RP
В 10-15% случаев за развитие ХLRP отвечают мутации в RP2 (кДНК 1 050 п.н.). Ген RP2 участвует в регуляции цилиарного транспорта фоторецепторов, и его мутации приводят к раннему апоптозу палочек и колбочек, что вызывает прогрессирующую потерю зрения. RP2-ассоциированный RP преимущественно проявляется в детском возрасте и характеризуется быстрой дегенерацией сетчатки, поражением желтого пятна и полной потерей эллипсоидов палочек и колбочек [4, 21].
Первые работы, посвященные генной терапии RP2-ассоциированного ХLRP, были опубликованы относительно недавно. В 2015 году был создан самокомплементарный вектор AAV с кодирующей последовательностью RP2 и впервые продемонстрировали способность индуцировать экспрессию RP2 в фоторецепторах мышей модели с нокаутом целевого гена. Сохранение функции колбочек достигалось при широком диапазоне доз в течение 18 месяцев, о чем свидетельствует фотопическая ЭРГ. Терапевтический эффект был достигнут даже у мышей, получавших лечение на поздней стадии заболевания. Установлено, что самая высокая доза AAV-RP2 1×109 vg/глаз оказывает токсичный эффект на сетчатку, что характеризовалось истончением или полным исчезновением ONL [37].
Дальнейшие исследования подтвердили эффективность AAV-опосредованной генной терапии RP2. В эксперименте [38] на культурах стволовых клеток сетчатки с нокаутом RP2 показано, что введение AAV2/5-CAGp-RP2 индуцирует экспрессию RP2 в 90% фоторецепторов, включая палочки и колбочки. Иммуногистохимический анализ подтвердил локализацию белка на плазматической мембране, а уровень мРНК RP2 увеличивался в 55 раз по сравнению с контролем. Генная терапия также приводила к значительному утолщению ONL и восстановлению экспрессии родопсина, что соответствует сохранению функции фоторецепторов. Эффективность AAV2/5 в доставке RP2 в фоторецепторы сопровождалась минимальным проникновением в другие слои сетчатки.
Введение вектора до начала истончения ONL предотвращало дегенерацию фоторецепторов, однако остается открытым вопрос о необходимости экспрессии RP2 в пигментном эпителии. Если в ходе дальнейших исследований выяснится, что для лучшего терапевтического эффекта необходима экспрессия RP2 в пигментоцитах и фоторецепторах одновременно, то векторную конструкцию нужно модифицировать так, чтобы обеспечивалась экспрессия в обоих типах клеток. Эффективность терапии RP2-ассоциированного ХLRP может повысить и оптимизация стратегии доставки, включая выбор промотора и времени введения, но на данный момент исследования в этом направлении крайне малочисленны или отсутствуют вовсе.
Генная терапия PDE6-ассоциированного RP
Гены PDE6α и PDE6β (размеры обоих кДНК 2 600 п.н.) кодируют соответственно α- и β-субъединицы фосфодиэстеразы 6 — ключевого фермента фототрансдукционного каскада, который регулирует уровень циклического гуанозинмонофосфата (цГМФ) в фоторецепторах. Мутации приводят к накоплению цГМФ в фоторецепторах, что приводит к их постепенной дегенерации и развитию одной из наиболее агрессивных форм RP, на долю которого приходится до 5% всех случаев заболевания [39, 40]. Установлено, что оба гена ферментативно эквивалентны друг другу, а результаты последних исследований подтверждают, что один ген может компенсировать дефицит другого [41].
Ранние попытки генной терапии были направлены на восстановление экспрессии PDE6β. После интравитреального введения AAV2-β-PDE у мышей модели rd1 наблюдалась повышенная экспрессия иммунореактивного белка в фоторецепторных клетках, дегенерация сетчатки лишь незначительно замедлилась по сравнению с контрольной группой. Основным ограничением исследования оказался низкий титр AAV2 в модели быстропрогрессирующей дегенерации сетчатки [42].
Дальнейший прогресс в инженерии капсидов и методах очистки векторов позволил создать AAV с высоким титром и улучшенной трансдукцией. Субретинальное введение оптимизированных векторов AAV5-smCBA-PDEβ предотвращает дегенерацию сетчатки у мышей модели rd10 и обеспечивает выживаемость фоторецепторов [43]. Но ни один из ранних подходов терапии PDE6β-ассоциированной RP не привел к устойчивому и долгосрочному сохранению функции сетчатки у мышиных моделей, включая rd1 и rd10. Основным ограничением в данном контексте является крайне узкое «терапевтическое окно», в рамках которого необходимо добиться достаточно высокого уровня экспрессии трансгена в фоторецепторах, прежде чем последствия дегенерации станут необратимыми [44].
Более поздние исследования терапии PDE6β доказали высокую эффективность самых различных векторов — AAV8, AAV2/8 и AAV2/5, AAV2/1 и AAV2 [43-49]. Но высокая скорость дегенерации и общая агрессивность заболевания до сих пор накладывает серьезные ограничения. Потенциальную эффективность демонстрирует генная терапия HORA-PDE6β с использованием AAV2/5, несущего кДНК человеческого PDE6β. На данный момент эта терапия проходит клиническое испытание I/II фазы, промежуточные результаты которого свидетельствуют о реактивации фототрансдукции в палочках у пациентов, получивших высокую дозу вектора [50].
В исследовании [51] продемонстрирована высокая терапевтическая эффективность вектора rAAV8-PDE6α на мышиной модели RP43. Обнаружено, что вектор приводит к стабильной и высокой экспрессии белка в палочках и существенной выживаемости фоторецепторов в течение не менее 6 месяцев [51]. Частичное восстановление функции палочек и сохранение структуры сетчатки наблюдались на мышиных моделях и собаках с различных мутациями PDE6α после введения rAAV8 [52]. Установлена связь между геном NRL и развитием PDE6α-ассоциированного RP. После инактивации NRL с помощью конструкции AAV2-SaCas9 наблюдалось улучшение выживаемости фоторецепторов и восстановление функции сетчатки у мышей с дефицитом PDE6α [53].
Дополнительно перспективной стратегией коррекции мутаций в PDE6α является использование технологий редактирования генома, таких, как прайм-редактирование. В работе [54] прайм-система, доставленная с помощью двойного AAV, продемонстрировала высокую точность и некоторую эффективность в редактировании патогенной мутации PDE6α в модели RP43. Коррекция была достигнута с эффективностью 9,4% без явных побочных мутаций, что позволило восстановить экспрессию белка, сохранить фоторецепторы и частично восстановить зрительную функцию. Несмотря на небольшой процент успешной коррекции целевого гена, по нашему мнению, прайм-редактирование имеет потенциал как альтернативный метод терапии PDE6α-ассоциированного RP ввиду отсутствия наблюдаемых побочных эффектов.
Параллельно рассматривается новый подход, основанный на CRISPR-опосредованной активации транскрипции. В недавнем исследовании [41] использовалась система CRISPR-dCasMINI, доставляемая с помощью AAV, для активации экспрессии гена PDE6β с целью компенсации дефицита PDE6α у мышей. У животных зафиксировано сохранение структуры сетчатки и улучшение зрительных функций. Значительное повышение мРНК и уровня экспрессии PDE6β было обеспечено оптимальной гидовой РНК. Таким образом, мутационно-независимый метод CRISPR-опосредованной активации является многообещающим терапевтическим лечением PDE6-ассоциированного RP.
Разработка новых технологий
Генные терапевтические агенты могут вводиться в глаз двумя основными способами: субретинальной или интравитреальной инъекцией. Интравитреальная инъекция является менее инвазивной процедурой, при которой вектор доставляется в стекловидное тело, преимущественно инфицируя ганглиозные клетки сетчатки. Метод технически проще и сопряжен с меньшими хирургическими рисками, но имеет ограниченную эффективность трансдукции фоторецепторов и может вызывать более выраженный иммунный ответ из-за системного распространения вектора.
Субретинальная инъекция позволяет доставить вектор непосредственно в пигментный эпителий и фоторецепторам, обеспечивая точечную и локализованную трансдукцию [16, 55, 56]. Данный метод более инвазивен и требует тщательного контроля над формированием субретинального пузыря, чтобы избежать таких осложнений, как отслоение сетчатки или формирование макулярных отверстий. Перспективные результаты в автоматизации подобных операций демонстрируют роботизированная система IRISS, разработанная в Институте Джулса Стейна и Калифорнийском университете, и R2D2 Оксфордского университета [20, 57].
Несмотря на высокую эффективность субретинальных инъекций, традиционные серотипы AAV ограничены в способности распространяться латерально, и клетки, находящиеся за пределами области инъекции, получают лишь незначительное количество вектора. Это создаёт необходимость в создании новых rAAV-векторов, обеспечивающих трансдукцию обширных участков сетчатки и пригодных для менее инвазивных методов доставки, таких как интравитреальная инъекция [18, 58].
В последние годы были разработаны новые инженерные стратегии для оптимизации rAAV с целью повышения эффективности доставки в сетчатку. В одном из таких подходов сочеталась системная доставка библиотеки AAV с локальным выделением AAV-геномов из клеток-мишеней сетчатки, что позволило создать высокий селекционный прессинг [59]. В результате трехэтапного скрининга in vivo, проведенных на мышах C57BL6/J, были получены два новых варианта капсидов: AAV2.GL и AAV2.NN. Векторы обеспечивают широкую трансдукцию сетчатки после единственной интравитреальной инъекции, демонстрируют высокую устойчивость к нейтрализующим антителам в сыворотке человека и эффективно инфицируют фоторецепторы у мышей, собак и нечеловекообразных приматов. Эксперименты на мышиной модели ахроматопсии CNGA3−/− подтвердили терапевтическую эффективность векторов при интравитреальной доставке гена в колбочки [58].
Разработан новый серотип AAV44.9 и его модифицированная версия AAV44.9(E531D), демонстрирующие высокую эффективность трансдукции фоторецепторов. Исследования показали, что после субретинального введения оба вектора обеспечивают более эффективную трансдукцию по сравнению с эталонными векторами AAV5 и AAV8. Введение AAV44.9(E531D) в сетчатку макак привело к трансдукции до 98% фовеальных колбочек, сохранившихся при заболевании, а также эффективному заражению парафовеальных и перифовеальных фоторецепторов. Кроме того, модифицированный вектор обеспечивал более широкое латеральное распространение векторного материала, что позволило расширить терапевтическую зону при введении. Эксперименты на модели дегенерации сетчатки у мышей подтвердили способность AAV44.9(E531D) восстанавливать функцию фоторецепторов [59], что делает его перспективным кандидатом для лечения наследственных ретинопатий, требующих трансдукции большого числа клеток.
Как уже было упомянуто ранее, значительным ограничением AAV является его небольшая упаковочная емкость, что делает невозможной доставку полноразмерных генов, таких, как RPGRORF15, или кассет редактирования CRISPR/Cas [20]. Для решения этой проблемы исследуются возможности расширения емкости до тройных векторов с потенциальным объемом до 14 000 п.н. и создания усеченных версий генов, кодирующих укороченные, но функциональные белки [60]. Данный подход был успешно реализован в терапии мышечной дистрофии Дюшенна с использованием усеченного дистрофина, который, несмотря на уменьшенный размер, сохраняет частичную функциональность и ослабляет тяжесть заболевания. Аналогичные стратегии разрабатываются для лечения дисферлинопатии и врожденного амавроза Лебера [6]. Однако усечение гена требует глубокого понимания структуры и функции белка, что делает этот метод специфичным для каждого отдельного гена и трудоемким в использовании.
Альтернативный подход заключается в использовании двух AAV-векторов, несущих разные половины гена, которые рекомбинируют внутри клетки, воссоздавая полную последовательность. Для усиления этого процесса могут использоваться оптимизированные рекомбинационные последовательности, механизмы транс-сплайсинга, аналогичные сплайсингу мРНК. Перспективным направлением является интеин-опосредованный транс-сплайсинг белка, который позволяет точно соединять две половины белка после экспрессии. Данный метод продемонстрировал свою эффективность для восстановления дистрофина и доставки Cas9, но остается на стадии доклинических испытаний [61]. Оптимизация рекомбинационных последовательностей и усовершенствование сплит-интеинов могут значительно повысить эффективность данного подхода и расширить его клиническое применение.
Заключение. Генная терапия пигментного ретинита с использованием AAV-векторов, таких как AAV2/5 и AAV8, доказала клиническую эффективность, особенно для RPGR- и PDE6-ассоциированных форм, обеспечивая устойчивую экспрессию генов и восстановление зрительных функций. Технологии CRISPR/Cas и прайм-редактирования, применяемые в доклинических и клинических исследованиях, открывают перспективы для лечения наследственных ретинопатий.
Информация о финансировании
Финансирование данной работы не проводилось.
Благодарности
Хакимов АР, Мусина ЛА, Лебедева АИ, и др. Современные достижения генной терапии пигментного ретинита с применением аденоассоциированного вируса (обзор). Научные результаты биомедицинских исследований. 2026;12(1):5-23. [Khakimov AR, Musina LA, Lebedeva AI, et al. Current advances in gene therapy for retinitis pigmentosa using adeno-associated virus (review). Research Results in Biomedicine. 2026;12(1):5-23. Russian]. DOI: 10.18413/2658- 6533-2026-12-1-0-1





















Список литературы