Миссенс-вариант rs11556924 в гене ZC3HC1 характеризуется протективным эффектом в отношении риска развития облитерирующего атеросклероза сосудов нижних конечностей у женщин
Aннотация
Актуальность: Облитерирующий атеросклероз сосудов нижних конечностей (ОАСНК) представляет собой одну из самых распространенных форм заболеваний периферических сосудов нижних конечностей. Принимая во внимание потенциальное участие полиморфных вариантов гена, реализуемое через регулирование пролиферации гладкомышечных клеток, эти участки ДНК могут рассматриваться как генетические маркеры предрасположенности к атеросклерозу. Цель исследования: Изучение взаимосвязи однонуклеотидных полиморфизмов (SNP), ассоциированных по результатам полногеномного анализа ассоциаций (GWAS) с риском развития ишемической болезни сердца, с предрасположенностью к ОАСНК. Материалы и методы: В исследование было включено 1278 пациентов, включая 630 больных ОАСНК и 648 относительно здоровых лиц. Проведено генотипирование четырех SNP rs9818870, rs17087335, rs11556924 и rs9982601 с использованием геномного масс-спектрометра MassARRAY-4. Анализ ассоциации аллелей и генотипов с ОАСНК проводился с использованием программы PLINK, v1.9. Адаптивный пермутационный тест использовался для расчета уровня статистической значимости ассоциаций (Pperm). Результаты: Установлено, что аллель rs11556924-T (OR=0,81 95%CI 0,69-0,95, Pperm=0,02) и генотип rs11556924-T/T (OR=0,60 95%CI 0,43-0,82, Pperm=0,006) гена ZC3HC1 ассоциированы с пониженным риском развития ОАСНК. Однако, стратифицированный по полу анализ показал, что SNP rs11556924 ассоциирован с пониженным риском развития ОАСНК исключительно у женщин (OR=0,56 95% CI 0,39-0,81, Pperm=0,002). Также установлено, что SNP rs11556924 ассоциирован с повышением уровнем триглицеридов крови у больных ОАСНК (β=0,131 Рperm=0,03). Другие исследованные SNP показали ассоциации с триглицеридами, ЛПНП, ангиографическими показателями у больных ОАСНК. В частности, полиморфизм rs9982601 гена MRPS6 ассоциировался с поражением атеросклеротическими бляшками подвздошных артерий (Рperm=0,001). Заключение: Настоящее исследование впервые установило, что полиморфизм rs11556924 гена ZC3HC1 является новым генетическим маркером предрасположенности к облитерирующему атеросклерозу сосудов нижних конечностей и характеризуется протективным эффектом в отношении риска развития болезни у женщин
Ключевые слова: облитерирующий атеросклероз, генетические биомаркеры, степень стеноза артерий, патогенез, однонуклеотидный полиморфизм
Введение. Заболевания периферических артерий (ЗПА) занимают одно из лидирующих мест в развитии заболеваемости и смертности от сердечно-сосудистых патологий. ЗПА характеризуются развитием стеноза или окклюзий любой локализации на всем протяжении участка от аорто-подвздошного сегмента до подошвенных артерий. Сегодня ЗПА подвержены около 236 миллионов человек, что ставит их на одну ступень с ишемической болезнью сердца (ИБС) и цереброваскулярными заболеваниями и дает право называть ЗПА самостоятельным заболеванием [1, 2].
Облитерирующий атеросклероз сосудов нижних конечностей (ОАСНК) –ведущее по значимости и распространенности заболевание артерий нижних конечностей, которое приводит к развитию синдрома хронической ишемии [3, 4]. Существует ряд исследований, указывающих на мультифакториальную природу ОАСНК, что означает вовлеченность, как средовых, так и генетических факторов в его развитие [5, 6]. Несмотря на данный факт, база исследовательских работ, результаты которых доказывают четкую связь между разными вариантами генов и риском прогрессирования облитерирующего атеросклероза сосудов нижних конечностей, малочисленна в сравнении с той, что посвящена изучению связи между генетической предрасположенностью к развитию атеросклероза коронарных и церебральных артерий.
Результаты пяти крупных исследований, опубликованных в базе данных каталога полногеномных ассоциативных исследований (GWAS, genome-wide association study), выявили 260 однонуклеотидных полиморфизмов (SNP), связанных с повышенным риском развития заболеваний периферических артерий [https://www.ebi.ac.uk/gwas/home]. В тоже самое время, значительная часть последующих исследований, выполненных в независимых популяциях мира, показала относительно низкую воспроизводимость выявленных в результате GWAS ассоциаций однонуклеотидных полиморфизмов (single nucleotide polymorphisms, SNP) с заболеваниями периферических артерий. Согласно данным недавно опубликованного мета-анализа, 112 статей, описывающих 231 ДНК-полиморфизм, ассоциированный с заболеваниями периферических артерий, установлено лишь 19 ассоциированных с болезнью вариантов, которые были воспроизведены в нескольких крупных когортах пациентов [7].
Опираясь на приведенные выше факты и учитывая межэтническую генетическую гетерогенность и территориальные различия во влияниях средовых факторов, требуется валидация результатов GWAS в отдельных популяциях мира с целью отбора генетических маркеров, которые могли бы использоваться для молекулярной диагностики болезни и персонализированных подходов к её лечению и профилактике.
Цель исследования. В рамках этого предварительного исследования была поставлена цель выявить взаимосвязи между разными вариантами генов, обнаруженных в исследованиях полногеномных ассоциаций с риском прогрессирования облитерирующего атеросклероза сосудов нижних конечностей. Исследование фокусировалось на жителях центральной России.
Материалы и методы исследования. При проведении исследования были учтены основные принципы медицинской этики и общие положения Хельсинской Декларации Всемирной Медицинской Ассоциации. Было получено одобрение регионального этического комитета Курского государственного медицинского университета (№9 от 10.12.2019). Перед началом работы все пациенты исследованной группы предоставили письменное информированное согласие на добровольное участие, а также понимание целей и всех проведенных процедур.
Проведен сбор клинического материала, включающего 1278 неродственных лиц славянского происхождения, в том числе 630 больных ОАСНК и 648 относительно здоровых лиц, с отсутствием хронических заболеваний.
Больные ОАСНК проходили стационарное лечение на базе отделения сосудистой хирургии Курской областной клинической больницы. Диагноз ОАСНК был установлен на основе критериев, изложенных в Национальных рекомендациях по диагностике и лечению заболеваний артерий нижних конечностей (2019 г.). Для оценки степени поражения периферических артерий у пациентов с ОАСНК использовались методы ультразвукового дуплексного сканирования и ангиографии артерий нижних конечностей. Эти методы обеспечивают точную визуализацию артерий и позволяют определить наличие и степень сужения или закупорки сосудов [8].
Каждому пациенту было произведено вычисление лодыжечно-плечевой индекс (Ankle Brachial Index или ABI) – показателя, который отражает состояние кровотока в нижних конечностях. Критериями включения пациентов в группу больных ОАСНК были: наличие клинически значимого стеноза одной или более артерий нижних конечностей согласно классификации Фонтейна, а также значение 0,6 и ниже лодыжечно-плечевого индекса. Степень атеросклеротического поражения артерий по результатам инструментального исследования выражали значениями: 1 (стеноз≤50%;), 2 (стеноз 51-70%) и 3 (стеноз ≥71%). Все участники исследования проходили анкетирование относительно факторов риска болезни с использованием валидированного опросника [9]. Для молекулярно-генетических исследований у каждого участника исследования проводился забор 5 мл венозной крови в пробирки с 0,5М этилендиаминтетрауксусной кислотой (ЭДТА). Геномную ДНК извлекали с использованием стандартного метода фенольно-хлороформной экстракции с последующей преципитацией этанолом. Для этого исследования были выбраны четыре однонуклеотидных полиморфизма (SNP) из различных генов, ранее связанных с риском развития коронарного атеросклероза в полногеномных ассоциативных исследованиях (GWAS). Для исследования из каталога GWAS (GWAS Catalog, https://www.ebi.ac.uk/gwas/home) были отобраны следующие локусы: полиморфизм rs9818870 гена в 3¢-нетранслируемой области гена MRAS (muscle RAS oncogene homolog), rs17087335 в области интрона гена NOA1 (nitric oxide associated 1), rs11556924 в экзоне гена ZC3HC1 (zinc finger C3HC-type containing 1) и rs9982601 в интроне гена MRPS6 (mitochondrial ribosomal protein S6). Данные по числу успешно прогенотипированных образцов ДНК участников исследования представлены в таблице 1.

Настоящее исследование было проведено в соответствии с руководящими принципами STregthening the REporting of Genetic Association Studies (STREGA). Статистическая мощность была оценена с использованием калькулятора мощности исследования генетических ассоциаций (GAS) (https://csg.sph.umich.edu/ abecasis/gas_power _calculator/). Ассоциативный анализ (α=0,05) позволил выявить относительный риск генотипа (OR) 1,30-1,50 с мощностью 88-99% в целом (630 больных ОАСНК и 648 представителей контрольной группы) и показателем OR 1,40-1,7 с мощностью 80-99%. в подгрупповом анализе. В рамках нашего исследования мы использовали статистические методы для анализа ассоциаций между вариантами генов и риском развития облитерирующего атеросклероза сосудов нижних конечностей. Для оценки частот генотипов и аллелей мы применили точный тест Фишера и критерий хи-квадрат, в соответствии с равновесием Харди-Вайнберга (HWE), сравнивались различные частоты аллелей и генотипов в исследуемых группах, чтобы выявить потенциальные ассоциации между ними и риском ОАСНК. использовалось программное обеспечение SNPStats. (https://www.snpstats.net/start.htm) и PLINK, v1.9.
Для оценки силы ассоциаций между генетическими вариантами и риском развития ОАСНК рассчитывались показатели отношения шансов (OR) и их 95-процентные доверительные интервалы (95%CI). Для анализа взаимосвязи исследованных полиморфных локусов на количественные показатели пациентов с ОАСНК (липидный состав крови, лодыжечно-плечевой индекс) использовался метод линейного регрессионного анализа. Уровень значимости (Pperm) ассоциаций оценивали с помощью адаптивного пермутационного теста с использованием программы PLINK. Для оценки влияния ДНК полиморфизма на количественные показатели использовали метод линейного регрессионного анализа, который предусматривает нормальные распределения количественных предикторов. В связи с тем, что все количественные показатели ЛПИ, липидный состав, данные УЗИ и ангиографии показали распределение отличное от нормального (тест Колмогорова-Смирнова), данные признаки были трансформированы методом обратного рангового преобразования. Учитывая то, что в полногеномных ассоциативных исследованиях для оценки ассоциаций ДНК-маркеров с фенотипами тестируется, как правило, аддитивная модель, все выполненные нами расчеты проводились исключительно в рамках данной генетической модели.
Функциональная аннотация генетического варианта rs11556924, связанного с риском развития ОСАНК, была проведена с использованием биоинформатических ресурсов и инструментов Ensembl Genome Browser. [https://www.ensembl.org/index.html], VannoPortal [http://www.mulinlab.org/vportal/index.html], QTLbase2 [http://www.mulinlab.org/ qtlbase/index.html] и HaploReg v4.2 https://pubs.broadinstitute.org/mammals /haploreg/haploreg.php].
Результаты и их обсуждение. Результаты клинических и лабораторных исследований участников исследования были детально описаны в нашем предыдущем исследовании [5]. Частоты генотипов изучаемых полиморфных вариантов соответствовали равновесию Харди-Вайнберга (p>0,05), что указывает на отсутствие отклонений от ожидаемых частот генотипов в популяции. Результаты анализа ассоциаций между этими полиморфными вариантами и риском развития облитерирующего атеросклероза сосудов нижних конечностей представлены в таблице 2.
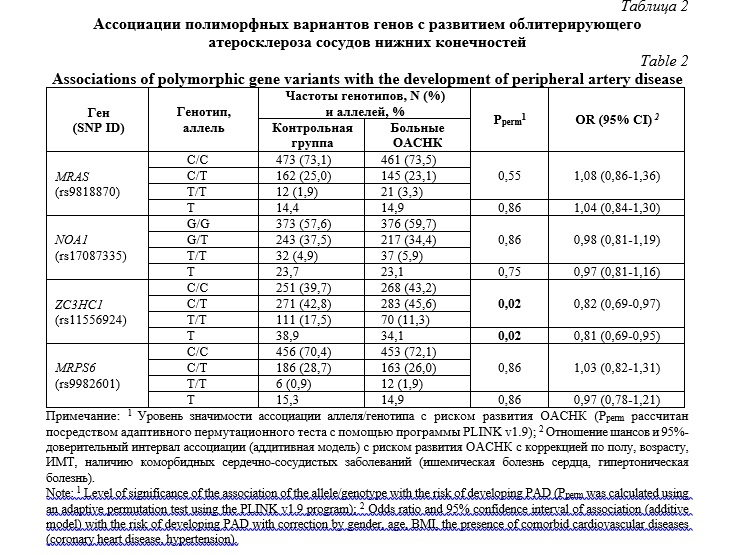
Таблица 2 содержит следующую информацию: аллель rs11556924-T (OR=0,81 95%CI 0,69-0,95, Pperm=0,02) и генотип rs11556924-T/T (OR=0,60 95%CI 0,43-0,82, Pperm=0,006, рецессивная модель) были ассоциированы с пониженным риском развития ОАСНК. Для остальных изученных генетических локусов не наблюдалось статистически значимых различий в частотах аллелей и генотипов между группами пациентов с ОАСНК и здоровыми лицами. Это указывает на отсутствие ассоциаций между этими локусами и риском развития ОАСНК в исследованной популяции.
Проведен стратифицированный анализ ассоциаций SNP с риском развития ОАСНК раздельно у мужчин и женщин. Результаты анализа ассоциации полиморфных вариантов генов с риском развития облитерирующего атеросклероза сосудов нижних конечностей (ОАСНК) у мужчин и женщин представлены в таблицах 3 и 4 соответственно.
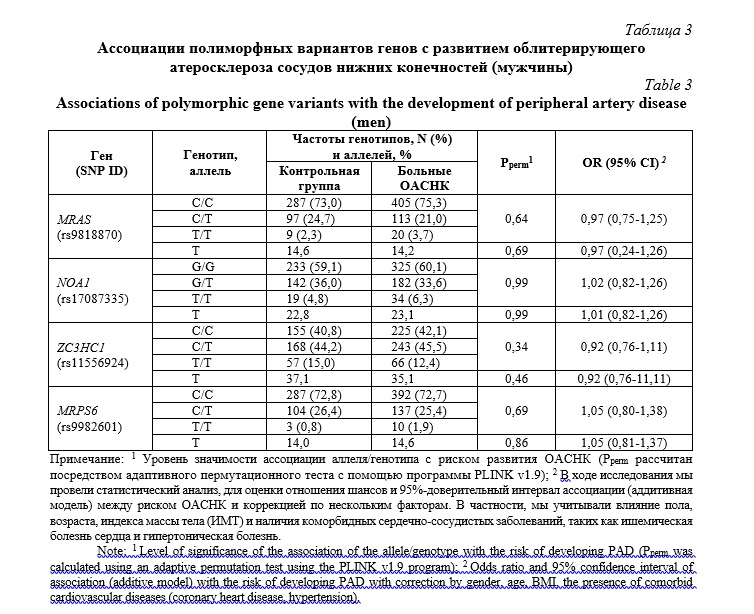
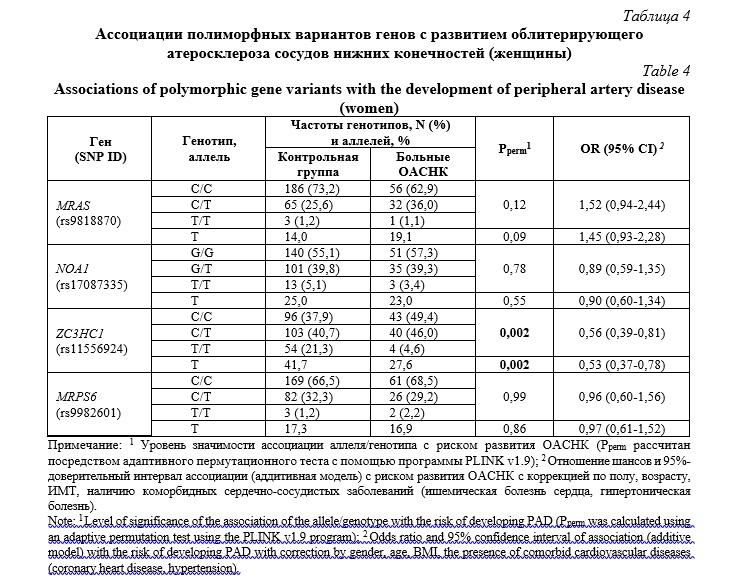
В ходе исследования не было обнаружено статистически значимых ассоциаций между исследованными локусами и ОАСНК у мужчин. Однако, при анализе данных у женщин было установлено, что полиморфный вариант rs11556924 гена ZC3HC1 имеет защитный эффект, ассоциируясь с пониженным риском развития ОАСНК. Эта находка будет иметь принципиальное значение для разработки новых подходов к профилактике и лечению ОАСНК у женщин, учитывая роль гена ZC3HC1 в регуляции процессов, связанных с развитием этого заболевания.
Анализ ассоциации, стратифицированный по статусу курения, не выявил статистически значимых различий во взаимосвязи исследуемых полиморфных вариантов генов с риском развития ОАСНК. Таблица 5.
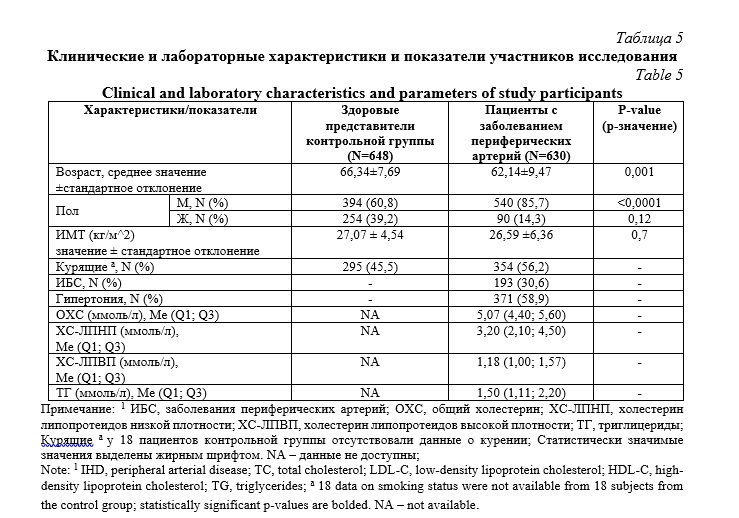
Исследованы ассоциации полиморфных вариантов с лабораторными и инструментальными (ультразвуковое исследование и ангиография периферических артерий) данными пациентов с ОАСНК. Установлено, что SNP rs11556924 был ассоциирован с повышением уровнем триглицеридов крови у больных ОСАНК (β=0,131 Рperm=0,03). Полиморфизм rs9818870 гена MRAS показал статистически значимые ассоциации с усредненным показателем ABI или лодыжечно-плечевым индексом (β=-0,019 Рperm=0,04), уровнем ЛПНП (β=0,377 Рperm=0,05), ТГ (β=-0,255 Рperm=0,02), а также c наличием стеноза аорто-подвздошного сегмента слева (Рperm=0,04). Полиморфизм rs9982601 гена MRPS6 был ассоциирован с поражением атеросклеротическими бляшками подвздошных артерий или синдромом Лериша (Рperm=0,001).
Таким образом, не смотря на половой диморфизм, нами впервые выявлена ассоциация rs11556924 гена ZC3HC1 с предрасположенностью к ОАСНК. Согласно результатам крупнейших международных геномных исследований, аллель rs11556924-T гена ZC3HC1 ассоциирован с пониженным риском развития ишемической болезни сердца [11], инфаркта миокарда [12], положительно коррелирует с уровнем лейкоцитов [13] и тромбоцитов [14] и отрицательно с уровнем гемоглобина крови [13]. Кроме того, аллель rs11556924-T ассоциирован со снижением уровня диастолического и систолического артериального давления [9], а также увеличением уровня тестостерона крови [15]. В контексте полового диморфизма выявленной нами ассоциации rs11556924 с ОАСНК у женщин заслуживают результаты крупного исследования у женщин европеоидного происхождения (N=189473), свидетельствующие о том, что аллель rs11556924-T тесно положительно коррелирует с уровнем глобулина, связывающего и транспортирующего половые гормоны [15, 16], преимущественно тестостерон и дигидротестостерон, и повышение уровня которых увеличивает риск метаболических заболеваний у мужчин и снижает их риск у мужчин.
Ген ZC3HC1 кодирует важнейший компонент лигазного комплекса E3 SCF-типа, SCF (NIPA), комплекса, который контролирует вход в митоз, опосредуя убиквитинирование и последующую деградацию циклина B1 (CCNB1). В свою очередь, CCNB1 участвует в пролиферации гладкомышечных клеток и, согласно Silvestre-Roig С et al, 2013, снижение его экспрессии и, как следствие уменьшение выработки циклина В1, приводит к уменьшению пролиферации гладкомышечных клеток и разрастанию неоинтимы. Данный механизм взаимодействия продуктов гена ZCHC1 и атеросклеротических процессов подтверждается и в работе Linseman T et al., 2017, направленной на изучение антиатерогенного эффекта изучаемого нами гена [17, 18]. В литературе опубликованы исследования, которые направлены на оценку влияния экспрессии гена ZC3HC1 на изменение комплекса интима-медиа. В работе Lopez-Mejias R et al., 2013 приведены данные, подтверждающие ассоциацию изучаемого нами полиморфизма с субклиническим атеросклерозом у лиц, страдающих ревматоидным артритом. При этом в качестве основного признака наличия атеросклеротического поражения, ассоциируемого с полиморфизмом, является увеличение показателя комплекса интима-медиа, что также позволяет установить связь между продуктами гена и атеросклерозом через вовлеченность в процессы клеточной пролиферации и ангиогенеза [19].
В таблице 6 представлены данные функционального аннотирования rs11556924 гена ZC3HC1 с использованием данных Ensembl Genome Browser.
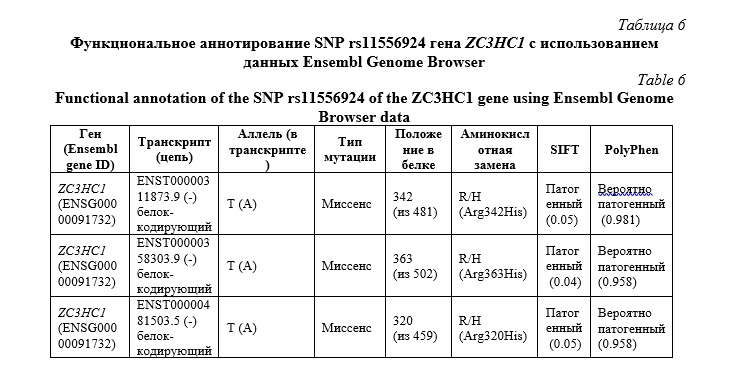
Нуклеотидная замена C>T (rs11556924) фактически представляет собой миссенс мутацию, которая сопровождается несинонимичной аминокислотной заменой аргинина на гистидин в одном из трех транскрибируемых вариантов гена ZC3HC1 (Arg342His, Arg363His и Arg320His). Биоинформатические инструменты SIFT и PolyPhen позволили предсказать, что данные аминокислотные замены представляют собой патогенные или вероятно патогенные варианты, влияющие на структуру белка ZC3HC1. Согласно данным QTLbase2 аллель rs11556924-T ассоциирован с выраженным снижением экспрессии гена KLHDC10 в крови (размер эффекта -0,2188, P=3,9×10-13). KLHDC10 (kelch domain containing 10) - белок, являющийся частью комплекса убиквитин-протеинлигазы E3 (CRL2) пути DesCEND (разрушение посредством дегронов на C-конце), который распознает C-дегрон, расположенный на C-конце белков-мишеней, что приводит к их убиквитинированию и деградации [20]. KLHDC10 расположен в том же геномом участке, что и ZC3HC1. По всей видимости, учитывая тот факт, что миссенс мутация rs11556924 может сопровождаться нарушением структуры белка и, следовательно, его конформации вследствие его неправильного сворачивания, можно полагать существование потенциальной взаимосвязи KLHDC10 с процессами убиквитинирования и деградация мутантной формы ZC3HC1. Кроме того, согласно данным порталов VannoPortal и QTLbase2, SNP rs11556924 может находиться в неравновесии по сцеплению с miQTL – участком связывания для микроРНК hsa-miR-183-5p, уровень экспрессии которой в крови отрицательно коррелирует с носительством аллеля rs11556924-T гена ZC3HC1 (размер эффекта -0,8819. P=0,01). Примечателен тот факт, что повышенный уровень экспрессии в крови микроРНК hsa-miR-183-5p является биомаркером атеросклероза и регуляции роста гладкомышечных клеток сосудов [21, 22]. Согласно данным HaploReg v4.2, данный полиморфизм также может представлять собой участок связывания гистондеацетилазы 2 (HDAC2), вовлеченной в регуляцию транскрипции и клеточного цикла. Известно, что данный класс ферментов играет роль в регуляции сосудистого гомеостаза и может иметь патогенетическое значение для развития атеросклероза [13]. Согласно данным VannoPortal, полиморфизм rs11556924 также располагается в области гистонового маркера H3K36me3, который действует как метка для гистондеацетилаз, связывающих и деацетилирующих гистоны, тем самым предотвращая неконтролируемую транскрипцию [23]. Таким образом, полиморфизм rs11556924, ассоциированный с риском развития ОАСНК, представляет собой функционально значимый вариант, который, хотя и является миссенс-мутаций, по всей видимости, находится в неравновесии по сцеплению с другими некодирующими SNP, которые представляют собой участки для эпигенетической регуляции экспрессии гена. Дальнейшие функциональные исследования позволят раскрыть молекулярные механизмы, посредством которых данный генетический вариант связан с формированием облитерирующего атеросклероза артерий нижних конечностей.
Заключение. По результатам настоящего исследования впервые установлено, что полиморфный вариант rs11556924 гена ZC3HC1 обладает протективным, антиатерогенным действием в отношении облитерирующего атеросклероза артерий нижних конечностей. Малое количество функциональных исследований данного варианта лишь частично позволяет объяснить молекулярные механизмы, посредством которых продукты данного гена реализуют свое антиатерогенное действие. Необходимы дальнейшие исследования по изучению вовлеченности гена ZC3HC1 в развитие ОАСНК, а также атеросклероза коронарных и церебральных артерий с оценкой вовлеченности в патогенез болезни показателей клеточной пролиферации структурных компонентов сосудистой стенки. Результаты таких исследований позволят не только понять природу выявленных нами генно-фенотипических взаимосвязей, но и оказаться востребованными в клинической практике ангиологов и сосудистых хирургов в качестве генетических предикторов атеросклероза периферических артерий и маркеров, на основании которых можно осуществлять индивидуальное прогнозирование риска развития рестенозов артерий и выбора способов хирургической реваскуляризации как элементов персонализированной медицины.
Информация о финансировании
Работа выполнена за счет средств Курского государственного медицинского университета.





















Список литературы