Антиаритмический эффект амиодарона на модели адреналовых желудочковых аритмий у крыс с гипергликемией и сочетанием гипергликемии с гиперхолестеринемией
Aннотация
Актуальность: Амиодарон, антиаритмический препарат III класса, показал свою эффективность в отношении желудочковых нарушений ритма, индуцированных адреналином у метаболически-нейтральных животных. Однако, его эффективность на моделях с сахарным диабетом до сих пор не изучена. Цель исследования:Оценить эффект амиодарона на течение адреналин-индуцированных желудочковых аритмий у животных с экспериментальной гипергликемией (условно, сахарный диабет 1-го типа) и сочетанием гипергликемии с гиперхолестеринемией (условно, сахарный диабет 2-го типа). Материалы и методы:Данное экспериментальное исследование проведено на белых нелинейных крысах-самцах массой 180-220 гр. Сахарный диабет 1 типа индуцировали однократным внутрибрюшным введением аллоксана в дозе 135 мг/кг. Сахарный диабет 2 типа воспроизводили путем однократного внутрибрюшного введения аллоксана в дозе 135 мг/кг с последующим ежедневным внутрижелудочным введением 1% масляного раствора холестерина в дозе 40 мг/кг/сут в течение 30 сут. Желудочковые аритмии моделировали внутривенным введением адреналина гидрохлорида 50 мг/кг внутривенно однократно на 30-е сутки экспериментального моделирования диабета. Оценивали изменения на ЭКГ и летальность животных в течение 30 минут; а также уровни глюкозы плазмы и общего холестерина в группах. Результаты:Амиодарона гидрохлорид (5 мг/кг внутривенно, за 1-2 минуты до воспроизведения адреналовых аритмий) не подавлял желудочковую экстрасистолию и желудочковую тахикардию, индуцированные адреналином, у крыс с сахарным диабетом 2 типа, но подавлял желудочковые аритмии у крыс с сахарным диабетом 1 типа, по сравнению с метаболически-нейтральными крысами. Мы полагаем, что снижение антиаритмической эффективности амиодарона может быть объяснено увеличением его токсичности на фоне сопутствующей гиперхолестеринемии, а также отсроченным началом действия антиаритмика. Заключение:Впервые показано снижение антиаритмической эффективности амиодарона в отношении адреналин-индуцированных желудочковых аритмий у крыс с сочетанием гипергликемии и гиперхолестеринемии. Необходимы дальнейшие клинические исследования, чтобы проверить полученные данные и найти эффективную и безопасную дозу амиодарона у пациентов с сахарным диабетом
Ключевые слова: амиодарон, эффективность, сахарный диабет 1 типа, сахарный диабет 2 типа, адреналовые аритмии, аритмии, желудочковая экстрасистолия, желудочковая тахикардия
Введение. Желудочковые нарушения сердечного ритма (ЖНР), способные трансформироваться в фибрилляцию желудочков и привести к внезапной сердечной смерти (ВСС), ежегодно во всем мире уносят около 18 миллионов человеческих жизней [1]. Сахарный диабет (СД) является общепризнанным фактором риска сердечно-сосудистых заболеваний [2] и ВСС [3]. При этом СД обладает риском, эквивалентным ишемической болезни сердца, и обычно поражает сердце посредством кардиальной автономной нейропатии (КАД), ишемической болезни сердца (ИБС) и/или диабетической кардиомиопатии (ДКМ) [4].
И хотя за последние годы достигнут значительный прогресс в интервенционной терапии ВСС, включающей радиочастотную абляцию и аппаратную терапию (имплантируемые кардиовертеры-дефибрилляторы), фармакотерапия до сих пор является основой лечения ЖНР [5]. Среди антиаритмических препаратов амиодарон является самым часто назначаемым [6] и самым мощным агентом III класса, эффективным как при наджелудочковых, так и ЖНР [7]. Однако всё больше сообщений свидетельствуют о низком [8, 9] или отрицательном [10, 11] влиянии амиодарона на ВСС и/или общую сердечную смертность у пациентов со структурными заболеваниями сердца, включая пациентов с СД. Есть основания полагать, что сахарный диабет может компрометировать антиаритмическую эффективность амиодарона и повышать его кардиальную токсичность. В экспериментальном исследовании [12] показано, что аллоксановая гипергликемия снижает антиаритмический эффект трех разных классов антиаритмиков (флекаинида, E-4031 и верапамила) на модели адреналовой аритмии у крыс. В клиническом исследовании [13] показано, что пациенты, имевшие сахарный диабет и получавшие амиодарон перед имплантацией устройства поддержки функции левого желудочка (LVAD) имели неудовлетворительные показатели долгосрочной выживаемости.
Нам не удалось найти исследований, напрямую оценивающих эффективность и безопасность амиодарона в отношении желудочковых нарушений ритма при сахарном диабете, поэтому мы инициировали данное экспериментальное исследование.
Цель исследования. Оценить эффективность амиодарона в отношении желудочковых нарушений ритма на модели адреналовой аритмии у лабораторных животных с экспериментальной гипергликемией (сахарный диабет 1-го типа) и сочетанием гипергликемии с гиперхолестеринемией (сахарный диабет 2-го типа).
Материалы и методы исследования
Лабораторные животные
Все протоколы экспериментов с участием лабораторных животных были одобрены локальным этическим комитетом МГУ им Н.П. Огарёва (протокол № 102 от 31.01.2022г). Эксперименты проведены на 92 белых нелинейных крысах-самцах массой 180-220 гр., которые содержались в стандартных условиях вивария при естественном освещении, свободном доступе к воде и пище. После 1 недели карантина крысы были случайным образом распределены на 3 группы: (1) контроля (метаболически-нейтральные), (2) гипергликемии, условно принятая как сахарный диабет 1 типа (СД 1 типа), (3) гипергликемии и гиперхолестеринемии, условно принятая как сахарный диабет 2 типа (СД 2 типа).
Воссоздание экспериментальных нарушений метаболизма
СД 1 типа у крыс был индуцирован однократным внутрибрюшным введением аллоксана в дозе 135 мг/кг (после предварительной 24-часовой депривации пищи при сохраненном доступе к воде). СД 2 типа воспроизводился путем однократного внутрибрюшного введения аллоксана в дозе 135 мг/кг с последующим ежедневным введением масляного раствора холестерина в дозе 40 мг/кг per os в течение 30 сут, по методу О.В. Артемьевой и А.В. Зорькиной (2005). Группа контроля однократно внутрибрюшинно получала эквивалентный объем 0,9% р-р натрия хлорида и затем - стандартный рацион вивария.
Биохимические исследования
На утро 30-х суток часть животных каждой группы (по 10 из группы) забивали гильотинным способом (после предварительной наркотизации этаминалом натрия в дозе 60 мг/кг внутрибрюшинно однократно) для получения образцов крови из декапитационной раны. В полученных образцах крови исследовали уровень общего холестерина (ОХС) по методу Илька и глюкозы плазмы в реакции с орто-толуидином. Биохимические исследования проводились на фотоэлектрокалориметре КФК-2МП и спектрофотометре СФ-46.
Моделирование адреналовых аритмий
На 30-е сутки эксперимента оставшихся крыс каждой группы сначала наркотизировали этаминалом натрия (60 мг/кг внутрибрюшинно однократно) и после интубации трахеи осуществляли ИВЛ с 1% фторотаном в 100% кислороде. Половине животных каждой группы вводили исследуемый антиаритмик – амиодарона гидрохлорид (5 мг/кг однократно внутривенно), а второй половине - эквивалентный объем 0,9% раствора натрия хлорида. И спустя 1-2 минуты вводили раствор адреналина гидрохлорида в дозе 50 мг/кг внутривенно однократно для моделирования ЖНР.
Оценка антиаритмического эффекта
На протяжении экспериментального моделирования желудочковых дизритмий проводили запись ЭКГ во II стандартном отведении. В течение 30 минут оценивали частоту сердечных сокращений (ЧСС), частоту желудочковых экстрасистол (ЖЭ), желудочковой тахикардии (ЖТ), фибрилляции желудочков (ФЖ), частоту нарушений проводимости и летальность.
Исследование острой токсичности амиодарона
Экспериментальные исследования по определению острой токсичности амиодарона проводили на 120 белых лабораторных мышах обоего пола, массой 18–20 граммов. Нарушения метаболизма (условно СД 1 и СД 2) у экспериментальных групп моделировались по вышеуказанным методикам. Амиодарон вводился внутрибрюшинно. Показатель острой токсичности (LD50) вычисляли по методу Беренса.
Статистическая обработка результатов
Данные представлены в виде таблиц и рисунков. Категориальные переменные представлены в виде чисел и процентов. Непрерывные переменные отображены в виде среднего значения и стандартной ошибки средней. Нормальность распределения оценивали с помощью критерия Шапиро-Уилка. Статистические различия между двумя средними значениями зависимых переменных оценивали с помощью парного t-критерия Стьюдента или Фридмана, в зависимости от нормальности распределения. Различия в независимых непрерывных переменных между двумя группами проверялись на статистическую значимость с использованием t-критерия Стьюдента или U-критерия Манна-Уитни, в зависимости от распределения данных. Различия в независимых непрерывных переменных между тремя и более группами с ненормальным распределением оценивались с использованием критерия Краскала-Уоллиса с последующим тестом Ньюмена-Кейлса. Различия в категориальных переменных проверялись на статистическую значимость с помощью теста χ2. В случае, когда размеры выборки были небольшими (<5%) при анализе таблиц сопряженности был использован точный тест Фишера. Различия считали статистически достоверными при р<0,05. Все статистические исследования проводили в программе Jamovi (версия 2.5.3).
Результаты
- Биохимические показатели животных с СД 1 и СД 2 типа.
Развитие хронической гипергликемии (модель сахарного диабета 1 типа) и сочетанного нарушения метаболизма – хронической гипергликемии с гиперхолестеринемией (модель сахарного диабета 2 типа) подтверждено достоверно повышенными уровнями глюкозы плазмы и общего холестерина у крыс (Табл. 1).
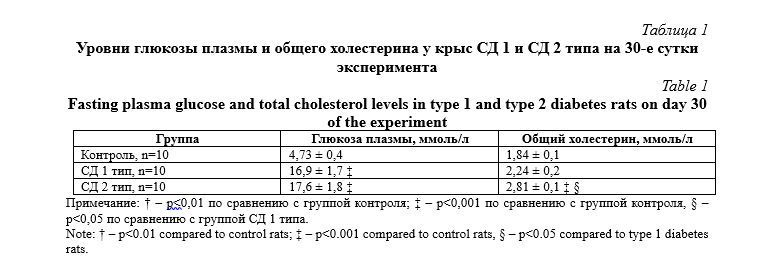
К 30-м суткам, средний уровень глюкозы плазмы крыс с СД 1 был значительно выше чем в группе контроля (16,9±1,7 и 4,73±0,4 ммоль/л, соответственно, р<0,01), тогда как уровень общего холестерина достоверно не различался между данными группами (2,24±0,2 и 1,84±0,1 ммоль/л, в группе СД 1 и контроля, соответственно, р=0,103). Животные с СД 2 имели достоверно повышенные уровни как глюкозы плазмы (17,6±1,8 ммоль/л), так и общего холестерина (2,81±0,1 ммоль/л) по сравнению с группой контроля (4,73±0,4 ммоль/л и 1,84±0,1 ммоль/л, соответственно).
- Антиаритмическая эффективность амиодарона на модели адреналовой аритмии у крыс с СД1 и СД 2 типа.
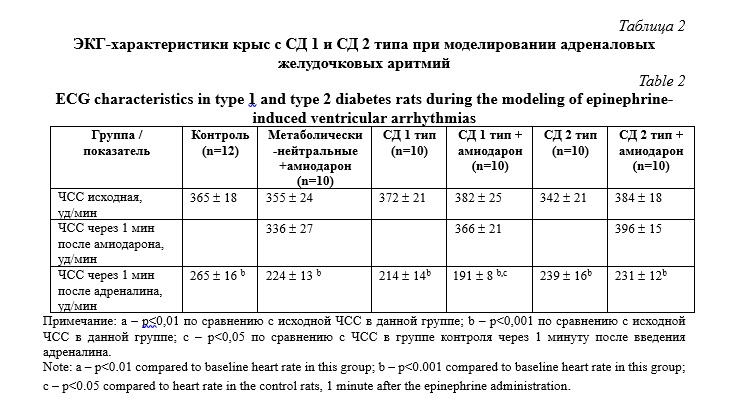
Все исследуемые группы животных исходно имели сопоставимые показатели ЧСС до начала экспериментального моделирования адреналовых аритмий (Табл. 2). ЧСС животных во всех трех группах через 1 минуту после введения амиодарона так же достоверно не отличалась от исходных значений. Через 1 минуту после введения адреналина животным отмечено достоверное снижение ЧСС на 27% и 37%, 42% и 50%, 30% и 40% в группе контроля и метаболически-нейтральных животных, получивших амиодарон, СД 1 типа и СД 1 типа, получавших амиодарон, СД 2 типа и СД 2 типа, получавших амиодарон, соответственно. Стоит отметить, что ЧСС крыс с СД 1 типа, получавших амиодарон, через 1 минуту после введения адреналина была достоверно ниже аналогичного показателя в группе контроля (Табл. 2).
Частота желудочковых аритмий, индуцированных введением адреналина в экспериментальных группах отражена на рисунке 1.
Однократное внутривенное введение амиодарона в дозе 5 мг/кг перед моделированием адреналовой аритмии животным без метаболических нарушений привело к достоверному снижению частоты желудочковых аритмий: ЖЭ зарегистрированы у 3 (30)%, а ЖТ у 2 (20%) метаболически-нейтральных крыс, получавших амиодарон, по сравнению с 11 (92%) и 8 (67%) крысами, соответственно, в группе контроля (не получавших амиодарон) (Рис. 1). Летальность в группе метаболически-нейтральных животных, получавших амиодарон была достоверно ниже, чем в группе контроля (0; 0% и 5; 42% животных, соответственно, p=0,0396). Достоверной разницы в частоте нарушений проводимости среди животных без метаболических нарушений, получавших и не получавших амиодарон не зафиксировано (Рис. 1).
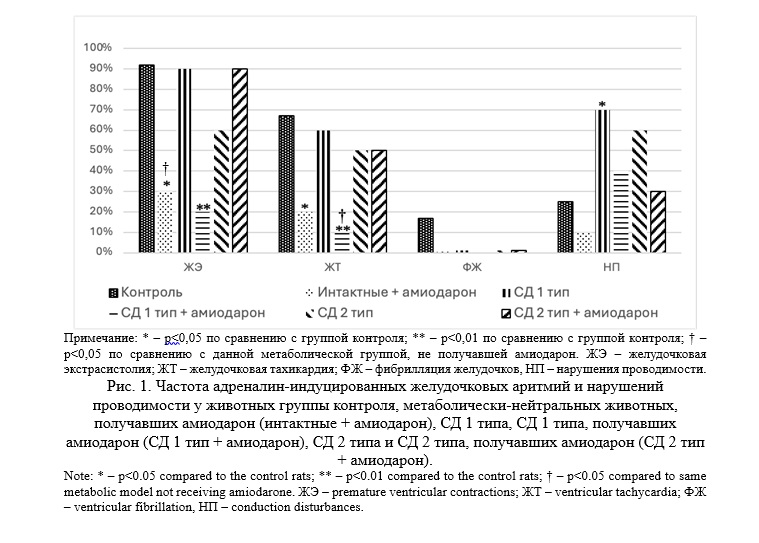
В группе животных с СД 1 типа введение амиодарона привело к достоверному уменьшению частоты ЖЭ и ЖТ (Рис. 1). ЖЭ зарегистрированы только в 2 (20%) случаях по сравнению с 11 (92%) в группе контроля и 9 (90%) – в группе животных с СД 1 типа не получавших исследуемого антиаритмика. ЖТ имело лишь одно (10%) животное по сравнению с 8 (67%) в группе контроля и 6 (60%) в группе крыс с СД 1 типа, не получавших амиодарона. Летальность животных в группе СД 1 типа, получавших амиодарон составила 20% и не отличалась достоверно от группы контроля (42%) и СД 1 типа без введения амиодарона (40%, р=1,0). Частота нарушений проводимости у крыс с СД 1 типа, получавших амиодарон также достоверно не различались от группы контроля и СД 1 типа без предварительного введения амиодарона (Рис. 1).
В группе СД 2 типа, введение амиодарона не привело к достоверному снижению частоты ЖНР (Рис. 1). ЖЭ регистрировались у 9 (90%) животных с СД 2 типа, получавших амиодарон, в сравнении с 11 (92%) – в группе контроля и 6 (60%) – в группе СД 2 типа, не получавших амиодарона. ЖТ имели 5 (50%) животных по сравнению с 8 (67%) в группе контроля и 5 (50%) в группе СД 2 типа, не получавших амиодарона. При этом, у 2 (20%) животных с СД 2 типа, получавших амиодарон возникли пароксизмы устойчивой желудочковой тахикардии, которых не отмечалось в других сериях. Атриовентрикулярные блокады 1-й и 2-й степени развились у 3 (30%) животных; их частота не отличалась от таковой в группе контроля (n=3; 25%) и СД 2 типа, не получавших амиодарона (n=6; 60%). Однако, несмотря на сопоставимую частоту и «отягощенность» ЖНР в группе крыс с СД 2, получавших амиодарон, летальность (n=1; 10%) достоверно не отличалась от группы контроля (n=5; 42%) и животных с СД 2 типа, не получавших амиодарона (n=1; 10%).
- Исследование острой токсичности амиодарона у животных с СД 1 и СД 2 типа.
Эксперимент проведен на 120 белых нелинейных мышах обоего пола, массой 18-20 граммов. Полученные результаты отражены в таблице 3.

Показано, что токсичность амиодарона возрастала в условиях нарушений метаболизма (СД 1 и СД 2 типа) по сравнению с группой контроля. Причем, ЛД50 была наименьшей в группе сочетания гипергликемии с гиперхолестеринемией (СД 2 типа).
Обсуждение. Сахарный диабет является одним из наиболее распространенных хронических заболеваний во всем мире и в большинстве случаев ассоциируется с серьезными сердечно-сосудистыми осложнениями, включая ЖНР, которые значительно повышают риск смерти у пациентов с диабетом. Из-за сложной и многофакторной природы взаимосвязь между СД и сердечными аритмиями еще не до конца понятна. Отклонения, наблюдаемые на ЭКГ и в работе сердца у пациентов с диабетом, в основном связаны с изменениями в работе вольтаж-зависимых ионных каналов, которые являются критическими факторами, определяющими продолжительность и морфологию сердечного потенциала действия. На клеточном уровне при СД удлинение потенциала действия и дефекты сократительной функции обычно возникают из-за сочетания снижения токов K+, измененных токов Na+ и Ca2+ наряду с нарушением внутриклеточного метаболизма Ca2+ в диабетических кардиомиоцитах [14]. Механизмом, с помощью которого гипергликемия способствует электрической нестабильности миокарда желудочков, может быть повышение симпатической активности, увеличение цитозольного Ca2+ кардиомиоцитов или сочетание обоих механизмов [15]. При этом крысы как с СД 1, так и СД 2 типа, по-видимому, имеют схожие нарушения в работе вольтаж-зависимых ионных каналов кардиомиоцитов [14]. В нашем исследовании частота как ЖЭ, так и ЖТ достоверно не отличалась между метаболически-нейтральными крысами, крысами с условным СД 1 и 2 типа (не получавших амиодарон) (Рис. 1), что потенциально свидетельствует об отсутствии значимых различий в задействованных механизмах аритмогенеза, обусловленных работой вольтаж-зависимых ионных каналов.
Традиционно для модификации аномальных ионных токов, и тем самым, устранения сердечных аритмий, используют антиаритмики. Амиодарон, антиаритмический препарат широкого спектра действия, при внутривенном введении оказывает свой эффект за счет нескольких механизмов, включая выраженное ингибирование входящих токов Na+ и Ca2+, а также β-адренергических рецепторов (в меньшей степени) [16]. И хотя данные механизмы эффективны для подавления адреналовых желудочковых аритмий у метаболически нейтральных животных [17, 18], их эффективность при сопутствующих нарушениях метаболизма изучена недостаточно. В настоящем исследовании впервые показан различный ответ на терапию амиодароном между животными с аллоксановым диабетом и сочетанием аллоксанового диабета с гиперхолестеринемией, подвергшихся адреналин-индуцированным ЖНР. У крыс с аллоксановым диабетом наблюдалось значительное снижение частоты и тяжести ЖНР на фоне введения амиодарона, что свидетельствует о его эффективности в этой группе. Данный эффект может быть обусловлен выраженным ингибирующим влиянием амиодарона на Ca2+ каналы и кардиальную автономную нервную систему, за счет повышения тонуса блуждающего нерва и снижения симпатической преганглионарной активности [19]. Напротив, крысы с условным СД 2 типа не продемонстрировали аналогичного терапевтического ответа, что подчеркивает потенциальную резистентность или снижение эффективности амиодарона при сочетании диабета с гиперхолестеринемией. На наш взгляд, различия в ответе на терапию амиодароном могут быть обусловлены рядом факторов.
Во-первых, мы выяснили, что у животных с СД 1 и СД 2 типа, в сравнении с животными без нарушений метаболизма возрастала токсичность амиодарона (Табл. 3). При этом ЛД50 амиодарона была наименьшей в группе с сочетанным нарушением метаболизма (гипергликемия-гиперхолестеринемия), что может гипотетически объяснить кардиодепрессивный эффект амиодарона, способствовавший не только его сниженной эффективности в отношении ЖНР, но и появлению устойчивой желудочковой тахикардии у крыс с СД 2 типа.
В свою очередь более значимое снижение ЛД50 амиодарона у животных с СД 2 типа может быть результатом изменения фармакокинетики и фармакодинамики амиодарона, обусловленных дислипидемией. В нескольких лабораторных [20, 21] и клинических исследованиях [22] показано изменение объема распределении амиодарона в тканях в пользу большего захвата тканями сердца, опосредованного липопротеиновыми рецепторами, что теоретически, может способствовать повышению кардиальной токсичности амиодарона в условиях нарушения липидного обмена.
Еще одним возможным объяснением сниженной эффективности амиодарона в отношении ЖНР при СД 2 типа может служить отсроченное начало действия исследуемого антиаритмика. В исследовании [23] было показано, что антиаритмические эффекты амиодарона у пациентов с СД 2 типа и неконтролируемой фибрилляцией или трепетанием предсердий были отсроченными по сравнению с лицами без диабета (6,8±6,0 часов в группе контроля против 98±14,8 часов в группе СД 2 типа, р=0,0004).
Заключение. Данное исследование показало, что, хотя амиодарон эффективно подавляет ЖЭ и ЖТ, вызванные адреналином у метаболически нейтральных животных и крыс с аллоксановым диабетом, его терапевтическая эффективность снижена у крыс с сочетанием диабета и гиперхолестеринемии. Измененный метаболизм и фармакокинетика амиодарона, обусловленные сочетанием хронической гипергликемии с дислипидемией могут способствовать вариабельному ответу на терапию амиодароном. Мы полагаем, что диабет и связанные с ним нарушения обмена веществ необходимо учитывать при выборе антиаритмической терапии. Дальнейшие исследования на популяции пациентов с сахарным диабетом и сопутствующими нарушениями метаболизма могут помочь в проверке данной гипотезы и определении эффективной и безопасной дозы амиодарона у дынных пациентов.
Информация о финансировании
Финансирование данной работы не проводилось.





















Список литературы