Кардиотокография с элементами искусственного интеллекта (обзор)
Aннотация
Актуальность: Внутриутробная гипоксия плода – это патологическое состояние, характеризующееся недостаточным снабжением тканей плода кислородом, при дефиците последнего имеет место каскад патологических осложнений, включая декомпенсацию, метаболический ацидоз и, в некоторых случаях, смерть. На сегодняшний день инструментальным методом оценки состояния плода и диагностики фетальной гипоксии является кардиотокография. В последние годы появились публикации, касающиеся искусственного интеллекта в области фетального мониторирования. Цель исследования:Оценить роль искусственного интеллекта в области фетального мониторинга или кардиотокографии в диагностике гипоксии или дистресса плода. Материалы и методы:Выполнен обзор литературы, посвященный искусственному интеллекту в области фетального мониторинга в диагностике гипоксии или дистресса плода при беременности и в родах, по источникам литературы в базах данных Pubmed, Elibrary, Scopus за последние 35 лет. Результаты:Анализ данных литературы показал улучшение качества диагностики гипоксических состояний плода при использовании элементов искусственного интеллекта в области кардиотокографии. Модели машинного обучения повышают эффективность прогнозирования состояния плода и имеют более высокую точность диагностики по сравнению с традиционными методами, 96,8-98,0% и 80,0-84,4% соответственно. Заключение:Элементы искусственного интеллекта в области фетального мониторинга или кардиотокографии показывают улучшение качества диагностики гипоксических состояний плода в антенатальном периоде и родах. Модели машинного обучения повышают эффективность прогнозирования состояния плода, точность диагностики систем КТГ на основе ИИ достигает 96,0-98,0%. Современная диагностическая технология на основе искусственного интеллекта в области КТГ может являться виртуальным цифровым помощником для врачей-акушеров в принятии медицинских решений
Введение. Внутриутробная гипоксия плода – это патологическое состояние, характеризующееся недостаточным снабжением тканей плода кислородом и жизненно важными источниками энергии, в частности глюкозой. При отсутствии своевременного восстановления адекватного кислородного обеспечения этот дефицит вызывает каскад патологических последствий, включая декомпенсацию, метаболический ацидоз и, в конечном счете, необратимые повреждения клеток [1].
Гипоксия плода поражает примерно 10% всех беременностей и является причиной 40% перинатальных потерь, подчеркивая ее значимость в современном акушерстве [1-6]. Дистресс плода – патологическое состояние, обусловленное временной или постоянной кислородной недостаточностью, и развивающееся в родах [1, 7-10].
На сегодняшний день инструментальным методом оценки состояния плода и диагностики фетальной гипоксии является кардиотокография [1, 7, 11-15].
Кардиотокография – определение, краткое описание.
Кардиотокография (КТГ) – ведущий метод оценки состояния плода человека и маточной активности (схваток) у женщин. Данный функциональный метод диагностики в акушерстве применяется для мониторинга состояния плода как на протяжении всей беременности, так и в процессе родов. Отсутствие метода точного прогнозирования гипоксии плода диктует развитие фетального мониторинга (американское название) или кардиотокографии (европейское название) [1, 7, 16, 17].
Антенатальная кардиотокография (фетальный мониторинг) – это регистрация изменений частоты сердечных сокращений плода и маточной активности до начала родов. В ходе родов существуют различные факторы, которые могут повлечь за собой возникновение асфиксии иди дистресса плода. Поэтому частоту сердечных сокращений плода и маточную активность контролируют и в процессе родов. Данная методика называется интранатальной кардиотокографией. Сокращения матки могут уменьшить приток крови по пуповине к плоду, что снижает поступление кислорода. Кроме того, эпидуральная анестезия, введение окситоцина, артериальная гипертензия, изменение цвета околоплодных вод или гипертермия у роженицы требуют проведения вышеназванного мониторинга. Это осуществляется с помощью аппарата кардиотокографа, который регистрирует частоту сердечных сокращений плода (тахограмму), маточную активность (токограмму) и шевеления плода (актограмму) на бумаге в виде кардиотокограммы [1, 7, 16, 17, 18].
Выделяют две технологии регистрации ЧСС плода с целью своевременного выявления гипоксии или дистресса плода – электронный допплеровский фетальный мониторинг и электрокардиографию плода (ЭКГ) плода.
При электронном допплеровском фетальном мониторинге регистрируется первоначальный аналоговый допплеровский сигнал тонов сердца плода, полученный ультразвуковым методом, который позже оцифровывается, а каждый кардиоинтервал пересчитывается в ЧСС плода в ударах в минуту. В России данные записи осуществляют на фетальных мониторах Российского ("УНИКОС", Москва, "Сономед", Москва, "Илифия", Москва, "МАК", Челябинск), а также импортного производства ("Huntleig", Великобритания, "GE" США, "PHILLIPS", Евросоюз и др.).
Другая технология - непрямая ЭКГ плода. Она проводится на фетальных мониторах "Monica AN24" (Великобритания) с помощью наружных ЭКГ электродов, которые накладываются на живот матери. Сначала на ЭКГ фильтруют R-зубцы плода от R-зубцов матери, а затем при помощи математического алгоритма каждый кардиоинтервал между R-R зубцами пересчитывается в ЧСС плода в ударах в минуту. Однако данная методика не нашла широкого применения из-за недостаточной надежности по сравнению с ультразвуковой кардиотокографией в диагностике гипоксических состояний плода при беременности и в родах [16, 19]. Существует прямая ЭКГ плода с помощью фиксации спирального электрода Goldtrace Fetal (FSE) на коже головки плода. Она реализована в мониторах "Neoventa" (Швеция), что позволяет получить более качественный сигнал фетальных R-зубцов [20].
Для улучшения фетального мониторинга в течение родов используется подъем сегмента ST и изменения T-волны ЭКГ плода как маркеров дистресса плода [21]. Однако этот прибор применяется только в родах, а в структуре перинатальной смертности ведущая роль принадлежит антенатальной гипоксии плода [22, 23].
Традиционная КТГ с визуальным анализом.
В основе ультразвуковой кардиотокографии имеет место наружный фетальный мониторинг. Кардиографический датчик фиксируется на передней брюшной стенке в области наилучшего выслушивания сердечных тонов плода, а тензометрический датчик для записи сократительной деятельности матки - в области ее дна [1, 7, 18].
Основными анализируемыми параметрами КТГ на сегодняшний день являются базальная частота сердечных сокращений плода (БЧСС), вариабельность ритма (амплитуда и частота осцилляций), акцелерации, децелерации, число шевелений плода в час и маточная активность [1, 7, 17].
Савельева Г.М. с соавторами (2022) выявляют начальные признаки гипоксии плода, использую следующие параметры: снижение вариабельности сердечного ритма, тахикардию (до 180 уд/мин) или умеренную брадикардию (до 100 уд/мин), кратковременную (до 50% записи) монотонность ритма и ослабление реакции на функциональные пробы [24]. При выраженном страдании плода наблюдается выраженная брадикардия (менее 100 уд/мин) или тахикардия (более 180 уд/мин), монотонность ритма (свыше 50% записи), парадоксальная реакция на функциональные пробы (поздние децелерации в ответ на шевеление плода при нестрессовом тесте) или же ее отсутствие [24].
Анализ кардиотокограмм в антенатальном периоде и в родах имеет некоторые различия. В родах согласно рекомендациям Международной федерации гинекологии и акушерства (FIGO) 2015 года типы кардиотокограмм классифицируют на нормальные, сомнительные (подозрительные) и патологические [1, 7, 17]. Нормальный тип КТГ характеризуется базальным ритмом 110-160 уд/мин, вариабельностью 5-25 уд/мин и отсутствием повторяющихся децелераций. Для сомнительного типа характерно отсутствие хотя бы одного из признаков нормального и патологического типов кривой. Патологический тип в свою очередь проявляется базальным ритмом менее 100 уд/мин; сниженной вариабельностью более 50 мин. или повышенной вариабельностью более 30 мин. или синусоидальным ритмом; кроме того, повторными поздними или пролонгированными децелерациями более 30 мин. или более 20 мин., если снижена вариабельность; или наличием одной пролонгированной децелерации более 5 мин. [1].
Кроме описанной выше классификации интранатальных кардиотокограмм по FIGO, существует скрининг антенатального состояния по наличию акцелераций, обусловленных движением плода – нестрессовый тест (НСТ) [24]. Тест называется нестрессовым, так как выполняется до начала родов, когда нет регулярных схваток и плод не подвергается «стрессу» маточных сокращений. Тест считается положительным (реактивным, нормальным), если в течение 20 мин. исследования на КТГ регистрируются не менее 2 акцелераций. Если 2 акцелерации регистрируются за более короткий период времени (более 10 мин), тест прекращают, считая его реактивным. Отмечают, что должно быть зарегистрировано хотя бы одно шевеление плода и отсутствие децелерации в течение записи. Иначе в конце проведения КТГ записи тест считается отрицательным (ареактивным, патологическим) [24].
Современная зарубежная классификация типов НСТ по антенатальной методике кардиотокографии на основе визуального анализа включает такие параметры, как базальный ритм, вариабельность, децелерации, малые акцелерации (до 32 недель гестации) и большие акцелерации (в сроке 32 недели беременности и более). Типы антенатальных кардиотокограмм классифицируют на нормальные, атипичные и патологические [17].
В качестве метода диагностики при неосложненном течении беременности проводят КТГ с 33 недель беременности 1 раз в две недели. При выявлении нарушения сердечного ритма плода в родах для исключения дистресса плода проводят непрерывную КТГ в течение не менее 20 минут. Запись КТГ проводится с 23-й недели беременности при осложненном течении беременности, а также в случаях высокого базального ритма (верхняя граница нормы), низкой вариабельности, отсутствия акцелераций или их низкой амплитуды, частых децелераций [1, 7].
Фетальный мониторинг в родах, а именно в активную фазу родов осуществляется минимум в течение 20 мин. каждый второй час. Дополнительно регистрацию КТГ следует производить при определенных случаях – спонтанном отхождении околоплодных вод, после амниотомии, перед и после применения эпидуральной анестезии. Непрерывная регистрация ЧСС плода начинается со второго периода родов [7].
Метод КТГ в родах может быть периодический или непрерывный. Периодическую регистрацию в родах применяют у женщин без факторов риска нарушений состояния плода. В свою очередь непрерывную регистрацию проводят при определенных факторах риска. Они включают в себя исходные нарушения состояния плода, многоплодную беременность, тазовое предлежание плода, запоздалые или преждевременные роды, сахарный диабет, рубец на матке, изосенсибилизацию по резус-фактору или системе АВ0, родостимуляцию окситоцином, обезболивание в родах, много- или маловодие, преэклампсию, задержку роста плода (ЗРП), нарушение кровотока в системе «мать - плацента - плод», аномалии родовой деятельности, гипертермию в родах и мекониальную окраску околоплодных вод [1, 7].
Предпочтительнее проводить регистрацию ЧСС плода лежа на боку, полулежа, лучше сидя или даже стоя [7]. Кроме того, еще один из анализируемых показателей, на который необходимо обратить внимание – это ЧСС матери и плода. С одной стороны, возможно учащение ЧСС женщины при гипертермии, во время схватки или потуги и она может приближаться к фетальной. С другой стороны, при аритмии плода его ЧСС может снижаться и достигать значений материнской. Для того, чтобы ЧСС матери и плода не накладывались друг на друга на кардиотокограмме на практике используют чаще пульсоксиметрический датчик, позволяющий правильно регистрировать ЧСС матери [7].
Используя при традиционной КТГ с визуальным анализом следующие шесть параметров – базальную ЧСС и вариабельность ритма плода, акцелерации, децелерации, маточную активность (схватки), актограмму, акушерская служба проводит своевременную диагностику нарушений состояния плода при беременности и в родах. Однако точность выявления внутриутробной гипоксии и дистресса плода составляет менее 80-90% [19].
Автоматизированная КТГ с компьютерным анализом.
Визуальная, то есть субъективная оценка кривых КТГ может быть мало достоверной, так как врачи могут трактовать одну кардиотокограмму по-разному. Поэтому в медицинской практике начал использоваться компьютерный анализ, который обеспечивает непротиворечивость результатов и повышает точность диагностики [25, 26, 27].
В России первым применил собственную методику автоматизированной антенатальной кардиотокографии с 1983г. Демидов В.Н. с соавторами (1991, 2008) с компьютерным расчетом ПСП (показатель состояния плода) [25, 26]. Анализатор состояния плода «Уникос» (Москва) производит поправку на сон, определяет длительность исследования и учитывает двигательную активность плода. В настоящее время существует интранатальная версия монитора, которая проводит оценку родовой деятельности (длительность схваток, возникновение гипертонуса матки и аномалии в регулярности, интенсивности и продолжительности сокращений матки), определяет время, необходимое для экстренного родоразрешения в случае возникновения дистресса плода (преждевременная отслойка плаценты, истинный узел пуповины). Чувствительность данного анализа КТГ при выявлении гипоксии плода составила 77%, специфичность – 91,8% и средняя точность – 84,4% [28].
Многолетний опыт применения в родовспомогательных учреждениях Воронежской области автоматизированной системы анализа КТГ по В.Н. Демидову показал достаточно высокую точность оценки состояния плода (до 90%) [19].
Другим способом оценки кардиотокограмм во время беременности являются различные шкалы, которые предполагают бальную оценку кардиотокограмм по сумме измененных и нормальных параметров (Фишер, Кребс) [19]. Система балльной оценки W.Fischer была предложена в 1976 г. Каждому из анализируемых параметров (базальная частота сердечных сокращений, амплитуда осцилляций, частота осцилляций, акцелерации, децелерации) присваивалось от 0 до 2 баллов. По сумме баллов делается заключение о состоянии плода: 8-10 баллов – отсутствие гипоксии у плода; 5-7 баллов – умеренные признаки гипоксии; 4 балла и менее - выраженные признаки гипоксии. Система была модифицирована в 1978 г. Н. Krebs: от 9 до 12 баллов - удовлетворительное состояние плода; от 6 до 8 баллов - гипоксия плода, угрозы гибели в ближайшие сутки нет; 5 баллов и менее – выраженная гипоксия плода, угроза внутриутробной гибели. В последние годы данные шкалы начали использовать в фетальных мониторах с автоматическим расчетом, преимущественно китайского производства. Однако точность оценки состояния плода по данным шкалам остается низкой (70,3%) [19].
Следующая методика автоматического (компьютерного) антенатального анализа КТГ – критерии Dawes-Redman (Доуза-Редмана). Для этого используют не более десяти параметров КТГ – потеря сигнала, шевеления плода в час, частота базального ритма, сокращения, акцелерации более 15 уд/мин, малые акцелерации более 10 уд/мин, децелерации более 20 потерянных ударов, значения кратковременной – КВВ (STV) и долговременной – ДВВ (LTV) вариабельности [29, 30, 31].
Для расчета параметра STV (Short Time Variation) – производится разбиение кривой ЧСС на так называемые эпохи, длительностью 3,75 с. Для каждой эпохи считается среднее значение ЧСС. Затем определяется среднее значение модуля разности ЧСС для соседних эпох, что соответствует величине STV. В норме параметр STV составляет более или равно 4 мс. Если этот показатель равен 3 мс прогноз гибели плода составляет 29%, если STV менее 2,5 мс – 72% соответственно. LTV (Long Time Variation) – долговременная вариабельность, определяется как разница между минимальным и максимальным значением ЧСС. Этот параметр также называется амплитудой осцилляций [30, 31]. Точность оценки состояния плода по критериям Dawes-Redman в антенатальном периоде составляет не более 91,0% [19].
Появились работы, освещающие автоматический анализ трудно интерпретируемых ритмов плода. Один из методов - спектральный анализ, который был использован в работе Ricardo S.C. et al (2024) [32]. Модели, в основе которых данный метод, способны выявлять синусоидальный тип кардиотокограмм или псевдосинусоидальный, связанный с артефактами и помехами в ходе исследования. Наиболее важной переменной для классификации сигналов было значение PE (potential energy) в частотном интервале. Значение PE менее 0,2965 классифицировало сигналы как нормальные; значение PE, попадающее в диапазон (0,2965-0,4792); и кратковременная изменчивость, превышающая 0,0992, классифицировали сигналы как псевдосинусоидальные. Сигналы классифицировались как синусоидальные, если они удовлетворяли любому из следующих критериев: значение PE больше или равно 0,4792 или значение в диапазоне (0,2965-0,4792) и кратковременная изменчивость меньше или равна 0,0992. Частота обнаружения синусоидального, псевдосинусоидального и нормального ритма составила 92,3%, 88,8% и 97,3%, соответственно. Чувствительность данного метода составила для синусоидального или псевдосинусоидального ритма плода 100%, а специфичность – 97,3% [32].
Giulio Steyde et al. (2024) также описывает применение спектрального метода анализа ЧСС плода [33]. В работе исследовали 2178 записей КТГ у женщин в сроках гестации от 32 до 38 недель беременности с гестационным сахарным диабетом и задержкой роста плода. Результаты показывают, что спектральный метод лучше дифференцирует патологический ритм плода от нормального по сравнению с другими математическими методами [33].
Все вышеперечисленные модели основаны на применении классических методов математики, статистики с использованием набора из десяти или чуть более параметров КТГ.
Искусственный интеллект. Терминология. Классификация.
Термин «искусственный интеллект» (ИИ) был впервые предложен Джоном Маккарти в «Дартмутском летнем исследовательском проекте по искусственному интеллекту» в 1955 году. Он определил интеллектуальную функцию как вычислительную составляющую способности достигать целей. Само определение искусственного интеллекта Маккарти объяснил, как науку и технологию создания интеллектуальных компьютерных программ.
В последние годы ИИ стал шире применяться в медицинской практике. Акушерство и перинатология не стали исключением, где ИИ начал использоваться для повышения эффективности перинатальной диагностики и снижения риска перинатальной смертности [34].
К основным направлениям ИИ относят машинное обучение (Machine Learning – ML), обработка естественного языка (Natural Language Processing – NLP) и роботизированная медицина [34]. Методы ML (дерево решений – DT, «случайный лес» – RF, метод опорных векторов – SVM и наивный байесовский классификатор) необходимы для автоматизированного создания моделей, предназначенных для решения большого количества задач, например, классификация пациентов по группам риска на основе анализа структурированных данных. DT и RF используются для классификации и прогнозирования. RF – это метод ансамблевого обучения для классификации и регрессии. Построив множество DT и суммировав выходы каждого слабого отдельного дерева, RF исправляет проблему перенапряжения в DT [35]. Такой метод ИИ, как машинное обучение, активно внедряется и для прогнозирования многих патологических состояний [36]. Разработано и глубокое машинное обучение (DL) на основе нейронных сетей ANN. Распространенные разновидности DL – сверточная нейронная сеть (CNN), рекуррентная нейронная сеть (RNN) и глубокая нейронная сеть (DCNN). CNN, например, хорошо работает с большим количеством объектов и при обработке изображений [35]. Значительная роль нейронных сетей в сегодняшнем мире отражена во многих публикациях [37].
Другой подвид машинного обучения – NLP (Natural language processing). Он в свою очередь позволяет извлечь значимую информацию из неструктурированных клинических данных, таких как электронные медицинские карты, чтобы дополнить ими структурированные данные. Процесс NLP включает обработку текста и его классификацию [35]. Некоторые методы ИИ будут освещены ниже, а также перечислены в работе М.В.Мокшанова (2024) “Применение искусственного интеллекта в анализе данных: обзор текущего состояния и будущих направлений” [38].
Искусственный интеллект и кардиотокография.
Интерпретация КТГ по-прежнему остается серьезной проблемой из-за высокой частоты ложноположительных результатов и низкой чувствительности. Применение методов ИИ в перинатологии расширяет возможности диагностики гипоксических состояний плода. На данном этапе такие исследования малочисленны, единичны по источнику и ретроспективны. Ниже на рисунке 1 представлена (Ivshin et al., 2020) концептуальная схема применения методов ИИ в перинатологии [35].
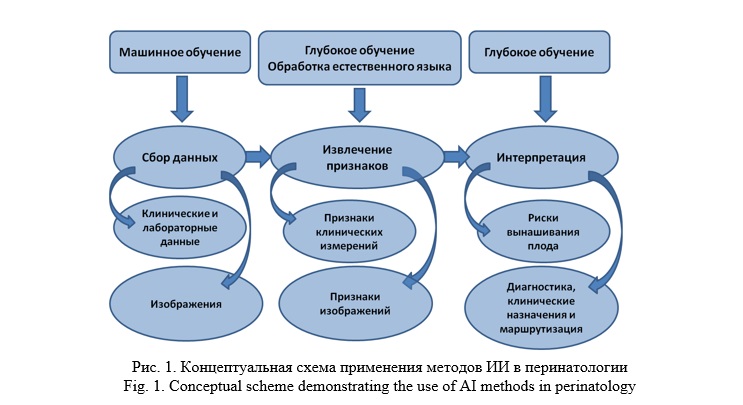
Chen C. et al. (2023) отмечают возможность внедрения направлений ИИ, таких как машинное обучение (ML) и глубокое обучение (DL), в профессиональной сфере акушеров-гинекологов и использования в клинической практике [39].
Kadarina TМ. et al. (2023) в своей работе также отмечают значимую роль машинного обучения в сфере акушерства и гинекологии [40].
В последнее десятилетие доступность больших клинических баз данных, а также появление методов машинного и глубокого обучения в здравоохранении привели к резкому росту числа исследований с применением этих методов для анализа сигналов в кардиотокографии [41]. Melaet R. et al. (2024) также описывают значение моделей на основе ИИ в выявлении патологического типа КТГ [42].
Далее будут освещены публикации, посвященные КТГ и элементам ИИ, представляющие ценность для практикующих специалистов в области акушерства и гинекологии.
В своем исследовании Dlugatch R. et al. (2024) рассмотрели использование метода кардиотокографии на основе искусственного интеллекта DSS (decision support system) [43]. В работе были приведены некоторые условия, которым должна соответствовать КТГ на основе искусственного интеллекта. К ним отнесли точность и эффективность оценки рисков, способность к персонализации и индивидуализированной медицине, отсутствие значимости в отношении типа учреждения, разрабатывающего технологии, прозрачность процесса диагностики. В основе данной разработки - система поддержки принятия решений на основе искусственного интеллекта AI-DSS (Оксфордская система OxSys). Это интеллектуальная компьютеризированная система, которая помогает специалистам в принятии более надежных решений и более точной диагностике патологических состояний плода [43].
O'Sullivan ME. et al. (2021) отмечают, что современные компьютерные системы, использующие более продвинутые методы машинного обучения, обладают анализом широкого диапазона [44]. Среди преимуществ – постоянная доступность и отсутствие влияния на них человеческих факторов, таких как рассеянность, усталость, предвзятость, когнитивная перегрузка и страх причинить вред. Современная система Omniview-SisPorto, версии 3.5 классифицирует КТГ на четыре класса (нормальная, сомнительная, патологическая и претерминальная) на основе рекомендаций FIGO. В основе ее работы – глубокое машинное обучение DL, а именно многомасштабная свёрточная нейронная сеть – MCNN. Данная система позволяет определять поздние, длительные или повторяющиеся децелерации, сниженную вариабельность. Результаты исследований показали, что совпадение между заключениями человека и компьютерной системой обнаружения сокращений, акцелераций и децелераций составило 87, 71 и 68% соответственно [44].
Spairani E. et al. (2023) для анализа кардиотокограмм начали использовать систему, в основе которой лежат Марковские модели – Hidden Markov Models (HMM) [45]. Это классическая модель машинного обучения. Данная система анализирует каждый отрезок кардиотокограммы и извлекает небольшой набор признаков – покой или активность плода, чтобы в дальнейшем определить состояние плода. После изучения сигналов 35 кардиотокограмм, относящихся к разным срокам беременности, были получены автоматические заключения состояния плода. Общее соответствие между прогнозами HMM и заключениями врача составило 90% [45].
Georgieva A. et al. (2022) отмечает одно из преимуществ вышеперечисленных систем, работа которых основана на ИИ - их возможность в ходе обработки медицинских сигналов быть устойчивыми к внешним артефактам (шуму и помехам) [46].
Как многим известно, КТГ зачастую имеет решающее значение для оценки состояния плода, а для точной оценки необходим хороший (без артефактов или помех) допплеровский сигнал тонов сердца плода. Современный алгоритм расчета частоты сердечных сокращений (ЧСС) плода, основанный на автокорреляции допплеровского ультразвукового сигнала, часто приводит к периодическим сбоям из-за его неспособности точно дифференцировать сигналы тонов сердца от шума и помех. Поэтому Zeng R. et al. (2021) разработали классификацию допплеровских ультразвуковых сигналов по типам на основе ИИ [47]. В исследовании использовали одномерную сверточную нейронную сеть (1D CNN) для обработки сигналов, а именно сверточные слои (convolutional layer, CNN). Классификация включала в себя: одиночное сердцебиение плода, артефакт, сигнал низкого уровня и множественные сердечные сокращения. Разделение ультразвуковых сигналов на различные типы позволяет оценивать параметры, недоступные при обычном мониторинге плода. Например, различие между частотой сердечных сокращений матери и плода. Точность результатов составила 79,6-80,9%. Тем не менее, система ИИ не позволяет классифицировать сигналы со 100% точностью и все же может принять артефакт за сердцебиение плода, поэтому необходимы дальнейшие исследования [47].
Zeng R. et al. (2021) говорит о том, что повысить точность диагностики можно путем дополнения в анализ сигнала маточных сокращений или схваток [47]. Данная модель ИИ более эффективна во время родов. Учитывая более высокую вероятность потери КТГ сигнала в ходе родов, интеграция этой модели может улучшить качество анализа кардиотокограмм [47].
Hirono Y. et al. (2024) также отмечают клиническую ценность данной методики, которая заключается в том, что она потенциально позволяет выявлять аномалии развития плода во время мониторинга. Например, возможна диагностика аритмий плода, которые ранее выявлялись только с помощью ультразвуковых диагностических устройств или электрокардиограммы плода [48].
Gude V. et al. (2022) в своем исследовании отразили, что компьютерный анализ данных КТГ при помощи ИИ уменьшает субъективность оценки состояния плода [49]. Авторы разработали интегративную модель, которая идентифицирует закономерности в таких параметрах, как ЧСС плода и сокращения матки, а затем с высокой эффективностью прогнозирует соответствующие значения с помощью модели глубокого обучения, а именно разновидности рекуррентных нейронных сетей – Long Short-Term Memory (LSTM), с целью классификации и прогнозирования внутриутробного состояния плода. Данные значения впоследствии классифицировались с помощью ансамблевого классификатора, который является прикладным направлением ИИ. Оценка состояния плода проводилась с использованием искусственных нейронных сетей (artificial neural network – ANN). Параметры КТГ (ЧСС плода и сокращения матки) обрабатывались при помощи модели глубокого обучения, которая извлекает необходимые признаки и классифицирует их с помощью алгоритма сборки, состоящего из «случайного леса» (RF) и метода опорных векторов (SVM). В ходе исследования было выявлено, что метод опорных векторов и нейронная сеть обладают более высокой точностью, чувствительностью и специфичностью в диагностике патологического состояния плода, чем «случайный лес». Алгоритм данной классификации показал точность теста – 85%. Авторы сообщили, что производительность модели может быть улучшена путем обучения на большом количестве наблюдений [49].
Еще один нейроклассификатор FCM-ANFIS (нейро-нечеткая система логического вывода ANFIS), описанный Fei Y. et al. (2020) [50]. Он объединяет в себе теорию нечетких множеств и нейросетевые технологии, а также основан на кластеризации данных КТГ для антенатального мониторинга плода. Данная модель обладает способностью к адаптации в условиях сложности при интерпретации антенатальных КТГ. FCM-ANFIS показала самую высокую точность, скорость запоминания и чувствительность. Также в отличие от других моделей данный нейроклассификатор имел самый низкий уровень ошибок в классификации и снижал вероятность неправильной классификации, например, «сомнительных» типов КТГ и «нормальных». В заключение следует отметить, что модель FCM-ANFISM превзошла традиционные методы машинного обучения по мнению авторов в интерпретации КТГ с помощью ИИ. Точность диагностики нейроклассификатором составила 87,01% [50].
В связи с тем, что в настоящее время в клинической практике оценка КТГ в основном проводится путем визуального анализа результатов зачастую возникает ошибочная интерпретация реального состояния плода. Spairani E. et al. (2022) отмечают, что внедрение КТГ-анализа на основе ИИ снизило бы субъективность интерпретации результатов КТГ [51]. В своей работе авторы показали, что система ИИ проводит дихотомическую классификацию (нормальные и патологические типы КТГ) с помощью гибридной архитектуры нейронной сети, состоящей из многослойного персептрона (MLP) и сверточной нейронной сети (CNN). Известно, что классификационные возможности методов искусственного интеллекта лучше всего проявляются только при работе с большими объемами данных, поэтому для такого исследования было необходимо значительное количество кардиотокограмм, чтобы повысить эффективность результатов работы. Авторами КТГ проводилась с помощью фетальных мониторов Philips и Corometrics, оснащенных ультразвуковым датчиком и трансабдоминальным токодинамометром. Исходные сигналы передавались данными устройствами в программное обеспечение 2CTG2, которое сохраняло данные ЧСС плода и маточной активности с частотой дискретизации 2 Гц. Каждое исследование КТГ длилось не менее 60 минут. Затем медицинская группа классифицировала каждую запись на нормальную и патологическую. Различные числовые коды были связаны с различной внутриутробной патологией, что упрощало извлечение записей, относящихся к различным категориям из всей базы данных. Нейронная сеть состояла из двух ветвей: MML, получающей массив из 15 регрессоров, и CNN, получающей набор изображений размером 64 × 64. Последние были получены путем нескольких преобразований. Средняя точность, достигнутая одним MLP в ходе 30 тренировочных испытаний на 2800 тестовых примерах, составила 75,5%, т.е. 2115 правильных классификаций против 685 ошибочных. В результате этой работы были получены 17483 записей КТГ – 7733 нормальных и 9750 патологических. Патологическая группа включала в себя данные о пациентках с различными заболеваниями как материнского, так и внутриутробного происхождения, такими как сахарный диабет, пороки развития, задержка роста плода (ЗРП) и т.д. Поскольку цель исследования заключалась в разделении здоровых плодов и патологических, каждая запись в наборе данных была разделена на две категории. Записи, относящиеся к группе физиологической беременности (нормальные), были обозначены 0, а записи, относящиеся к патологическим, были обозначены символом 1. Затем сигналы ЧСС плода были преобразованы в набор изображений. CNN анализировала двумерные объекты (изображения) путем кодирования информационного содержимого сигнала сердцебиения плода в 2D. Точность предложенной нейронной сети достигла 80,1% [51].
Liang H. et al. (2022) отобразили современный метод классификации, использовав модели 1D-CNN и GRU (Gated Recurrent Unit), для извлечения абстрактных характеристик сердцебиения плода и сигналов сокращения матки [52]. Для оценки выбрали несколько оценочных показателей, точность которых составляла 96%, чувствительность – 95%, а специфичность – 96%. Смысл модели GRU заключается в анализе сигналов ЧСС плода и впоследствии классификации состояния плода. Полученные сигналы обрабатывались при помощи 2D-CNN и преобразовывали одномерную информацию в двумерные частотно-временные изображения. Модель GRU обладает более простой структурой сети и меньшим объемом вычислений, кроме того, ее производительность аналогична LSTM (разновидность RNN). Эксперимент показал, что данная разработка эффективна и может обеспечить врачам более стабильную, эффективную и удобную диагностику состояния плода [52].
Такие же направления ИИ (CNN) использовались и в исследовании Aswathi Mohan PP. et al. (2023) [53], а мультимодальные сверточные нейронные сети в работе Petrozziello A. et al. (2019) [54].
Имеют место работы, посвященные такому осложнению, как дистресс плода, а именно его возможным предикторам.
Mendis L. et al. (2023) сообщают, что они первыми обобщили инновационные методы анализа КТГ в своем обзоре [55]. Ими были описаны физиологические методы классификации, которые использовались в автоматизированных фетальных мониторах для выявления нарушений состояния плода. Данный обзор актуален, так как дистресс плода - это наиболее распространенная причина мертворождения во всем мире. Ее возникновение связано с определенным механическим давлением на плод во время родов, что снижает поступление кислорода к плоду. Низкий уровень кислорода ведет к перестройке аэробного метаболизма на анаэробный. В результате этого накапливается кислота, которая оказывается негативное влияние на клетки головного мозга плода. Это может привести к травме головного мозга и даже детскому церебральному параличу. Таким образом, одновременный мониторинг ЧСС плода и сокращений матки с помощью КТГ может помочь клиницистам оценить, как течение родов, так и состояние плода. Авторы отмечают, что для такого анализа КТГ и для эффективного прогноза очень важно качество входных сигналов ЧСС плода и сокращений матки. Методы глубокого обучения работают непосредственно с необработанными сигналами КТГ. Данный процесс направлен на извлечение соответствующей информации или характеристик из исходных сигналов КТГ. Данные выделенные параметры служат индикаторами состояния плода, позволяя медицинским работникам или современным моделям с ИИ контролировать и оценивать клиническую ситуацию. Авторы указывают, что на сегодняшний день модели могут классифицировать входные сигналы ЧСС плода и маточной активности. Кроме того, разработаны искусственные нейронные сети. Эти очень мощные модели способны изучать сложные паттерны и взаимосвязи в данных с помощью нейронных слоев. В этой области была продемонстрирована эффективность 1D CNN. Этот тип CNN может обрабатывать временные ряды данных ЧСС плода, извлекая определенные признаки и классифицируя сигналы на нормальные или патологические. Кроме того, при разработке функциональных возможностей систем ИИ необходимо учитывать зашумленность сигнала и низкую частоту дискретизации, что обеспечивает максимально возможную точность подсчета ЧСС плода [55].
Alotaibi D. et al. (2024) в свою очередь упоминают применение машинного глубокого обучения и нейронных сетей [56]. Дистресс плода – это тяжелая патология, которую необходимо своевременно диагностировать, чтобы снизить перинатальные осложнения. Методы непрерывного мониторинга необходимы для наиболее раннего выявления такой патологии. В данном обзоре подчеркивается важность анализа данных КТГ с использованием различных методов искусственного интеллекта MLT и DLL. Они позволяли классифицировать случаи гипоксии плода на острую или хроническую. Более того, благодаря ИИ были поставлены более точные заключения и разработаны индивидуальные схемы лечения. В исследовании использовался набор данных, состоящий из 300 сигналов КТГ, запись которых длилась 20 минут, с использованием программного обеспечения для анализа ЧСС плода. Модель ANN идентифицировала три состояния плода (нормальное, сомнительное, патологическое) [56].
Francis F. et al. (2024) в своей статье затрагивает такие же направления ИИ [57], как и Harish S. et al. (2024) [58], а именно машинное обучение и глубокое машинное обучение.
Темой гипоксии плода заинтересован и Tarvonen M. et al. (2024) [59]. В своей работе он отображает возможность выявления и оценки гипоксии плода при помощи современных технологий ИИ. Так, новая методика ML SALKA с высокой чувствительностью и специфичностью определяет особенности ЧСС плода во время родов. SALKA распознает потенциальные ранние признаки дистресса плода. Чувствительность теста SALKA составила 0,981, показатель положительного прогноза – 0,822 (95%), а показатель ложноотрицательного результата – 0,01 (95%) [59].
Frasch MG. et al. (2023) отмечает, что искусственный интеллект позволяет разработать инструменты поддержки принятия клинических решений при ведении родов [60]. Апробация и внедрение таких инструментов может снизить частоту и тяжесть перинатальных травм головного мозга. Согласно недавнему отчету Национальной службы здравоохранения Великобритании (NHS) 70% внутриутробных травм головного мозга можно было бы предотвратить, если бы специалисты вовремя отреагировали на нарушения в родах, например, на дистресс плода [60].
M’Barek IВ. et al. (2023) представили DeepCTG 1.0 – модель для прогнозирования гипоксии с помощью КТГ [61]. В ее основе лежит предварительная обработка сигналов, извлечение функций и линейная интерполяция. Для улучшения предварительной обработки сигналов было предложено сначала определять частоту сердечных сокращений матери, которая иногда ошибочно регистрируется монитором вместо ЧСС плода. Несмотря на эти ограничения, авторы пришли к выводу, что их модель работает несколько лучше, чем другие модели, основанные на относительно простых статистических моделях (логистическая регрессия / методы опорных векторов). Для расчета необходимых характеристик изучали кардиотокограммы за последние 30 минут перед родоразрешением. В работе исследовали 552 записи КТГ с соответствующими данными о матери и плоде (срок беременности, возраст матери, паритет родов) и состоянии плода (рН крови плода, оценка по шкале Апгар через 1 и 5 минут, вес). Случаи с последующим кесаревым сечением не учитывались в работе. Это связано с тем, что между окончанием записи КТГ и моментом оперативного родоразрешения был достаточный промежуток времени. С другой стороны, исключение этих случаев может привести к очень сильному искажению результатов отбора, что отрицательно скажется на эффективности модели при ее использовании в клинической практике. Исследователи отмечают, что этот вопрос ранее не рассматривался в литературе, и необходимо провести дополнительные исследования, чтобы учесть роды путем кесарева сечения при построении данной модели. Более того, важно указывать причину, по которой было проведено оперативное родоразрешение. Коэффициент полезного действия модели составил 0,74. Это позволяет получить гораздо более низкую частоту ложноположительных результатов по сравнению с заключениями медицинских специалистов (12% против 25%). Дальнейшие исследования должны быть направлены на оптимизацию системы для улучшения раннего выявления гипоксии плода, например, путем использования сигнала на ранних стадиях родов для прогнозирования исхода родов [61].
Sajal B. (2021) обращает внимание, что основной причиной перинатальной смертности сегодня являются антенатальные осложнения [62]. Данную патологию можно легко выявить при беременности с помощью нестрессового теста. Но сегодня все большую актуальность приобретают модели машинного обучения, которые выступают в качестве системы поддержки принятия клинических решений. Они способны помочь специалистам в принятии своевременных и более обоснованных решений. Было собрано около 1800 записей КТГ в третьем триместре беременности. Эти данные были обработаны с помощью алгоритма отбора признаков для выявления важных переменных в наборе. После чего этот набор данных был случайным образом разделен на 2 независимые выборки. В качестве анализа был выбран алгоритм «случайного леса», который точно классифицировал кардиотокограммы на нормальные, подозрительные или патологические. В результате было выделено несколько категорий. Из них 77,85% нормальных, 19,88% подозрительных и 8,28% патологических. Авторы указывают, что данная модель может быть использована медицинскими работниками для выявления беременных женщин группы высокого риска и принятия решения о том, какая медицинская помощь должна быть им оказана [62].
Этот же метод классификации c помощью «случайного леса» продемонстрирован в исследовании Chen M. et al. (2022) [63]. Они упоминают алгоритм Apriori. Он основан на поиске частотных множеств элементов в наборе данных и построен на ассоциациях и корреляциях между наборами элементов. После чего уже происходит классификация [63].
Все современные направления искусственного интеллекта могут использоваться не только для своевременного выявления гипоксии плода, но и предотвращения более тяжелых осложнений, которые будут упомянуты ниже.
Несмотря на существование прямой связи между патологическими картинами КТГ и впоследствии неблагоприятными исходами беременности, многие специалисты не в состоянии распознать сложные паттерны ЧСС плода и высокие риски, такие как асфиксия, ЗРП (задержка роста плода) и мертворождение. Jones GD. et al. (2024) сообщили о разработке первого алгоритма машинного обучения для выявления беременностей высокого риска с сопутствующими неблагоприятными исходами (преждевременные роды), в основе которого лежит мониторинг сердечного ритма плода с помощью ИИ [64]. В ходе работы были получены данные о ЧСС плода с исходами преждевременных родов и с выявленным впоследствии неблагоприятным состоянием новорожденных. Используя клинически подтвержденный алгоритм ИИ, авторы из каждой кардиотокограммы выделили семь различных паттернов сердечного ритма плода, которые затем были отфильтрованы от артефактов. Шесть алгоритмов машинного обучения были обучены с использованием определенного алгоритма (классификатор на основе «случайного леса»), чтобы идентифицировать каждую КТГ как нормальную или патологическую с вероятностью преждевременных родов. В ходе исследования было определено 4867 патологических кардиотокограмм с неблагоприятным исходом и 4014 записей, отражающих нормально протекающую беременность. Эпизоды высокой вариабельности были выше в группе с нормальным исходом (р<0,001), в то время как эпизоды низкой вариабельности оказались значительно выше в группе с преждевременным неблагоприятным исходом (р<0,001). Чувствительность составила 76,2%, специфичность 87,5%, что указывает на высокую способность прогнозировать исходы беременности. Таким образом, данное исследование успешно продемонстрировало, что алгоритмы машинного обучения способны выявлять преждевременные роды высокого риска с сопутствующими неблагоприятными исходами при помощи мониторинга сердечного ритма плода. Эти результаты показывают высокий потенциал машинного обучения в повышении точности и эффективности дородового мониторинга плода, особенно в случаях высокого риска, когда своевременное вмешательство имеет решающее значение [64].
В своем исследовании Frasch MG. et al. (2021) описывают современный механизм глубокого обучения для предотвращения тяжелых осложнений состояния плода [65]. В его основе лежит своевременное выявление на кардиотокограмме критической точки «А» и предотвращение точки «В», что отражает декомпенсированное состояние плода. В точку «А» отнесли такие показатели, как появление децелераций, чрезмерная активность матки и т.д. К точке «В» отнесли снижение вариабельности, учащение сердцебиения плода и другие. Среди мер, которые разработчики предлагают принять в случае обнаружения точки «А», например, уменьшение дозы окситоцина, оценка возможности безопасных вагинальных родов. В ходе исследования модель достигла точности 93,6% [65].
Среди методов машинного обучения представлены и такие, как линейная интерполяция и фрактальный анализ.
Исследование, проведенное Zhong M. et al. (2022) посвящено оценке состояния плода с помощью ИИ (UNet – сеть глубокого обучения) [66]. В работе авторы учитывали морфологические характеристики сигналов и использовали традиционные методы фильтрации сигнала от артефактов. Алгоритмы для автоматизированного анализа ЧСС плода вначале вычисляли базальный ритм ЧСС плода, а затем эпизоды акцелераций и децелераций. Исследование показало, что если точно рассчитать базальный ритм ЧСС, то можно определить все патологические эпизоды, за исключением синусоидальных паттернов. Записи КТГ были сделаны на устройствах производства Lian-Med Technology Co., Ltd. (Гуанчжоу, Китай). Также были использованы ультразвуковой допплеровский фетальный монитор Lian-Med F3 (LM-F3), система центрального акушерского мониторинга Lian-Med (LM-ObVue) и система управления акушерской информацией Lian-Med (LM-OBIS). Монитор F3 использовался для получения данных КТГ, ObVue использовался для помощи врачам в определении состояния плода, а OBIS - для сбора и записи информации из электронных медицинских карт беременных женщин. В ходе работы исследователи собрали в общей сложности 43888 записей КТГ в период с января 2012 по декабрь 2020 года. Все беременные женщины были старше 18 лет и родили живых доношенных детей. Для того, чтобы получить высококачественные сигналы ЧСС плода были соблюдены следующие правила: одноплодная беременность; частота потери сигналов составляла менее 10% за 10 минут; роды в сроке 36-42 недель гестации; общая продолжительность записи КТГ от 60 до 90 минут [66].
Устройство на основе искусственного интеллекта CTGNet отслеживало несколько параметров. К ним относится ЧСС плода, сигнал сокращения матки, профиль движений плода и т.д. Затем данный аппарат классифицировал сигналы ЧСС плода и автоматически рассчитывал базальный ритм. В данном устройстве также используется UNet – это сеть глубокого обучения, в основе которой имело место структура кодирования-декодирования. Кроме того, для уменьшения шума в сигналах применили линейную интерполяцию. Дифференцировать ЧСС плода на патологическую и нормальную помогает также фрактальный анализ. Он исследует природу долгосрочных корреляций сигнала вариабельности сердечного ритма плода [66].
Такой же фрактальный анализ для определения ЧСС плода был использован в работе Ponsiglione AM. et al. (2021) и отнесен к нетрадиционому анализу [67].
Другой метод оценки ЧСС плода FHR-LINet использовался для быстрого выявления нарушений внутриутробного состояния плода. Он примерно на 25% эффективнее по сравнению с современной мультимодальной сверточной нейронной сетью. Данная диагностическая система позволила обеспечить своевременное выявление дистресса плода и предотвращение риска перинатальной смертности [65].
Ниже на рисунке 2 представлена (Frasch M.G. et al., 2021) блок-схема анализа сердечного ритма плода с использованием искусственного интеллекта CTGNet [65].
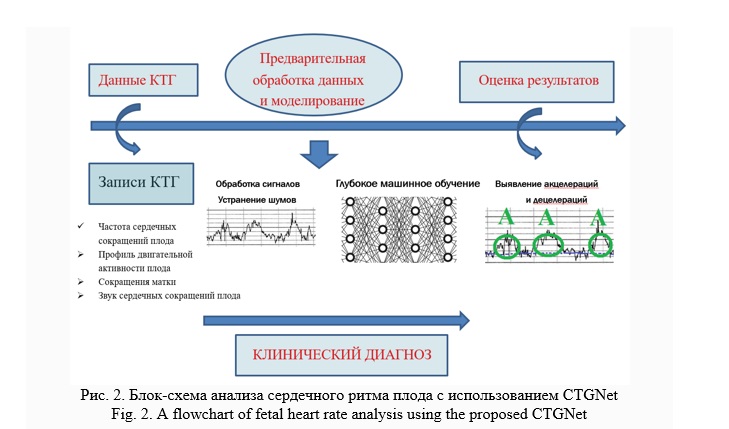
Одним из показателей ИИ, отражающим тактику врача акушера-гинеколога, является time to predict (TTP). Он описан в статье Mendis L. et al. (2024) о применении метода глубокого обучения для предотвращения субъективной оценки состояния плода [68]. Используя в своей работе данный показатель, авторы на 25% сокращают время, необходимое для выявления патологии плода, по сравнению с современной мультимодальной сверточной нейронной сетью (MCNN). Чувствительность – 20% ложноположительных результатов. Преимущество данной диагностической системы в том, что она потенциально обеспечивает более раннее вмешательство при нарушениях внутриутробного состояния плода и улучшает клинические результаты [68].
Sahin H. et al. (2020) отмечают, что роль алгоритмов машинного обучения в выявлении заболеваний становится все более важной в настоящее время [69]. Результаты экспериментов показали, что классификатор с использованием ансамбля пакетов показал удовлетворительные результаты, а при использовании «случайного леса» имел лучшие результаты с точностью 99,2% [69].
Существуют и другие модели для оценки состояния плода. Например, модифицированная модель GANomaly была создана Bertieaux J. et al. (2022) для обнаружения аномалий в сигналах КТГ при помощи структуры кодер-декодер с дискриминатором, что сводит к минимуму ошибки при изучении сигнала КТГ [70].
Еще одна модель CTGGAN (Generative Adversarial Networks – порождающие состязательные сети) предложена Zichang Yu et al. (2024), которая использует генерирующие состязательные сети (GANs) для анализа сигналов ЧСС плода [71].
CCWGAN-GP-нейронная сеть, разработанная Zhang Y. Et al. (2022), в основе которой лежит классификатор состояния плода, способен работать с достаточно большой выборкой по сравнению с другими системами, поэтому точность на 12% выше соответственно [72].
Другим методом анализа состояния плода является алгоритм компьютерной диагностики ацидоза плода (Hybrid-FHR), описанный Zhao Z. et al. (2024), который помогает врачам принимать своевременно решения для снижения осложнений [73]. Для извлечения пространственно-временного представления признаков одномерных сигналов ЧСС плода была разработана магистральная модель многомасштабной временной сверточной сети сжатия и возбуждения (SE-TCN) на основе расширенной причинно-следственной свертки. Она эффективно фиксировала долгосрочную зависимость сигналов ЧСС за счет расширения поля восприятия ядра свертки каждого уровня при сохранении относительно небольшого размера параметра. Кроме того, был исследован метод кросс-модального объединения признаков (CMFF), который использовал механизмы многоголового внимания для изучения взаимосвязей между различными модальностями, получения более информативных представлений признаков и повышения точности диагностики. Механизм многоголового внимания (англ. multi-head attention mechanism) – это механизм внимания с несколькими головами, который позволяет модели одновременно принимать во внимание информацию из разных подпространств векторных представлений. Авторы указали, что данный метод превосходит традиционные методы, которые применялись ранее, со средней точностью 96,8%, специфичностью 97,5%, чувствительностью 96% [73].
Cao Z. et al. (2023) описывают мультимодальную систему для антенатального мониторинга плода, способную автоматически извлекать признаки КТГ и классифицировать их [74]. В ее основе лежит сверточная нейронная сеть (CNN). Признаки КТГ были извлечены из предварительно обработанных сигналов КТГ с помощью CNN. Также был применен LightGBM – классификатор повышения градиента в машинном обучении, который использовал древовидные алгоритмы обучения. MMDLA способствует реализации интеллектуального мониторинга состояния плода в антенатальном периоде. Данный метод достиг точности 90,77% [74].
Black S. et al. (2024) в своем исследовании предлагают нововведение в практическом применении – системы с ИИ для дистанционного мониторирования состояния плода (NeuroFetalNet) [75]. В основе работы данной модели опять же метод глубокого машинного обучения и классификация данных с помощью наивного байесовского классификатора, дерева принятия решений, многослойного персептрона и радиальной базисной функции. Авторы указывают, что внедрение в систему здравоохранения таких современных систем могло бы улучшить охрану здоровья матери и ребенка [75].
Заключение. Таким образом, исследования, посвященные искусственному интеллекту в области фетального мониторинга или кардиотокографии, показывают улучшение качества диагностики гипоксических состояний плода в антенатальном периоде и родах. Однако они имеют в настоящее время уровень разработок и анализа данных.
Модели машинного обучения повышают эффективность прогнозирования состояния плода и позволяют снизить перинатальную смертность [76]. Следует подчеркнуть более высокую точность диагностики систем КТГ на основе ИИ по сравнению с традиционными методами, 96,8-99,2% и 80,0-84,4% соответственно [19, 28, 69, 73].
Современная диагностическая технология на основе искусственного интеллекта в области КТГ может являться виртуальным цифровым помощником для акушеров в принятии медицинских решений [77]. Все это диктует необходимость дальнейших исследований в области КТГ и ИИ. Полученные данные могут быть использованы для улучшения перинатальных исходов.
Информация о финансировании
Финансирование данной работы не проводилось.





















Список литературы