Влияние реабилитационных мероприятий на гериатрический профиль пациентов с глаукомой
Aннотация
Актуальность: Высокая распространенность глаукомы сопровождается неуклонным снижением функциональной активности из-за существенного зрительного дефицита и ухудшением гериатрического статуса пациентов, который в настоящее время изучен недостаточно. При наличии зрительного дефицита специалистами осуществляется в основном его коррекция хирургическими методами, но реабилитационные мероприятия, направленные на улучшение гериатрического профиля среди лиц в старческом и пожилом возрасте, осуществляется редко. Цель исследования: Анализ влияния реабилитационных мероприятий на гериатрический профиль пациентов с глаукомой. Материалы и методы: В исследовании приняли участие 165 пациентов пожилого и старческого возраста с глаукомой (основная группа), среди которых после лазерной трабекулопластики осуществлялись реабилитационные мероприятия с гериатрической направленностью: физические упражнения по улучшению координации глаз и движений рук; выполнение когнитивной гимнастики; силовых упражнений; повышение социальных коммуникаций; увеличение в рационе питания растительного белка, применение нутрицевтика «Фрезубин». В контрольной группе (108 пациентов) проводилось только хирургическое лечение глаукомы. Через год после реабилитации выполнена комплексная гериатрическая оценка с выявлением ведущих клинических дефицитных синдромов. Результаты: Среди пациентов старческого и пожилого возраста с глаукомой основной группы на момент завершения наблюдений статистически значимо снизилась распространенность синдрома риска падений с 49,1±4,0 до 22,8±1,9 случаев на 100 пациентов (p˂0,01) с достоверным различием в сравнении с контрольной группой. Среди пациентов основной группы также уменьшилась распространенность синдрома падений и когнитивных нарушений. В контрольной группе пациентов с глаукомой снизилась только распространенность синдрома падений. При снижении зрительного дефицита пациентов пожилого и старческого возраста через год реабилитации с достижением остроты зрения без коррекции более 0,3 в основной группе отмечено улучшение гериатрического статуса по четырем дефицитарным синдромам при этом наиболее существенно уменьшилась частота синдрома нарушения общей двигательной активности (p˂0,01). В контрольной группе уменьшилась частота синдрома гипомобильности. Величина максимально корригированной остроты зрения повысилась в основной группе статистически значимо с 0,28±0,03 до 0,52±0,04 (p˂0,01), а в контрольной группе с 0,24±0,02 до 0,39±0,03 (p˂0,01). Заключение: Дополнение оперативного лечения пациентов с глаукомой комплексом реабилитационных мероприятий гериатрической направленности существенно улучшает гериатрический профиль.
Введение. Глаукома в настоящее время выступает ведущей причиной потери зрения и такая тенденция сохранится в последующие годы [1]. Экспертами сообщается, что в 2020 году общее число больных с первичной глаукомой составило около 76 миллионов человек в мире, а к 2040 году число таких пациентов прогнозируется до 112 миллионов человек [1]. По другим оценкам, вследствие увеличения в мире количества пожилого и старческого населения, считается, что глаукома будет являться одной из причин наступления слепоты в мире [2]. На втором месте в структуре причин развития слепоты находятся рефракционные нарушения, составляющие 13,1%. Однако, по прогнозным оценкам количество ослепших в мире из–за развития глаукомы может достигнуть 5,9 и 5,3 миллионов соответственно [3, 4]. Общее же количество заболевших разными формами первичной глаукомы составит в мире 79,6 миллионов человек [5].
Среди гериатрических синдромов, которые изучаются у пациентов с первичной глаукомой, в публикациях последних лет представлены преимущественно сведения о распространенности когнитивных нарушений и депрессии. Изучением когнитивного дефицита и депрессивного статуса у пациентов с первичной глаукомой занимаются в основном иностранные ученые и лишь в нескольких публикациях опубликованы результаты российских специалистов. В частности, в исследовании Малишевской Т.Н. [6] установлены более высокие уровни тревожности и депрессии, увеличение распространённости синдрома нарушения сна, тревожно-депрессивного синдрома среди пациентов с первичной глаукомой по сравнению с возрастным контролем с отсутствием названного заболевания. Показаны особенности синдрома нарушений общей двигательной активности у пациентов с глаукомой [7]. Сообщается о позитивном влиянии рискориентированного лечения на когнитивный статус пожилых пациентов с глаукомой и катарактой [8], но данное исследование, как рассмотренные ниже, не дают целостного представления о гериатрическом континууме пациентов с глаукомой. Однако о связи когнитивных нарушений и плохого зрения вследствие глаукомы в настоящее время имеются скудные и противоречивые данные [5]. Известно о шестилетнем лонгитудинальном изучении когнитивных нарушений в Сингапуре в рамках Сингапурского эпидемиологического исследования глазных болезней, которое состояло из трех основных азиатских этнических групп, набранных в рамках трех исследований: Сингапурского Малайского исследования глаз (2004–2006 гг.), Сингапурского Индийского исследования глаз (2007–2009 гг.) и Сингапурского Китайского исследования глаз (2009–2011 гг.) Пациенты стратифицированы по возрасту и в исследование включены лица в возрасте от 40 до 80 лет в общей сложности 10 033 малайских, индийских и китайских взрослых, завершивших исследование. Когнитивная оценка проведена по сокращенному тесту ментальных функций из 10 вопросов и только у пациентов старше 60 лет (n=4407 человек). Повторно были обследованы 2478 человек, так как другие пациенты выбыли из исследования по разным причинам [9, 10].
Цель исследования. Анализ влияния реабилитационных мероприятий на гериатрический профиль пациентов с глаукомой.
Материалы и методы исследования. В исследовании приняли участие 165 пациентов пожилого и старческого возраста с глаукомой, входящих в основную группу (Табл. 1).
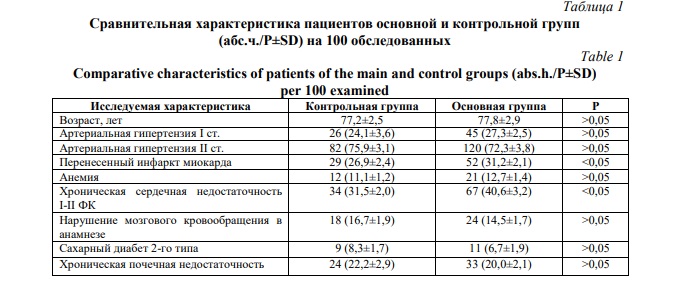
Контрольную группу составили 108 пациентов аналогичного возраста, которым выполнялась только лазерная трабекулопластика. В основной группе после выполнения лазерной трабекулопластики проводились на амбулаторном этапе реабилитационные мероприятия. Предложенные нами реабилитационные мероприятия были направлены на выявленные в настоящем исследовании доминирующие и представленные дефицитарные синдромы у пациентов с глаукомой – синдром риска падений, падений, психологических проблем и когнитивных нарушений. Они включали в себя физические упражнения по улучшению координации глаз и движений рук по 30-40 минут в неделю; выполнение когнитивной гимнастики по общепринятой методике; силовых упражнений в положении сидя с гантелями весом до 0,5 кг; повышение социальной активности путем общения с родственниками по телефону, волонтерами, специалистами социальной службы; повышение в рационе питания растительного белка до 10-20% суточной потребности, злаков, бобовых и орехов; выполнение дыхательной гимнастики, применение нутрицевтика «Фрезубин» по 300 мл ежедневно в течение 2 месяцев.
Анализ пациентов основной и контрольной групп по наличию сопутствующей соматической патологии не выявил статистически значимых различий, за исключением некоторых заболеваний. Сказанное относится к частоте перенесенного инфаркта миокарда, который чаще встречался среди пациентов основной группы и частоте хронической сердечной недостаточности I-II ФК с аналогичной закономерностью, как и для перенесенного инфаркта миокарда.
При оценке результативности реабилитационных мероприятий через год после их реализации среди пациентов обеих клинических групп проводилась комплексная гериатрическая оценка [11]. Зрительный дефицит и состояние функции зрения определялись на основе комплексного офтальмологического обследования. Острота зрения без коррекции и с коррекцией изучались по таблицам Сивцева-Головина. Проводилось также определение внутриглазного давления, оптическая когерентная томография с функцией ангиографии.
Исследование осуществлялось с соблюдением всех этических норм и принципов, принятых в клинической практике.
При статистической обработке производился расчет интенсивных показателей, стандартных отклонений. Сравнение результатов проводилось по критерию X2. Статистически значимыми считались различия при p˂0,05.
Результаты и обсуждение. Анализ частоты основных клинических гериатрических синдромов у пациентов старческого возраста с глаукомой в зависимости от остроты зрения без коррекции после выполненного курса реабилитации выявил различные результаты в сравниваемых группах (Табл. 2).
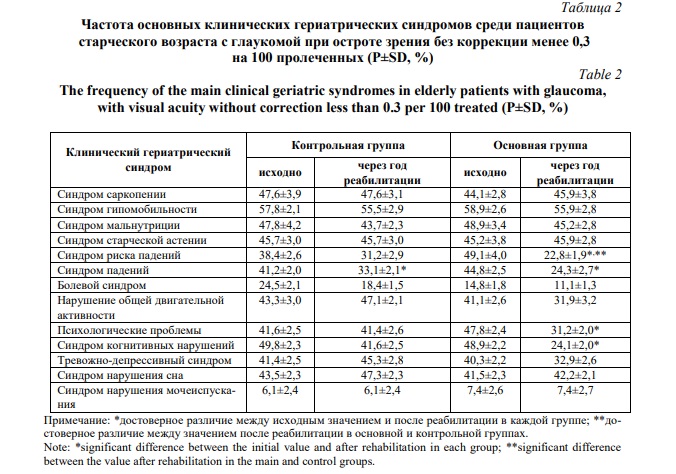
Так, в контрольной группе при использовании стандартной схемы реабилитации к моменту завершения наблюдения среди изученных клинических гериатрических синдромов у пациентов с остротой зрения без коррекции менее 0,3 статистически значимо уменьшилась только распространенность синдрома падений (Р<0,001). Распространенность синдрома саркопении, синдрома старческой астении осталась без изменений. Частота болевого синдрома, синдрома нарушения общей двигательной активности, психологических проблем, синдрома когнитивных нарушений, тревожно-депрессивного синдрома и синдрома нарушения сна не имели существенных различий между исходным показателем и после завершения лечения (Р>0,05).
На фоне предложенной нами гериатрической реабилитации глаукомы у пациентов старческого возраста с остротой зрения без коррекции менее 0,3 к моменту окончания динамического наблюдения достоверно уменьшилась распространенность 4-х клинических гериатрических синдромов. При этом наиболее существенно после лечения понизилась частота синдрома риска падений, которая была достоверной не только по отношению к величине при обращении за медицинской помощью, но и по отношению к показателю после завершения лечения в контрольной группе (Р<0,01). Среди пациентов 75-89 лет с глаукомой основной группы статистически достоверно к окончанию лечения снизилась также распространенность синдрома падений, психологических проблем и синдрома когнитивных нарушений. Однако вышеназванные клинические гериатрические синдромы не имели достоверных различий в сравнении с таковыми контрольной группы, диагностированными на момент завершения лечебных мероприятий. Вместе с тем, на наш взгляд, снижение в основной группе частоты синдрома риска падений обусловлено не только уменьшением степени зрительного дефицита, но и улучшением синдромов когнитивно-психологического статуса.
Таким образом, снижение зрительного дефицита по остроте зрения без коррекции менее 0,3 у пациентов старческого возраста с глаукомой после реализации предложенной нами гериатрической реабилитации значительнее улучшилась их функциональность за счет достоверного уменьшения частоты синдрома риска падений, синдрома падений, психологических проблем и синдрома когнитивных нарушений, тогда как после стандартного протокола снизилась частота только синдрома падений.
При снижении зрительного дефицита у пациентов старческого возраста с глаукомой через 1 год после выполненной реабилитации с достижением остроты зрения без коррекции более 0,3 результаты исследования по частоте основных клинических гериатрических синдромов незначительно отличаются от рассмотренного ранее зрительного дефицита менее 0,3. При достижении остроты зрения без коррекции более 0,3 среди больных, которым проводилось стандартное лечение, гериатрический статус достоверно улучшился по 2-м клиническим гериатрическим синдромам – синдрому гипомобильности и тревожно-депрессивному синдрому. Недостоверное уменьшение среди рассматриваемых клинических гериатрических синдромов в контроле характерно для синдрома падений, болевого синдрома, нарушения общей двигательной активности, психологических проблем, синдрома нарушения сна. Несмотря на проведенное лечение у больных 75-89 лет с глаукомой не изменилась распространенность синдрома саркопении, синдрома мальнутриция и старческой астении (P>0,05).
При оценке зрительного дефицита по максимально корригированной остроте зрения у больных старческого возраста после завершения реабилитационных мероприятий выявлено статистически достоверное повышение данного параметра в обеих группах. Однако максимально корригированная острота зрения достоверно выше оказалась на момент завершения лечения среди пациентов основной группы (Р<0,05). Следовательно, предложенная тактика по такому важному показателю зрительного дефицита как максимально корригированная острота зрения у пациентов старческого возраста с глаукомой является более успешной. Такой результат достигнут у пациентов основной группы с глаукомой благодаря комплексной гериатрической тактике, предусматривающей коррекцию не только гериатрического статуса, но и зрительного дефицита (Рис. 1).
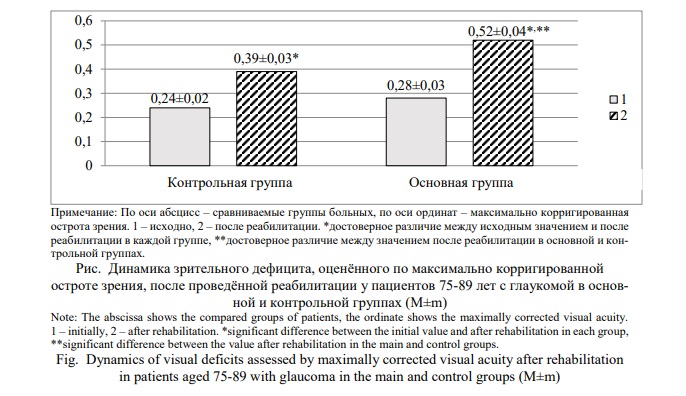
Итак, предложенные и реализованные реабилитационные мероприятия в основной группе пациентов привело к улучшению гериатрического профиля пациентов с глаукомой по снижению частоты синдрома риска падений, падений, психологических проблем и когнитивных нарушений, не оказав значительного влияния на другие дефицитарные состояния (синдром саркопении, мальнутриции, старческой астении, тревожно-депрессивный синдром, синдром нарушения общей двигательной активности и другие).
Глаукома является серьезной проблемой общественного здравоохранения и ведущей причиной необратимых нарушений зрения во всем мире. Первичная открытоугольная глаукома (ПОУГ) является наиболее распространенным типом глаукомы, на долю которого приходится три четверти (74%) всех случаев глаукомы. Недавние исследования показали, что число случаев ПОУГ в 2019 году в 49 миллионов, а к 2025 году оно увеличится до 3 миллионов из-за старения населения [1]. Однако неопределенность в отношении числа людей с ПОУГ все еще сохраняется, поскольку эти глобальные оценки связаны с двукратной разницей в странах содружества независимых государств (т.е. оценки варьируют от 31 миллионов до 61 миллионов случаев заболевания в 2019 году и увеличится до 57-73 миллионов к 2025 году [2]. Такая неопределенность затрудняет точное планирование соответствующих реабилитационных медицинских услуг. Причины этой неопределенности многочисленны и связаны с географическими различиями в лежащей в основе распространенности ПОУГ, а также связаны с различиями в методах изучения глаукомы.
Глаукома в настоящее время изучена недостаточно не только в эпидемиологическом, но и гериатрическом аспектах. Гериатрический статус пациентов с глаукомой, как правило, редко анализируется в отличие от общесоматической патологии. Вместе с тем в оценке дефицитарного статуса пациентов с глаукомой превалируют когнитивные нарушения.
Показано, что лица, получившие инвалидность по причине глаукомы, в большей степени были подвержены развитию когнитивных нарушений, что подчеркивает еще раз важность сохранения хорошего зрения среди пожилых с глаукомой. Установлено также, что среди пациентов с исходным плохим зрением и значительными когнитивными нарушениями, ведущими причинами ухудшения зрения являлись глаукома и нарушение рефракции [12].
Средний балл когнитивных нарушений у больных с первичной закрытоугольной глаукомой составил 26,3±3,7 и распространенность ее при этой форме глаукомы более низкая, чем при других офтальмопатологиях [13]. Такие результаты о частоте и проявлении когнитивных нарушений у пациентов пожилого возраста получены при обследовании 3127 человек. Однако распространенность первичной глаукомы, а также других сенсорных дефицитов, таких как возрастная макулярная дегенерация, диабетическая ретинопатия, окклюзия вен сетчатки, катаракта любого типа или псевдоэксфолиативный синдром достоверно не коррелировали с субфовеальной толщиной хориоидеи. Несмотря на то, что причинно-следственная связь неясна, ассоциация более низкой когнитивной функции с недокорректированной остротой зрения предполагает необходимость более раннего и более регулярного контроля зрения у пожилых людей.
В пожилом возрасте при наличии ПОУГ повышается частота когнитивных нарушений по сравнению с лицами среднего возраста, а именно распространенность легких когнитивных нарушений до 39,0% против 13,5% – в среднем возрасте и 62,2% - в старческом возрасте. Зависимости частоты когнитивного дефицита от стадии первичной глаукомы не установлено. Изучение полей зрения у пациентов с глаукомой имеет важное значение для выявления взаимоотношений с когнитивными нарушениями [12]. Исследование ассоциаций между полем зрения, структурно–функциональными отношениями и когнитивными изменениями проведено у 51 больного с глаукомой в возрасте старше 75 лет. Используя перекрестную валидацию, среднее стандартное отклонение, оптическую когерентную томографию и взаимосвязи между баллом MMSE, а также возрастом, ложноположительными и ложноотрицательными результатами построены прогностические линейные модели. Наблюдалась высокая распространенность умеренных когнитивных нарушений у пациентов с глаукомой.
Для оценки когнитивных нарушений у больных глаукомой предложен тест быстрой оценки когнитивных функций, а также для сравнения их у пациентов с глаукомой и катарактой [13]. Оценка когнитивных функций выполнена у 30 пациентов с глаукомой и 30 пациентов с катарактой посредством метода Фрейда с использованием 7 бальной шкалы и методом Ракуса с использованием 4–бальной шкалы. Величина когнитивных способностей по краткому тесту у пациентов с катарактой и глаукомой составила 3,5 балла и 6,5 балла соответственно. Указывается, что полученные результаты можно использовать при оценке реабилитационных мероприятий.
Показано влияние когнитивных нарушений у пациентов с открытоугольной глаукомой на функциональную работоспособность 20 водителей в сравнении с 13 водителями без когнитивных нарушений [14]. Состояние поля зрения оценивали при различной степени когнитивного нарушения. Определялось статическое состояние поля зрения, динамическое состояние поля зрения и динамическое состояние поля зрения с активным вождением и использованием интерактивного настольного симулятора вождения. Развитие когнитивных нарушений отрицательно повлияло на точность и время выполнения с симулятором вождения у водителей с открытоугольной глаукомой. Все тесты у пациентов с глаукомой выполнялись хуже, чем в возрастном контроле (без глаукомы). В частности, при изменении статического состояния в динамическое точность функций у пациентов с глаукомой в среднем составила 3 балла против 2 баллов в контрольной группе (р=0,05).
В единичных публикациях зарубежных исследователей сообщается о распространенности депрессивных изменений среди больных с первичной глаукомой [14, 15, 16]. Показано, что распространенность депрессии или депрессивных симптомов при глаукоме выявлена в 25 % случаев [17, 18]. В целом же, по различным оценкам, у больных с сенсорными дефицитами депрессия встречается от 5,4% до 57,0%. У пациентов с катарактой депрессивные нарушения отмечены приблизительно у такой же части, как и при первичной глаукоме – в 23% случаев [19, 20]. Согласно другим публикациям, распространенность депрессии в Китае у пациентов с глаукомой несколько ниже и составляет 16,40% [2]. Считается, что развитие депрессивных нарушений у пациентов с офтальмологическими заболеваниями связано с активацией иммунного воспаления [2]. Депрессия при катаракте, согласно единичным опубликованным работам, невысока и встречается у 3,33% против 1,84% без катаракты у лиц пожилого возраста [2].
Заключение. Завершение реабилитационных мероприятий среди пациентов пожилого и старческого возраста с глаукомой обеспечило существенное и статистически значимое улучшение гериатрического профиля пациентов основной группы, чем в контрольной при использовании только лазерной трабекулопластики для коррекции зрительного дефицита. Среди пациентов основной группы на момент завершения наблюдений снизилась распространенность синдрома падений и когнитивных нарушений. Максимально корригированная острота зрения на фоне реализации реабилитационных мероприятий гериатрической направленности повысилась с 0,28±0,03 до 0,52±0,04, что существенно выше, чем в контрольной группе и свидетельствует о её результативности. Улучшение гериатрического профиля пациентов обусловлено не только снижением зрительного дефицита, но и улучшением их когнитивно-психологического статуса.




















Список литературы
advanced glaucoma. Medicine. 2020;99(7):e19149. DOI: https://doi.org/10.1097/MD.0000000000019149
phagocytosis and pathological changes in the development and degeneration of the visual system. Frontiers in Immunology. 2020;11:566892. DOI: https://doi.org/10.3389/fimmu.2020.566892