Молекулярный профиль людей разного возраста в «норме» и при дилатационной кардиомиопатии
Aннотация
Актуальность: Дилатационная кардиомиопатия (ДКМП) является сердечно-сосудистой патологией, перспективной для рассмотрения в качестве клинической модели преждевременного старения организма. Клиническое значение для оценки преждевременного старения организма на модели ДКМП, согласно данным литературы, могут иметь сиртуины-1, 2, 3, 6; мелатонин и рецепторы к нему (МТ-1 и МТ-2); маркеры клеточного старения (белки р16, р21) и апоптоза (ВАХ). Сравнительного изучения экспрессии указанных молекул у людей разного возраста в зависимости от наличия ДКМП ранее не проводилось. Цель исследования:Выявить и сравнить молекулярные профили у людей разного возраста с отсутствием сердечно-сосудистых заболеваний и наличием ДКМП по уровню экспрессии изучаемых сигнальных молекул в буккальном эпителии и аутопсийном материале миокарда. Материалы и методы:Проведено исследование буккального эпителия (174 человека) и аутопсийного материала миокарда (175 человек) у пациентов 45-89 лет на предмет экспрессии сигнальных молекул: сиртуины 1, 2, 3, 6, белки р16, р21 и ВАХ. Использовались методы иммуноцитохимического и иммуногистохимического исследования. Выделены группы среднего, пожилого и старческого возраста с ДКМП и без сердечно-сосудистой патологии в анамнезе. Результаты:Выявлены характерные изменения молекулярного профиля (уровень исследуемых сигнальных молекул) в буккальном эпителии, ассоциированные с возрастом и наличием ДКМП: у пациентов среднего возраста – снижение уровня экспрессии сиртуинов 3 и 6 в 2,2-2,3 раза, мелатонина в 1,8 раза и его рецепторов в 1,4-2,5 раза; у пациентов пожилого возраста – снижение экспрессии сиртуинов 1 и 3 в 2,5 раза; сиртуина 2 в 2,3 раза; мелатонина и рецепторов к нему 1,4-1,8 раза; у пациентов старческого возраста – снижение экспрессии сиртуинов 3 и 6 в 3,0-4,7 раза; сиртуинов 1 и 2 в 6,7-7,3 раза; мелатонина в 2,8 раза; МТ-1 – в 4,1 раза и МТ-2 – в 23,7 раза. Дополнительную диагностическую информативность в диагностике ДКМП у лиц различных возрастных групп имеет повышение экспрессии белков р16 и ВАХ в 0,6-0,8 раза в буккальном эпителии. Наблюдается взаимосвязь изменений экспрессии данных молекул в буккальном эпителии и аутопсийном материале миокарда. Заключение:Молекулярные профили у людей различных возрастных групп, определяемые по уровню экспрессии изученных сигнальных молекул достоверно различаются в зависимости от наличия ДКМП. Характерно, что направленность изменений в буккальном эпителии носит сходный характер с соответствующим молекулярным профилем в аутопсийном материале миокарда
Ключевые слова: дилатационная кардиомиопатия, сиртуины, мелатонин и рецепторы к нему, ВАХ, молекулярный профиль, возрастные изменения, преждевременное старение
Введение. Изменения, затрагивающие сердечно-сосудистую систему и наступающие с возрастом, приводят к ухудшению функционирования миокарда (очаговая атрофия мышечных волокон, эндомиокардиальный фиброз, ухудшение распространения импульсов по проводящей системе, дисфункция активности пейсмейкеров и др.) и сосудистого русла (повышение жесткости и общего периферического сопротивления сосудов, атеросклеротические изменения, снижение количества функционирующих капилляров на единицу площади) [1]. Указанные процессы ассоциированы с развитием ишемической болезни сердца, клапанной дисфункции, артериальной гипертензии, кардиомиопатий, хронической сердечной недостаточности. Развитие данных патологических состояний в свою очередь ускоряет течение возрастных изменений, и обусловливает в конечном счете развитие старения по патологическому типу.
Дилатационная кардиомиопатия (ДКМП) является, по нашему мнению, перспективной для рассмотрения в качестве клинической модели преждевременного старения организма с современных позиций. Для этого заболевания характерно развитие процесса старения по патологическому типу. В основе ДКМП лежит дилатация камер сердца, преимущественно левого желудочка, что приводит к появлению систолической дисфункции [2]. Порядка 30% всех случаев ДКМП обусловлено мутациями на генном уровне, приводящими к нарушению образования белков, формирующих мышечный цитоскелет кардиомиоцитов (в первую очередь, дистрофины, ламинин). При их дефиците развивается дистрофия миокарда, снижается передача возбуждения, происходит медленное «ослабление» насосной функции сердца. Если несколько десятилетий назад ДКМП встречалась преимущественно у людей молодого возраста, то благодаря развитию социально-медицинских технологий сегодня ДКМП составляет значительную долю у лиц старше 60 лет [3].
Уточнение клеточно-молекулярных механизмов патогенеза заболеваний, вызывающих преждевременное старение, позволяет разрабатывать новые подходы к диагностике и лечению пациентов старших возрастных групп. Одним из направлений для решения этой задачи является изучение молекулярного профиля при старении в норме и при ДКМП, а также выявление диагностических маркеров преждевременного старения организма. Среди сигнальных молекул, которые по данным литературы могут иметь диагностическую ценность и клинически значимое прогностическое значение для оценки преждевременного старения организма на модели ДКМП, выделяют сиртуины (SIRT)-1, 2, 3, 6; мелатонин (МТ) и рецепторы к нему (МТ-1, МТ-2); маркеры клеточного старения (белки р16, р21) и апоптоза (Bcl-2-ассоциированный X-белок, BАX) [4-9]. Сравнительного изучения экспрессии указанных молекул у людей разного возраста, имеющих ДКМП и не имеющих верифицированных сердечно-сосудистых заболеваний, до сих пор не проводилось.
Цель исследования. Выявление и сравнение молекулярных профилей у людей разного возраста с отсутствием сердечно-сосудистых заболеваний («норма») и наличием ДКМП по уровню экспрессии изучаемых сигнальных молекул в буккальном эпителии и аутопсийном материале миокарда.
Материалы и методы исследования. У пациентов 45-89 лет было проведено исследование буккального эпителия (БЭ) (174 человека) и аутопсийного материала миокарда (АММ) (175 человек). Обследуемые были разделены на две группы: с наличием ДКМП, верифицированной согласно современным рекомендациям, и с отсутствием сердечно-сосудистой патологии. Материалы для исследования были получены в СПб ГБУЗ «Городская многопрофильная больница № 2» (г. Санкт-Петербург). В полученных материалах оценивалась площадь экспрессии сигнальных молекул SIRT1, SIRT2, SIRT3, SIRT6; мелатонина и рецепторов к нему МТ-1, МТ-2; белков р16, р21 и ВАХ при помощи иммуноцитохимического, иммуногистохимического методов и компьютерного анализа микроскопических изображений.
Взятие материала слизистой оболочки щеки (буккальный эпителий) проводилось после полоскания полости рта 0,9% раствором хлорида натрия, через 4 и более часа после приема пищи. Для забора БЭ использовались одноразовые стерильные зонды с синтетическим ворсом, использовались стерильные одноразовые пробирки «эппендорф» с транспортной средой. Цитологические мазки были подготовлены при помощи метода (автоматизированная система Novoprep, Франция). В таблице 1 представлена характеристика пациентов, у которых было проведено исследование БЭ.

Аутопсийный материал был получен от пациентов с верифицированной ДКМП, в качестве группы сравнения использовался АММ, забранный от людей с отсутствием кардиоваскулярной патологии в анамнезе («нормальный» АММ). В таблице 2 представлена характеристика групп пациентов, от которых был получен аутопсийный материал.

Для иммуноцитохимического исследования БЭ и иммуногистохимического исследования АММ использовали первичные моноклональные антитела, представленные в таблице 3.

В качестве вторичных антител для проведения иммунофлуоресцентной реакции использовали антитела, конъюгированные с флуорохромом Alexa Fluor 647 (Abcam, Англия, 1:1000). Материал инкубировали 30 мин при комнатной температуре в темноте. Ядра клеток докрашивали Hoechst 33258 (Sigma, США). Визуализацию результатов иммунофлуоресцентого окрашивания осуществляли с помощью конфокального микроскопа Zeiss LSM 980. Для оценки результатов иммунофлуоресцентного окрашивания было проведено морфометрическое исследование с помощью системы компьютерного анализа микроскопических изображений Image J. В каждом случае анализировали 5 полей зрения при х200. Проводилось измерение площади экспрессии. Площадь экспрессии рассчитывалась как отношение площади, занимаемой иммунопозитивными клетками, к общей площади клеток в поле зрения и выражалась в процентах для маркеров с цитоплазматическим окрашиванием и как отношение площади, занимаемой иммунопозитивными ядрами к общей площади ядер в поле зрения для маркеров с ядерной экспрессией.
Для статистической обработки полученных результатов использовалось программное обеспечение Statistica 7.0. Критический уровень достоверности нулевой гипотезы по критерию Стьюдента (об отсутствии различий) принимали равным 0,01.
Результаты и их обсуждение. В зависимости от уровня исследуемых сигнальных молекул были выявлены характерные изменения молекулярного профиля, ассоциированные с возрастом и наличием ДКМП.
Молекулярный профиль людей среднего возраста в «норме» и при ДКМП. У пациентов среднего возраста с дилатационной кардиомиопатией в БЭ было установлено достоверное уменьшение площади экспрессии SIRT3 в 2,2-2,3 раза (р=0,004); SIRT1, SIRT2 в 1,7-2 раза (р=0,000 и р=0,002 соответственно). Отмечена тенденция к снижению экспрессии SIRT6 в 2,2-2,3 раза (р=0,021); мелатонина в 1,8 раза (р=0,052). Экспрессия рецепторов к мелатонину МТ-2 достоверно уменьшалась в 1,4-2,5 раза (р=0,002) при сравнении с группой пациентов соответствующего возраста, не имевших ДКМП. В АММ у пациентов с ДКМП отмечено достоверное уменьшение площади экспрессии SIRT3, SIRT6 в 1,3-1,6 раза (р=0,000 в обоих случаях); SIRT1, SIRT2 в 2-2,2 раза (р=0,000 и р=0,001 соответственно); мелатонина в 1,7 раза (р=0,000). Площадь экспрессии рецепторов к мелатонину МТ-2 уменьшалась в 1,2-1,3 раза (р=0,002), увеличивалась площадь экспрессии белка р16 в 1,2 раза (р=0,010) при сравнении с соответствующим возрастом в норме.
Была также отмечена тенденция к снижению экспрессии МТ-1 в 1,4-2,5 раза, повышению экспрессии маркеров старения р16, р21 и ВАХ в 0,6 раза в буккальном эпителии, увеличению площади экспрессии р21 в 1,2 раза и маркера апоптоза ВАХ в 1,7 раза в аутопсийном материале миокарда, однако различия не были статистически значимы.
Данные, иллюстрирующие площадь экспрессии исследуемых сигнальных молекул, представлены не рисунке 1.

Молекулярный профиль людей пожилого возраста в «норме» и при ДКМП. Выявлено, что уровень экспрессии сигнальных молекул SIRT1 (р=0,000), SIRT2 (р=0,003), SIRT3 (р=0,007), SIRT6 (р=0,004) в БЭ у людей пожилого возраста без сердечно-сосудистой патологии достоверно уменьшился в 1,7-2,2 раза. У группы лиц пожилого возраста выявлено достоверное уменьшение площади экспрессии в аутопсийном материале миокарда сигнальных молекул: SIRT1, SIRT2, SIRT6 в 1,3-1,4 раза (р=0,003; р=0,000 и р=0,001 соответственно); SIRT3, мелатонина и рецепторов к нему МТ-1 и МТ-2 – в 1,5-1,6 раза (р=0,000 во всех случаях) и увеличение площади экспрессии маркеров старения р16, р21 и маркера апоптоза ВАХ в 1,3-1,5 раза при сравнении с материалом группы лиц среднего возраста (р=0,000; р=0,002 и р=0,000 соответственно).
При дилатационной кардиомиопатии у пациентов пожилого возраста в аутопсийном материале миокарда установлено: достоверное уменьшение площади экспрессии SIRT6 в 1,6 раза; SIRT1, SIRT3 в 2,5 раза; SIRT2 в 2,3 раза; мелатонина и рецепторов к нему МТ-2 в 1,4-1,8 раза и увеличение площади экспрессии маркера апоптоза ВАХ в 1,4 раза (р=0,000 во всех случаях). Уровень р21 остался практически без изменений при сравнении с соответствующей возрастной группой в норме. У пациентов пожилого возраста при дилатационной кардиомиопатии в БЭ установлено уменьшение площади экспрессии SIRT6 в 2 раза (р=0,011); достоверное снижение экспрессии SIRT1, SIRT3 в 2 раза; SIRT2 в 2,7 раза (р=0,001 во всех случаях). Отмечено снижение мелатонина и рецепторов к нему МТ-2 в 1,9-3,4 раза (р=0,017 и р=0,000 соответственно) и увеличение площади экспрессии маркера старения р21 в 0,7 раза (р=0,034).
Дополнительно отмечена тенденция к уменьшению экспрессии мелатонина и рецепторов к нему МТ-1 и МТ-2 – в 1,3-1,8 раза и увеличению площади экспрессии маркеров р16, р21 и ВАХ в 0,63-0,8 раза при сравнении с материалом группы лиц среднего возраста в буккальном эпителии и увеличению площади экспрессии р16 в 1,1 раза и ВАХ в 1,4 раза в АММ.
Полученные данные представлены на рисунке 2.
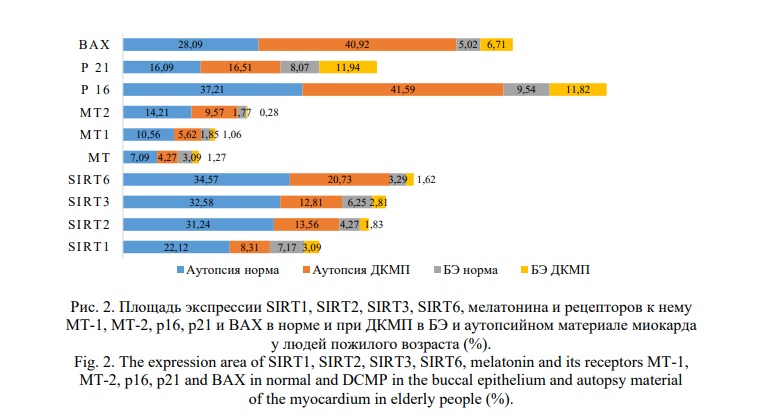
Молекулярный профиль людей старческого возраста в «норме» и при ДКМП. Отмечено достоверное уменьшение площади экспрессии SIRT1, SIRT2, SIRT3, SIRT6 в БЭ в группе лиц старческого возраста в 2,6-4,1 раза (р=0,000 во всех случаях); мелатонина и рецепторов к нему МТ-1, МТ-2 – в 2,5-6 раз (р=0,007; р=0,000 и р=0,000 соответственно). Установлено достоверное уменьшение площади экспрессии в АММ в группе лиц старческого возраста: SIRT2, SIRT6 в 1,7-1,8 раза; SIRT1, SIRT3 – в 2,3-3 раза, мелатонина и рецепторов к нему МТ-1, МТ-2 – в 3,3-4 раза (р=0,000 во всех случаях) и достоверное увеличение площади экспрессии маркеров старения р16, р21 и маркера апоптоза ВАХ в 1,4-1,8 раза (р=0,000; р=0,006 и р=0,000 соответственно), по сравнению с материалом группы лиц среднего возраста.
В старческом возрасте у пациентов с ДКМП в аутопсийном материале миокарда отмечено достоверное уменьшение площади экспрессии: SIRT1, SIRT2, SIRT6 в 2-2,3 раза; SIRT3 в 5,6 раза; мелатонина в 3,2 раза; МТ-1 – в 2 раза и МТ-2 – в 4 раза, при увеличении площади экспрессии маркеров р16, ВАХ в 1,3-1,4 раза (р=0,000 во всех случаях). Уровень р21 остался практически без изменений при сравнении с соответствующей возрастной группой в норме. В БЭ у пациентов данной возрастной группы выявлено достоверное уменьшение площади экспрессии: SIRT3, SIRT6 в 3-4,7 раза; SIRT1, SIRT2 в 6,7-7,3 раза (р=0,000 во всех случаях). Отмечена тенденция к снижению экспрессии мелатонина в 2,8 раза (р=0,013) и МТ-2 – в 23,7 раза (р=0,000), Уровень экспрессии р16, р21 и ВАХ в буккальном эпителии был сопоставим с таковым у лиц старческого возраста, не имевших ДКМП. Данные представлены на рисунке 3.

Согласно литературным данным, уровень сиртуинов снижается при гипертрофии миокарда, хронической сердечной недостаточности [10, 11]. Кроме этого, отмечается снижение экспрессии мелатонина и рецепторов к нему МТ-1 и МТ-2, участвующих в регуляции ответа при повреждении миокарда, воспалении, окислительном стрессе, метаболических нарушениях и старении [12, 13]. В ряде исследований отмечено, что экспрессия маркеров клеточного старения р16, р21 и апоптоза BAХ при старении и сердечно-сосудистых заболеваниях увеличивается [14, 15].
Уровень важнейших агентов, участвующих в регуляции функционирования миокарда - сиртуинов-1, 2, 3 и 6, а также мелатонина и его рецепторов (МТ-1, МТ-2) снижается с возрастом как в буккальном эпителии, так и в кардиомиоцитах, наблюдается увеличение маркеров клеточного старения и апоптоза – белков р16, р21 и ВАХ. При отсутствии сердечно-сосудистой патологии в буккальном эпителии, клетках миокарда и культурах кардиомиоцитов этот процесс выражен умеренно, тогда как при ускоренном старении, ассоциированным с дилатационной кардиомиопатией, эта тенденция значительно нарастает. Полученные данные свидетельствуют о том, что при сердечно-сосудистой патологии повышается активность воспаления, окислительного стресса и клеточной гибели и согласуются с результатами проведенных ранее исследований в отношении экспрессии указанных сигнальных молекул. [4, 8, 10, 15, 16, 17]. Более низкая экспрессия рассматриваемых сиртуинов и мелатонина и его рецепторов, а также больший уровень белков р16, р 21 и ВАХ выявлены у лиц, имеющих ДКМП, вне зависимости от возраста как в буккальном эпителии, так и в аутопсийном материале миокарда. Полученные данные свидетельствуют об участии этих молекул в патогенезе дилатационной кардиомиопатии.
По результатам проведенного исследования выявлено, что молекулярные профили у людей различных возрастных групп, определяемые по уровню экспрессии сигнальных молекул SIRT1, SIRT2, SIRT3, SIRT6, мелатонина и рецепторов к нему МТ-1, МТ-2, а также молекул р16, р21 и ВАХ в БЭ, достоверно различаются в зависимости от наличия ДКМП, что имеет важное значение для дифференциальной диагностики данного заболевания. Характерно, что направленность изменений в буккальном эпителии носит сходный характер с соответствующим молекулярным профилем в аутопсийном материале миокарда. Соответственно, уменьшение площади экспрессии сиртуина 1 в 1,7-2,5 раза, сиртуина 2 в 1,7-2,3 раза, сиртуина 3 в 2,2-2,5 раза, сиртуина 4 в 2,2-2,3 раза, сиртуина 6 в 1,6-2,3 раза может расцениваться как маркер формирования ДКМП для лиц средней и пожилой возрастных групп; для лиц старческого возраста таковыми являются снижение сиртуинов 1 и 2 в 6,7-7,3 раза, сиртуина 6 в 5,6 раза. Выявленные изменения экспрессии сиртуинов объясняются тем, что данные молекулы играют важную роль в патогенезе воспаления, старения сосудов и патологии сердца [4]. Сиртуины-1 и 2 обладают кардио- и вазопротекторным действием, которое реализуется в том числе за счет подавления воспаления, поддержания липидного баланса, уменьшения выраженности атеросклеротических изменений сосудистой стенки. [5, 16]. По результатам проведенных ранее исследований, снижение уровня их экспрессии в сердце и сосудистой сети отмечается при гипертрофии миокарда, сахарном диабете 2 типа, сердечной недостаточности [18-21]. Снижение сиртуина-3, выявленное у пациентов с ДКМП, взаимосвязано с повышенным повреждением кардиомиоцитов, ускорением процессов ремоделирования миокарда [6]. Сиртуин-6 регулирует различные клеточные процессы при старении клеток, его экспрессия изменяется при ряде хронических сердечно-сосудистых заболеваний [22].
В качестве маркера преждевременного старения миокарда и формирования ДКМП может использоваться оценка экспрессии мелатонина и его рецепторов МТ-1 и МТ-2 в буккальном эпителии. Диагностически значимым, на основе полученных результатов, может считаться снижение в 1,4-3,4 раза в среднем и пожилом возрасте; для лиц старческой возрастной группы информативным следует считать снижение экспрессии МТ-1 в 2 раза, МТ-2 в 4 раза. Данные изменения коррелируют со снижением экспрессии указанных сигнальных молекул в миокарде. Снижение экспрессии мелатонина и его рецепторов у пациентов, имеющих ДКМП, объясняется тем, что мелатонин является регулятором обмена глюкозы и энергетического метаболизма [12], его ключевые эффекты опосредованы через мембранные рецепторы MT-1 и MT-2 [7, 23]. MT-1 выполняет защитную роль при окислительном стрессе и воспалительных процессах [18, 24]. MT-2 является эндогенным защитным агентом против повреждения миокарда при ишемии/реперфузии [17].
Рассматривая процессы клеточного старения и апоптоза, нельзя не отметить и роль других сигнальных молекул – белков p16, p21 и BAX [14]. Длительная экспрессия p16 «подталкивает» клетки к старению, необратимой остановке клеточного цикла, которая предотвращает рост потенциальных раковых клеток, но также способствует клеточному старению. Белок р21 участвует в регуляции воспалительного и окислительного стресса [8]. Bcl-2-ассоциированный X-белок является регулятором внутреннего, так называемого «митохондриально регулируемого» пути клеточной гибели, участвуя в ключевых этапах апоптоза [9]. Физиологическая функция BAX обеспечивает тканевой гомеостаз, нарушение регуляции данного белка приводит к аберрантной гибели клеток [15]. При ДКМП наиболее выраженные изменения экспрессии данных молекул отмечены в кардиомиоцитах в виде увеличения экспрессии ВАХ в 1,4 раза в среднем возрасте и в 1,3-1,4 раза в пожилом возрасте. Статистически значимое увеличение экспрессии рассматриваемых маркеров старения р 16 и р 21 наблюдалось у лиц среднего возраста при ДКМП, в то время как в старших возрастных группах информативным было увеличение экспрессии только белка р16.
В связи с тем, что высокий уровень экспрессии сиртуинов способствует предотвращению развития дилатационной кардиомиопатии, инфаркта миокарда и эндотелиальной дисфункции, снижение уровня данной молекулы может рассматриваться в качестве одного из предикторов развития дисфункции миокарда и развития заболеваний сердца. Повышение экспрессии маркеров старения р16, р21 и апоптоза ВАХ, определяемое в биопсийном материале миокарда и культурах клеток миокарда, полученных от пациентов с ДКМП, может указывать на ускоренное старение сердечно-сосудистой системы.
Заключение. Молекулярные профили у лиц разного возраста с дилатационной кардиомиопатией, определяемые по уровню экспрессии сиртуинов 1, 2, 3, 6; мелатонина и рецепторов к нему МТ-1, МТ-2; а также белков р16, р21 и ВАХ в буккальном эпителии, достоверно различаются с соответствующими возрастными профилями при отсутствии сердечно-сосудистой патологии. При этом наблюдается взаимосвязь изменений экспрессии данных молекул в буккальном эпителии и аутопсийном материале миокарда. Полученные данные согласуются с результатами современных исследований, направленными на уточнение роли и значения оцениваемых в нашей работе сигнальных молекул в окислительном стрессе, воспалении и других патологических процессах, связанных с возраст-зависимыми состояниями.
Наибольшую информативность для оценки изменений миокарда, ассоциированных с ДКМП, имеет оценка площади следующих сигнальных молекул в буккальном эпителии: у пациентов среднего возраста – снижение уровня экспрессии SIRT3 и SIRT6 в 2,2-2,3 раза, мелатонина в 1,8 раза и его рецепторов МТ-1, МТ-2 – в 1,4-2,5 раза; у пациентов пожилого возраста – снижение экспрессии SIRT1, SIRT3 в 2,5 раза; SIRT2 в 2,3 раза; мелатонина и рецепторов к нему 1,4-1,8 раза; у пациентов старческого возраста – снижение экспрессии SIRT3, SIRT6 в 3,0-4,7 раза; SIRT1, SIRT2 в 6,7-7,3 раза; мелатонина в 2,8 раза; МТ-1 – в 4,1 раза и МТ-2 – в 23,7 раза. Дополнительную диагностическую информативность в диагностике ДКМП у лиц различных возрастных групп имеет повышение экспрессии белков р16 и ВАХ в 0,6-0,8 раза в буккальном эпителии.
Информация о финансировании
Финансирование данной работы не проводилось.





















Список литературы